��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����������ӵ���Һ�м���������NaOH��Һ�����ã����ˣ�ȡ������ϴ�Ӻ�������м������������ᣬ�õ�����Һ�����������ӵ�������ԭ��Һ ��ͬ����
��ͬ����
A��Na+��Ag+��Mg+
B��Fe2+��Mg2+��NH4+
C��Al3+��Ca2+��Cu2+
D��Mg2+��Fe3+��Cu2+
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
2��ѡ���� ��������ʵ�����ݵó��Ľ��۲���ȷ����
ѡ��
| ʵ������
| ����
|
A
| �����ʯ��ˮ��ͨ��ij���壬������ɫ����
| ������һ������CO2
|
B
| ��ij��Һ�еμ������ữ��BaCl2������ɫ����
| ����Һһ����SO42-
|
C
| ��ij�ε�ˮ��Һ�м����������Ƽ��ȣ�������ʹʪ��ĺ�ɫʯ����ֽ����������
| ����һ�������
|
D
| ���ˮ�еμӱ���FeCl3��Һ�õ����ɫҺ��
| ��Һ����Fe(OH)3����
�ο��𰸣�B
��������������ʯ��ˮ��ͨ��ij���壬������ɫ�����������岻һ����CO2��������SO2��Z��ȷ����ij��Һ�еμ������ữ��BaCl2������ɫ����������Һ���ܺ�SO42-�����ܺ��������ӣ���ѡB��
������������ĿҪ��ѧ�����ճ��������ʼ�ķ�Ӧ���ر������Ʒ�Ӧ�IJ�ͬ�㣺��CO2��SO2����ʹ����ʯ��ˮ����ǣ�ͨ��������ܱ���壻�����Ȼ��������ɳ����ļȿ����Ǻͱ����ӽ��Ҳ�����Ǻ������ӽ�ϡ�
�����Ѷȣ���
3��ʵ���� (6��)��һƿ������Һ�����ܺ���NH��4��K����Mg2����Ba2����Al3����Fe3����SO2�D 4��CO2�D 3��NO�D 3��Cl�D��I�D�ֽ�������ʵ�飺
��1����֪��Һ��ǿ���ԣ�
��2��ȡ��������CCl4������������ˮ��CCl4��Ϊ�Ϻ�ɫ��
��3����ȡ���μ�ϡNaOH��Һ��ʹ��Һ��Ϊ���ԣ��˹����о��������ɣ�
��4��ȡ��������������Һ����Na2CO3��Һ���ְ�ɫ������
��5����ʵ��(3)�еļ�����Һ���ȣ�������ų�����������ʹʪ��ɫʯ����ֽ������
�ʣ���ԭ��Һ�п϶����ڵ�������____________________��
�ڿ϶������ڵ�������______________________________��
�۲���ȷ���Ƿ���ڵ�������______________________________��
�ο��𰸣�
��NH��4��Ba2����I�D
��Mg2����Al3����Fe3����CO2�D 3��NO�D 3��SO2�D 4
��K����Cl�D
�����������
�����Ѷȣ���
4��ѡ���� ��������Һ�У���������һ���ܹ������������
A��ijǿ������Һ��Na+��Fe2+��Cl����ClO��
B�����������ܷų�����H2����Һ��K+��NH4+��SO42����CO32��
C��������pH��14����Һ��Al3+��Na+��Cl����HCO3��
D��������c(OH��)/c(H+)��1012����Һ��K+��Ba2+��Cl����NO3��
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
5������� �����⣨10�֣�ij��Һ�к���Ba2+��Cu2+, Ag+������NaOH��Һ�������Na2SO4��Һ��������������һ�������롣������ͼ������ʾ��д����Ѵ𰸣�
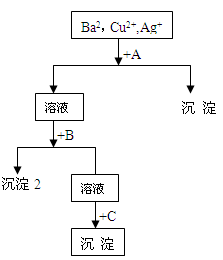
��1�������Ļ�ѧʽ������1 ������2 ������3 ��
��2��д�����Һ+A�����ӷ���ʽ�� ����Һ+B�����ӷ���ʽ�� ��
�ο��𰸣���1��AgCl, Cu(OH)2, BaSO4 ��2�� Ag+ + Cl- = AgCl�� Cu2+ + 2OH- = Cu(OH)2��
���������
�����������1����Һ����Ba2+��Cu2+��Ag+��Ӧ�ȼ���HCl������AgCl���������˺��ڼ���Na2SO4���ɵõ� BaSO4������������NaOH���ɵõ�Cu��OH��2���������Գ���1���Ȼ���������2��������ͭ������3�����ᱵ����2�����Һ+A��Ӧ�����ӷ���ʽΪAg++Cl-=AgCl������2ΪCu��OH��2����Һ+B��Ӧ�����ӷ���ʽΪ��Cu2++2OH-=Cu��OH��2�����ʴ�Ϊ��Ag++Cl-=AgCl����Cu2++2OH-=Cu��OH��2����
���㣺���ʵķ��롢�ᴿ�ͳ��ӣ����ӷ���ʽ����д
�����Ѷȣ�һ��
|