微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 标准状况下,在三个干燥的烧瓶内分别装入干燥纯净的NH3,含一半空气的氯化氢气体,NO2和O2按4∶1体积比混合的混合气体,然后分别做喷泉实验,三个烧瓶中所得溶液的物质的量浓度之比为
A.2∶1∶2
B.5∶5∶4
C.1∶1∶1
D.无法确定
参考答案:B
本题解析:
本题难度:一般
2、选择题 NO因污染空气而“臭名昭著”,而其奇妙作用也使其成为“明星分子”。如制HNO3肥料、炸药、促进血管扩张、促进免疫功能、增强记忆等。其工业主要来源可能是
A.Cu+HNO3→
B.N2+O2→
C.NH3+O2?→
D.NO2+H2O→
参考答案:C
本题解析:A通常在实验室中利用该反应;B反应在常温下很难进行;D选项原料污染大,不适用。故C正确。
点评:工业生产的前提应当是低成本,原料容易得到,整个过程不污染空气,这是关键。
本题难度:一般
3、选择题
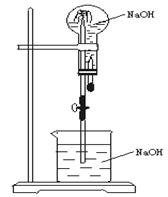
A.HCl和CO2
B.NH3和CH4
C.SO2和CO
D.NO和NO2
参考答案:A
本题解析:应选择极易与NaOH反应(或说极易被NaOH吸收)的物质。其中只有A符合。B中的CH4,C中的CO,D中的NO本身都不与NaOH反应,故不选。
注:如是混合气,则NO2与NO又为等摩尔混合时也可进行喷泉实验。因NO2+NO+2NaOH===2NaNO2+H2O。
本题难度:简单
4、选择题 下列试剂必须用棕色试剂瓶装的有(?)
①浓氨水?②氯水?③硝酸银?④浓硝酸?⑤浓盐酸?⑥溴化银
A.①②③④⑤⑥
B.②③④⑥
C.②③⑤⑥
D.①③④⑥
参考答案:B
本题解析:凡是见光易分解的物质及受热易分解的物质在实验室中都放在棕色试剂瓶中保存以避光。
本题难度:简单
5、计算题 铁与HNO3作用时,还原产物除与HNO3浓度有关外,还与温度有关。已知在与冷稀HNO3反应时,</PGN0076B.TXT/PGN>主要还原产物为NO气体;在与热的稀HNO3作用时,主要还原产物为N2O气体;当HNO3更稀时,其重要还原产物是NH4+。现有铁与稀HNO3的作用,请分析图10-3,回答有关问题。
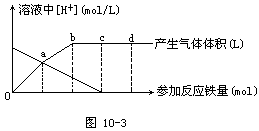
假设曲线的各段内只有一种还原产物。
(1)0点到a点的还原产物是______;
(2)a点到b点的还原产物是______,其原因是______;
(3)试完成b点到c点的反应方程式:
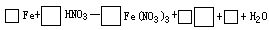
(4)反应过程中,到达______点时HNO3已完全反应。
(5)已知达到d点时,反应结束,此时溶液中的主要阳离子是______;
(6)c点和d点参加反应的铁的物质的量之比是______;
参考答案:(1)NO;(2)N2O,反应放热,使溶液温度升高;(3)8,30,8,3NH4NO3,9;(4)C;(5)Fe2+;(6)2∶3
本题解析:根据图形,应先对气体体积曲线和溶液中[H+]变化曲线作出正确判断。溶液中的[H+]逐渐减小,至c点为0,说明HNO3逐渐参与反应,到c点时恰好反应完全,即0点到c点是铁与HNO3的反应,c点到d点是生成的Fe(NO3)3与铁的反应,到d点时,溶液中生成的Fe(NO3)3完全反应,全部转化为Fe(NO3)2;搞清了[H+]浓度的变化曲线,也就不难理解气体曲线了,只要抓住题目中的已知和铁用量、转移电子数、产生NO或N2O体积的多少的关系及曲线斜率,就不难断定其主要还原产物了。oa:NO,ab:N2O;bc:NH4NO3;cd;Fe(NO3)2。计算c、d点参加反应的铁的物质的量之比时,要明确是0到c铁与HNO3反应生成的Fe(NO3)3,由2Fe(NO3)3+Fe=3Fe(NO3)2可知:生成的Fe(NO3)3的物质的量是cd段“Fe”物质的量的2倍,所以oc段参加反应的铁量是cd段的2倍,这也是本题的巧点。
本题难度:一般