| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ���ܽᡶ��������ԭ������Ƶ����ǿ����ϰ��2017�����°棩(��)
 2��ѡ���� һ�������£����ܱ������м���?X���ʣ�������Ӧ3X��g��?Y��g��+Z��g����H��0����Ӧһ��ʱ���ı�ijһ�������������Ӧ�и�ʱ��X���ʵ�Ũ�����±���ʾ������˵���в���ȷ���ǣ������� | |||||
| ��Ӧʱ�䣨min�� | 0 | 5 | 15 | 17 | 20 X��Ũ�ȣ�mol/L�� 1.0 0.4 0.4 0.7 0.7 |
3��ѡ���� ������ʵ��������������ԭ�������͵���
[? ]
A����ѹ������SO2��O2��Ӧ����SO3
B���¶ȹ��߶Ժϳɰ���Ӧ����
C�����¼������������ʹ�ϳɰ��ķ�Ӧ���ʼӿ�
D���ù�����������������FeS2���������ԭ�ϵ�������
4������� ��ҵ������Ϊԭ���Ʊ�����Ĺ�����ͼ1��ʾ��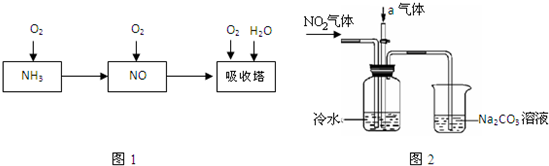
ij����С��ģ���������ֹ����������ͼ2��ʾʵ��װ���Ʊ����ᣨ��������Ʒ���ѱ���������
��1����ҵ���ð�����ȡNO�Ļ�ѧ����ʽ��______��
��2�����Ӻ�װ�ú����Ƚ��еIJ�����______��
��3��ͨ��a�����Ŀ����______��
��4��ʢ��Na2CO3��Һ���ձ�Ϊβ������װ�ã���װ���з�����Ӧ�Ļ�ѧ����ʽ��2NO2+Na2CO3�TNaNO2+______+______
��5����֪���¶ȵ���21.15��ʱ��NO2����ȫ��ת��ΪN2O2����ҵ�Ͽ���N2O4��ˮ��Ӧ�����������ʣ�N2O4��a��������ˮ����������Ļ�ѧ����ʽ��______��
��6��һ�������£�ij�ܱ�������N2O4��NO2�Ļ������ﵽƽ��ʱ��c��NO2��=0.500mol/L��c��N2O4��=0.125mol/L����2NO2��g��?N2O4��g����ƽ�ⳣ��K=______����NO2��ʼŨ��Ϊ2mol/L����ͬ�����£�NO2�����ת����Ϊ______��
5��ѡ���� �����£��ݻ���Ϊ2L���ܱ�����M��N�У��ֱ���������������ʼͶ�Ͻ����Ŀ��淴Ӧ��3A��g��+2B��g��?2C��g��+xD��s��?�Ļ�ѧƽ��״̬������������£�M��3molA?2molB��?2min�ﵽƽ�⣬����D1.2mol����ôӷ�Ӧ��ʼ��ƽ��C������Ϊ0.3mol/Lmin��N��2molC?ymolD��?�ﵽƽ��ʱc��A��=0.6mol/L�������ƶϵĽ����в���ȷ���ǣ�������
A��x=2
B��ƽ��ʱM��c��A��=0.6mol/L
C��y��0.8
D��y=2
|
||
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | ||
| ��һƪ���߿���ѧ֪ʶ����������ѧ��Ӧ��.. | ||
| �����Ŀ |