微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知R原子有b个中子,R2+核外有a个电子。表示R原子符号正确的是(? )
参考答案:C
本题解析:R原子有b个中子,R2+核外有a个电子,则原子核外的电子数是a+2,质子数是a+2,所以表示R原子符号正确的是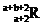 ,故选项的C。
,故选项的C。
本题难度:一般
2、选择题 H、D、T、H+可以用来表示(?)
A.同一种原子
B.化学性质不同的氢原子
C.同一种氢元素
D.氢的四种核素
参考答案:C
本题解析:元素是指具有相同的核电荷数即质子数的同一类原子的总成,而具有一定数目质子和一定数目中子的原子是核素,所以根据微粒的化学式可知,H、D、T、H+可以用来表示化学性质不同的氢原子,C正确,其余选项都是错误的,答案选C。
点评:该题主要是考查学生对元素以及核素概念的熟悉了解程度,意在巩固基础,提高学生的应试能力,调动学生的学习兴趣和学习积极性。
本题难度:简单
3、选择题 下列叙述正确的是?
A.人们已经发现了109种原子

C.H,D,H+,H-,T都是氢元素的微粒
D.最外层电子数相同的微粒化学性质相似
参考答案:B、C
本题解析:A.不正确。因为大多数元素都有同位素,因而发现的原子远远超过109种。D.不正确。如Ne和S2-最外层都为8个电子,但Ne很难得失电子,而S2-易失电子有强还原性。
本题难度:一般
4、选择题 根据元素周期表和元素周期律分析下面的推断,其中错误的是:
A.砹的氢化物不稳定
B.氢氧化锶比氢氧化钙的碱性强
C.铍的原子失电子能力比镁弱
D.硒化氢比硫化氢稳定
参考答案:D
本题解析:砹为六周期第七主族元素,所以其氢化物不稳定,锶比钙活泼,所以氢氧化锶比氢氧化钙的碱性强,铍比没有镁活泼,所以铍的原子失电子能力比镁弱,硒化氢比硫化氢更不稳定,所以ABC的叙述式正确的,D是错误的,答案为D。
点评:该题考查了元素周期表和元素周期律,是高考考查的重点,本题信息量较多,但是难度适中。
本题难度:简单
5、填空题 (共8分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
?
| IA
| ?
| ?
| ?
| ?
| ?
| ?
| 0
|
1
| ①
| ⅡA
| ⅢA
| ⅣA
| ⅤA
| ⅥA
| ⅦA
| ?
|
2
| ?
| ?
| ?
| ②
| ③
| ④
| ?
| ?
|
3
| ⑤
| ?
| ⑥
| ?
| ⑦
| ?
| ⑧
| ?
|
(1)、④、⑤、⑥的原子半径由大到小的顺序为 (填元素符号)。
②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是 (填化学式)。
(2)、①、④、⑤、⑧四种元素中,某些元素间可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: 。
(3)、由表中两种元素的原子按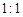 组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号) 。
组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号) 。
a.MnO2? b.Na2SO4? c.Na2SO3? d.CaCO3
(4)、由表中元素形成的物质X、Y、Z、M、N可发生以下反应:?
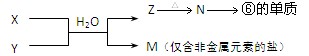
X溶液与Y溶液反应的离子方程式为 ;
常温下,为使0.1 mol/L M溶液中电离出的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至pH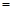 。
。
参考答案:(1).? Na>Al>O? (1分)? HClO4>H3PO4> H2CO3? (1分)
(2).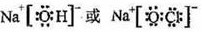 ? (1分)?(3). a? (1分)
? (1分)?(3). a? (1分)
(4).Al3++3NH3?H2O→Al(OH)3↓+3NH4+? (2分)? pH=7? (2分)
本题解析:根据元素在周期表中的位置可知,①-⑧分别是H、C、N、O、Na、Al、P、Cl。
(1).同周期自左向右原子半径逐渐减小,金属性逐渐减弱,非金属性逐渐增强。同主族自上而下,原子半径逐渐增大,金属性逐渐增强,非金属性逐渐减弱。非金属性越强,最高价氧化物的水化物的酸性越强,所以答案是Na>Al>O 、 HClO4>H3PO4> H2CO3。
(2)符合条件的是氢氧化钠或次氯酸钠,电子式分别是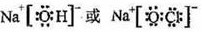
(3)该液态化合物是双氧水,常用二氧化锰作催化剂,答案选a。
(4)M是只含有非金属元素的盐,因此是铵盐。X和Y的反应应该是复分解反应,所以Z是沉淀,即为氢氧化铝,氢氧化铝加热分解得到氧化铝,氧化铝电解得到单质铝。所以X、Y分别是铝盐和氨水。M中NH4+水解显酸性,所以应该加入氨水,才有可能使M溶液中电离出的阴、阳离子浓度相等。根据电荷守恒可知,当pH=7时即可。
本题难度:一般