微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离,其流程如右图所示。下列说法正确的是(?)
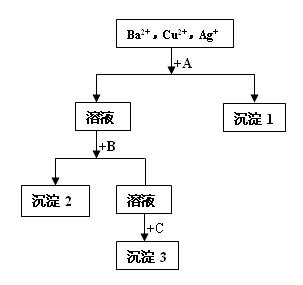
A.试剂A为Na2SO4溶液
B.沉淀3的化学式可能是BaSO4
C.生成沉淀1的离子方程式为:Cu2+ + 2OH- = Cu(OH)2↓
D.生成沉淀2的离子方程式为:Ag++ Cl- = AgCl↓
参考答案:B
本题解析:略
本题难度:简单
2、填空题 某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;将沉淀过滤、洗涤、灼烧,得到1.6g固体;向上述滤液中加入足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。
回答下列问题:
(1)原溶液中一定不存在 。
(2)根据实验和必要的计算确定溶液中一定存在的离子有哪些 (写出必要的推理及计算过程)。
参考答案:(1)CO32-(2分)(2)Fe3+、NH4+、SO42-和Cl-(2分)
本题解析:加入NaOH溶液共热有气体和红褐色沉淀,知溶液含NH4+、Fe3+,而不含CO32-,加BaCl2溶液生成不溶于盐酸的沉淀,知溶液中含SO42-。n(NH3)=0.02mol,知n(NH4+)=0.02mol,n(Fe2O3)=1.6g/160g・mol-1=0.01mol,知n(Fe3+)=0.02mol,n(BaSO4)=4.66g/233g・mol-1=0.02mol,知n(SO42-)=0.02mol,溶液中NH4+、Fe3+所带正电荷为0.02mol+3×0.02mol=0.08mol,SO42-所带负电荷为2×0.02mol=0.04mol,据电荷守恒,知溶液中必然大量存在另一种阴离子,由题意知为Cl-,综上知,原溶液中一定含Fe3+、NH4+、SO42-和Cl-。
考点:考查溶液中离子的共存和离子的判断,同时考查了电荷守恒原理的运用。
本题难度:困难
3、选择题 下列物质混合发生化学反应,且反应属于离子反应的是:
A.H2和O2反应生成水
B.锌片投入稀硫酸中
C.K ClO3(固体)和MnO2(固体)混合加热制O2
ClO3(固体)和MnO2(固体)混合加热制O2
D.NaOH溶液和K2SO4溶液混合
参考答案:B
本题解析:略
本题难度:简单
4、选择题 常温时,某无色溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该无色溶液中一定大量共存的离子组是( )
A.AlO2-、K+、NH4+、Na+
B.I-、Ca2+、HCO3-、Na+
C.MnO4-、SO42-、K+、Al3+
D.Na+、SO42-、Cl-、NO3-
参考答案:A.AlO2-在酸性条件下不能大量共存,故A错误;
B.无论溶液呈酸性还是碱性,HCO3-都不能大量共存,故B错误;
C.MnO4-有颜色,与题目无色不符,故C错误;
D.溶液无色,无论溶液呈酸性还是呈碱性,离子之间不发生任何反应,可大量共存,故D正确.
故选D.
本题解析:
本题难度:简单
5、选择题 常温下,下列各组离子在指定溶液中能大量共存的是?(?)
A.pH=11的溶液中:Na-、K+、HS-、ClO-
B.加入铝片能产生氢气的溶液中:Ba2+、K+、SO42-、HCO3-
C.c(H+)=c(OH-)的溶液中:NH4+、Fe3+、NO3-、Cl-
D.c(Cu2+)=0.1mol/L的溶液中:K+、NH4+、SO42-、Br-
参考答案:D
本题解析:略
本题难度:简单