|
|
|
高考化学必考知识点《物质的量》答题技巧(2017年最新版)(六)
2017-03-05 15:15:16
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 设NA为阿伏加德罗常数的值。下列叙述错误的是
A.常温常压下,0.17g NH3中含有的共用电子对数为0.1NA
B.常温常压下,1 L pH=1的稀H2SO4中含有的氢离子数为0.1NA
C.标准状况下,2.24 L C12与足量稀NaOH反应转移电子数为0.1NA
D.10 g由CaCO3与KHCO3组成的混合物中含有的碳原子数为0.1NA
参考答案:A
本题解析:A、1个NH3分子中含有3个共用电子对,故0.17g NH3中含有的共用电子对数为0.03NA,错误;B、根据pH计算氢离子浓度,与几元酸无关,正确;C、 与稀NaOH反应既是氧化剂又是还原剂,反应中0.1molC12转移电子数为0.1NA,正确;D、CaCO3与KHCO3摩尔质量相同为100g/mol,碳原子数相同,正确。
本题难度:一般
2、选择题 向KI溶液中加入AgNO3溶液,直到恰好完全反应,反应后溶液的质量恰好等于原KI溶液的质量,则原AgNO3溶液的质量分数为
A.72.3%
B.50%
C.48.3%
D.38%
|
参考答案:A
本题解析:
试题解析:由题意可知:m(KI溶液)+m(AgNO3溶液)=m(AgI)+m(KNO3溶液),生成的新溶液的质量与原碘化物溶液的质量相等,根据质量守恒,则有m(AgNO3溶液)=m(AgI),设生成1molAgI,则AgNO3为1mol,m(AgNO3)=170g,则ω(AgNO3)=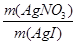 ×100%= ×100%=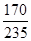 ×100%≈72.3%,故A正确。 ×100%≈72.3%,故A正确。
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算
本题难度:一般
3、计算题 硫有多种化合物,许多含硫化合物在工业上有重要的用途。
(1)工业上可用黄铁矿、焦炭在有限的空气中燃烧制备硫磺。
3FeS2 + 12C+ 8O2  Fe3O4 + nA↑+ 6S Fe3O4 + nA↑+ 6S
A是?(写化学式)。若得到192克的硫磺,则产生标准状况下的A气体?L。?
(2)硫的氯化物常做橡胶工业的硫化剂。硫与氯气在一定条件下反应,得到两种硫的氯化物B和D。B物质中的含硫量为0.3107,D物质中的含氯量为0.5259,B的相对分子质量比D小32。计算确定这两种氯化物的分子式分别为?。
(3)硫化氢有毒。在120℃、101kPa,将H2S和O2在密闭容器中点燃,充分反应后又恢复到了原来的温度和压强时,气体体积减少30%,求原混合其气体中H2S的体积分数。写出推导过程。(不考虑硫化氢的分解)
(4)硫代硫酸钠是重要的还原剂,可用亚硫酸钠和硫粉在水溶液中加热制得。取15.12g Na2SO3溶于80.0mL水中,加入5.00g硫粉,用小火加热至微沸,反应约1小时后过滤,将滤液蒸发至体积为30.0mL,再冷却到10℃,则理论上析出Na2S2O3?5H2O多少克?写出推导过程。(已知:Na2S2O3的溶解度,10℃时为60.0g/100g水,100℃时为207g/100g水。100℃时,Na2S2O3饱和溶液的密度为1.14g/mL)。
参考答案:(1)CO? 268.8?(各1分)?
(2)SCl2、S2Cl2?(各2分)
(3)0.7或0.3?
(4)23.4
本题解析:(1)根据原子守恒可知,A应该是CO,且n=12。192克的硫磺的物质的量=192g÷32g/mol=6mol,所以根据方程式可知,生成的CO是6mol×2=12mol,则CO在标准状况下的体积是12mol×22.4L/mol=268.8L。
(2)B物质中的含硫量为0.3107,则B分子中S和Cl的原子个数之比=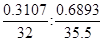 =1:2。D物质中的含氯量为0.5259,则D分子中S和Cl的原子个数之比= =1:2。D物质中的含氯量为0.5259,则D分子中S和Cl的原子个数之比=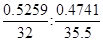 =1:1。又因为B的相对分子质量比D小32,所以B和D的化学式分别是SCl2、S2Cl2。 =1:1。又因为B的相对分子质量比D小32,所以B和D的化学式分别是SCl2、S2Cl2。
(3) H2S燃烧的有关方程式是2H2S+ O2 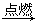 2S+ 2H2O(1)? 2H2S+ 3O2? 2S+ 2H2O(1)? 2H2S+ 3O2?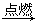 ?2SO2+ 2H2O(2) ?2SO2+ 2H2O(2)
由反应知,当H2S:O2>2:1时,按(1)进行,气体体积可能减少30%;
当2:1>H2S:O2>2:3时既有反应(1)又有反应(2)
设原混合气体中H2S、O2分别为x、yL,气体体积可能减少30%
Ⅰ? 2H2S+ O2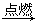 2S+ 2H2O?气体体积减少 2S+ 2H2O?气体体积减少
2? 1? 2? 1
2y?y? 2y?y?
所以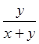 =0.3 =0.3
解得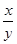 = =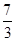
因此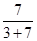 =0.7 =0.7
Ⅱ? xH2S+ yO2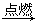 (y-x/2)SO2+(1.5x-y)S+ xH2O?气体体积减少 (y-x/2)SO2+(1.5x-y)S+ xH2O?气体体积减少
x? y? (y-x/2)? x?x/2
所以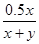 =0.3 =0.3
解得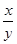 = =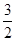
所以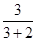 =0.6 =0.6
(4)n(Na2SO3)=15.12g÷126g/mol=0.12mol、n(S)=5.00g÷32g/mol=0.16mol (S过量)?
根据100℃的溶解度计算可知,微沸时生成的硫代硫酸钠全部溶解。设析出Na2S2O3?5H2Oxg
所以根据原子守恒可知,滤液中Na2S2O3有0.12mol,其质量是18.96g。10℃30.0ml溶液中水=30×1.14-18.96=15.24g,所以有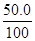 = =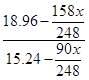 ,解得x=23.4。 ,解得x=23.4。
本题难度:一般
4、选择题 浓度不等的两种硫酸等质量混合后,溶液的质量分数为a%,而等体积混合时,质量分数则为b%;浓度不同的两种乙醇溶液等质量混合后,其质量分数也为a%,而等体积混合时,质量分数则为c%,那么a、b、c数值关系为
A.a>b>c
B.b>a>c
C.c>b>a
D.c>a>b
|
参考答案:B
本题解析:两种溶液的质量分数分别是x y,其中x<y,对于硫酸溶液,等质量(假设都是m g)混合之后,混合溶液质量分数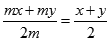 ,等体积混合时,由于质量分数小的硫酸密度比较小,等体积的两种硫酸,质量分数大的质量大,那么等体积混合相当于先将二者等质量混合,然后再加入一定量的高质量分数组分的硫酸,因此混合溶液质量分数>
,等体积混合时,由于质量分数小的硫酸密度比较小,等体积的两种硫酸,质量分数大的质量大,那么等体积混合相当于先将二者等质量混合,然后再加入一定量的高质量分数组分的硫酸,因此混合溶液质量分数>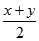 ,同样,对于乙醇溶液,等质量混合时其浓度依然是
,同样,对于乙醇溶液,等质量混合时其浓度依然是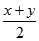 ,等体积混合时,由于质量分数小的乙醇溶液密度比较大(因为乙醇的密度比水小),等体积的两种乙醇溶液,质量分数大的质量小,那么等体积混合相当于先将二者等质量混合,然后再加入一定量的低质量分数组分的乙醇溶液,因此混合溶液质量分数<
,等体积混合时,由于质量分数小的乙醇溶液密度比较大(因为乙醇的密度比水小),等体积的两种乙醇溶液,质量分数大的质量小,那么等体积混合相当于先将二者等质量混合,然后再加入一定量的低质量分数组分的乙醇溶液,因此混合溶液质量分数<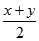 ,则有b>a>c,故选B.
,则有b>a>c,故选B.
考点:质量分数
本题难度:一般
5、选择题 设NA为阿伏加德罗常数,下列说法中正确的是
A.NA个氢气分子所占的体积为22.4L
B.2NA个二氧化碳分子的质量为44g
C.1000mL0.1mol/L 的NaCl溶液中,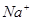 与
与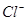 离子总数为0.2NA
离子总数为0.2NA
D.17g氨气中所含原子数为NA
参考答案:C
本题解析:阿伏伽德罗常数NA在含义上就是指1mol粒子的粒子数.或者1NA粒子的物质的量就是1mol。
A、没表明标准状况下,不能用22.4L/mol,所以A错误;
B、2NA个二氧化碳分子,也就是2mol,即其的质量为88g,所以错误;
C、NaCl溶液中的电解质NaCl是全部电离的,所以正确;
D、17g氨气中所含原子数为3NA,所以错误。
故选C。
点评:题主要考查了物质的量微粒数、阿伏伽德罗常数、质量等定量关系,一般求粒子的质量或微粒数要通过物质的量这个桥梁。
本题难度:一般
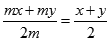 ,等体积混合时,由于质量分数小的硫酸密度比较小,等体积的两种硫酸,质量分数大的质量大,那么等体积混合相当于先将二者等质量混合,然后再加入一定量的高质量分数组分的硫酸,因此混合溶液质量分数>
,等体积混合时,由于质量分数小的硫酸密度比较小,等体积的两种硫酸,质量分数大的质量大,那么等体积混合相当于先将二者等质量混合,然后再加入一定量的高质量分数组分的硫酸,因此混合溶液质量分数>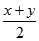 ,同样,对于乙醇溶液,等质量混合时其浓度依然是
,同样,对于乙醇溶液,等质量混合时其浓度依然是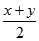 ,等体积混合时,由于质量分数小的乙醇溶液密度比较大(因为乙醇的密度比水小),等体积的两种乙醇溶液,质量分数大的质量小,那么等体积混合相当于先将二者等质量混合,然后再加入一定量的低质量分数组分的乙醇溶液,因此混合溶液质量分数<
,等体积混合时,由于质量分数小的乙醇溶液密度比较大(因为乙醇的密度比水小),等体积的两种乙醇溶液,质量分数大的质量小,那么等体积混合相当于先将二者等质量混合,然后再加入一定量的低质量分数组分的乙醇溶液,因此混合溶液质量分数<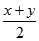 ,则有b>a>c,故选B.
,则有b>a>c,故选B.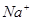 与
与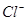 离子总数为0.2NA
离子总数为0.2NA