��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������У���OH-������ͬ�������͵��������ǣ�������
A��O2-
B��F-
C��NH3
D��NH4+
�ο��𰸣�OH-��������Ϊ8+1=9��OH-�ĵ�����Ϊ9+1=10��
A��O2-��������Ϊ8��������Ϊ8+2=10����A����
B��F-������������9��������Ϊ9+1=10����B��ȷ��
C��NH3��������Ϊ7+3=10��������Ϊ+3=10=10����C����
D��NH4+��������Ϊ7+4=11��������Ϊ11-1=10����D����
��ѡB��
���������
�����Ѷȣ�һ��
2������� A+��B-��C��D�������о�����ԭ�ӣ��ҵ���������Ϊ10������Һ�е�A+��B-�ڼ���ʱ���Ӧ��ת��ΪC������D����A+Ϊ______��B-Ϊ______��C��D�ֱ�Ϊ______��______��
�ο��𰸣�������10e-�ĺ���H����������OH-����������NH4+��H3+O��������CH4��NH3��H2O��HF�����������ܹ��ڼ���ʱ������Ӧ�������ַ��ӵ�ֻ����OH-��NH4+�������ӷ���ʽ��
OH-+NH4+�TH2O+NH3���� A+��B-��C��D�������ֱ�Ϊ NH4+��OH-��H2O��NH3���ʴ�Ϊ��NH4+��OH-��H2O��NH3��
���������
�����Ѷȣ�һ��
3������� A��B��C��D��E��F���ֶ�����Ԫ�ص�ԭ��������������A�������к������Ԫ�أ�BԪ�ص�ԭ�Ӽ۵����Ų�Ϊnsnnpn��DԪ�ص�����������������Ӳ�����3����F������������Ӧˮ���������ԣ�������C��E������������Ӧˮ�����У��Իش�
��1��д��Cԭ�ӵļ۲���ӹ����ʾʽ��______��Dԭ�ӵļ۲�����Ų�ʽ��______��E��ԭ�ӽṹʾ��ͼ��______��
��2��Bλ��Ԫ�����ڱ��ĵ�______�壬A��B�γ�ԭ�Ӹ�����1��1��ֱ���η��ӵĽṹʽ��______��
��3��C�Ļ�̬ԭ�Ӻ�����______�ֲ�ͬ�˶�״̬�ĵ��ӣ�
��4��E�����ڿ�����ȼ��������ĵ���ʽ��______�����е��������������ӵĸ�������______��
��5��F�Ĺ�̬���������;��______��˵��һ�֣���F�ĵ��ʡ�ʯī�Ͷ������ѣ�TiO2����������ϣ������·�Ӧ�õ������ֻ������������Ԫ����ɣ��Ҷ��������մɲ��ϣ��ڻ���͵���������ҪӦ�ã����䷴Ӧ�Ļ�ѧ����ʽ��______��
�ο��𰸣�A�������к������Ԫ�أ�����A��HԪ�أ�BԪ�ص�ԭ�Ӽ۵����Ų�Ϊnsnnpn��nΪ2�����Լ۵����Ų�Ϊ2s22p2��ΪCԪ�أ�DԪ�ص�����������������Ӳ�����3�������Ӳ�����2������������������6��ΪOԪ�أ���C��NԪ�أ�F������������Ӧˮ���������ԣ�����F��ClԪ�أ�������C��E������������Ӧˮ�����У���E��ԭ������С��F������E��NaԪ�أ�
��1��ͨ�����Ϸ���֪��C��NԪ�أ���ԭ�Ӽ۵��Ӳ�����5�����ӣ�2s�������2�����ӣ�2p��3�����ӣ��ֱ��ڲ�ͬ�Ĺ����������������ͬ����۵��ӵĹ����ʾʽΪ��
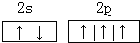
��D����Ԫ�أ��۵��������������ӣ���6�����ӣ�2s�������2�����ӣ�2p��4�����ӣ���۵����Ų�ʽΪ��2s22p4��E����Ԫ�أ�ԭ�Ӻ�����11�����ӣ���ԭ�ӽṹʾ��ͼΪ��
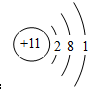
��
�ʴ�Ϊ��

��2s22p4��

��
��2������Ԫ�ص�������������������������̼Ԫ�����������4�����ӣ�����λ�ڵ�IVA�壻H��C�γ�ԭ�Ӹ�����1��1��ֱ���η�������Ȳ�����ĽṹʽΪ��H-C��C-H��
�ʴ�Ϊ��IVA��H-C��C-H��
��3��ԭ�Ӻ�������ӵ��˶�״̬������ͬ������ԭ�Ӻ����м������Ӿ��м����˶�״̬��Nԭ�Ӻ�����7�����ӣ�������7���˶�״̬��
�ʴ�Ϊ��7��
��4�����ڿ�����ȼ�����ɹ������ƣ����������������Ӻ���������֮��������Ӽ�����ԭ�Ӻ���ԭ��֮����ڹ��ۼ��������ʽΪ��
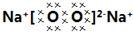
��һ���������ƻ�ѧʽ�к���2�������Ӻ�һ�����������ӣ����������Ӻ������Ӹ���֮��Ϊ2��1��
�ʴ�Ϊ��
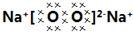
��2��1��
��5���������۵�ܸߣ����Կ��������ͻ���ϣ�ש��������ʯī�Ͷ������ѣ�TiO2����������ϣ������·�Ӧ�õ������ֻ������������Ԫ����ɣ��Ҷ��������մɲ��ϣ��ڻ���͵���������ҪӦ�ã�������������ֱ�����������̼���ѣ���Ӧ����ʽΪ��4Al+3TiO2+3C?����?.?2Al2O3+3TiC��
�ʴ�Ϊ���ͻ���ϣ�4Al+3TiO2+3C?����?.?2Al2O3+3TiC��
���������
�����Ѷȣ�һ��
4��ѡ���� ���и����У��������Ӳ���������ﵽ2n2�����ǣ�������
A��Ne��Ar
B��Al3+��S2-
C��F-��Na+
D��Ne��Cl-
�ο��𰸣��������Ӳ���������ﵽ2n2����������������������8��������㲻����18�������������㲻����32����
��n=1ʱ�����Ӳ�ֻ��һ������һ���Ӳ�Ҳ����������Ӳ㣬�����2�����ӣ�
��n=2ʱ��������ǵڶ����Ӳ㣬�����8�����ӣ������Ӳ��ܴﵽ2n2�����ӣ�����ֻҪ�����������10����ԭ�ӻ����Ӷ��ɣ�
��n=3ʱ��������ǵ������Ӳ㣬�����8�����ӣ����Ǹ����Ӳ��ܴﵽ2n2�����ӣ�������ȥ��
���Է�������������2�����ӻ�10�����ӵ�ԭ�ӻ����ӣ�
A��Ar�������������ʴ���
B��S2-�������������ʴ���
C��F-��Na+�������Ӳ���������ﵽ2n2��������ȷ��
D��Cl-�������������ʴ���
��ѡC��
���������
�����Ѷȣ�һ��
5��ѡ���� ԭ������Ϊ1-18�ŵ�Ԫ���У�����������ȷ���ǣ�������
A�������ֻ��1�����ӵ�Ԫ��һ���ǽ���Ԫ��
B�������ֻ��2�����ӵ�Ԫ��һ���ǽ���Ԫ��
C��ԭ�Ӻ�������������ȵ�Ԫ��һ���ǽ���Ԫ��
D���˵����Ϊ17��Ԫ�ص�ԭ���ڻ�ѧ��Ӧ�����õ�1������
�ο��𰸣�CD
���������
�����Ѷȣ�һ��