��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� Ŀǰ������60%��þ�ǴӺ�ˮ����ȡ�ģ���ˮ��þ����Ҫ�������£�

��ش��������⣺
��1�������ӷ�Ӧ�ĽǶ�˼������ˮ�м���ʯ�����������______��д���ڳ������з�Ӧ�����ӷ���ʽ______��
��2��ʯ��������ʯ����ˮ�γɵĻ����ӳ�����ú���ѧ��Դ����߾���Ч��ĽǶȣ�������ʯ�ҵ���Ҫԭ����Դ�ں����е�______��
��3������A��______������B��______��
��4������������Լ�a��______���ѧʽ����
��5����ˮMgCl2������״̬�£�ͨ��������Mg��Cl2���÷�Ӧ�Ļ�ѧ����ʽ��______���ӿ��dzɱ��ͷ���ѭ�����õĽǶȣ�������������������______��
��6����ˮ��þ�Ĺ��̣�ΪʲôҪ����ˮ�е��Ȼ�þת��Ϊ������þ����ת��Ϊ�Ȼ�þ��______��
�ο��𰸣���1��þ�����������������ӷ�Ӧ����������þ������Mg2++2OH-=Mg��OH��2����д���ӷ���ʽʱ������þ����д��ѧʽ��
�ʴ�Ϊ������Mg2+����ʹMg2+�γ�Mg��OH��2��������Mg2++2OH-�TMg��OH��2����
��2�����ǻ�ĵ�ÿǵ���Ҫ�ɷ�Ϊ̼��ƣ��ʴ�Ϊ�����ǣ���ĵ�ÿǵȣ���
��3�����벻����ˮ�Ĺ����Һ�壬���ù��˵ķ������ӳ������еõ�������þ�ù��˵ķ��������Ȼ�þ��Һ�еõ���ˮ���Ȼ�þ�����ᾧˮ��ʧ��ͨ������Ũ���������ᾧ�ķ��������ˮ���Ȼ�þ��
�ʴ�Ϊ�����ˣ�����Ũ�����������ᾧ����
��4����������þ���Ȼ�þ��������þ�����ᷴӦ�õ��Ȼ�þ��ˮ����Ӧ�Ļ�ѧ����ʽΪ��Mg��OH��2+2HCl=MgCl2+2H2O������������Լ�a��HCl��
�ʴ�Ϊ��HCl��
��5����ˮMgCl2������״̬�£�ͨ�������������ʧȥ������������������þ���ӵõ���������þ���ʣ������Ȼ�þ�������Mg��Cl2��������������������Ӧ�����Ȼ��⣬��ѭ��ʹ�ã�
�ʴ�Ϊ��MgCl2�����ڣ�ͨ��.Mg+Cl2���������ᣬѭ��ʹ�ã�
��6������ˮ�е��Ȼ�þ����������δ������þ����Ũ�Ⱥܵͣ�ֱ�Ӽ���Ũ����ȡ�����Ĵ����ĵ��ܣ��ɱ��ߣ�����ȡ���Ȼ�þ���л��д����������Ȼ����ε����ӣ������뽫��ˮ�е��Ȼ�þת��Ϊ������þ����ת��Ϊ�Ȼ�þ��
�ʴ�Ϊ����ˮ���Ȼ�þ�ĺ����ܴ�þ����Ũ�Ⱥܵͣ��ù��̿���ʹþ���Ӹ�����Ũ�ȸߣ��ҳɱ��ͣ�
���������
�����Ѷȣ�һ��
2��ѡ���� ����ͨѶ��һ���ִ�����ͨѶ�ֶΣ�����ͨѶ������һ�Թ��˿�ͬʱ����3���ŵ绰��������ά����Ҫԭ����SiO2�����й���SiO2��˵����ȷ����
A.SiO2��Ħ��������60
B.1 molSiO2���1 molO2
C.1.5 molSiO2�к���18.06��1023����ԭ��
D.1 molSiO2��������60 g��mol-1
�ο��𰸣�C
���������1.5 molSiO2�к���ԭ��3 mol����������ԭ����Ϊ��6.02��1023��3��18.06��1023��
Ħ�������ĵ�λ��g��mol-1���������ĵ�λ��g��
�����Ѷȣ�һ��
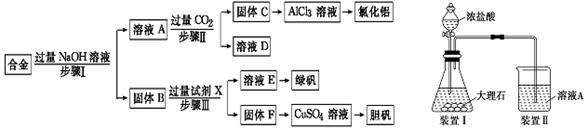
3��ʵ���� Ϊ̽����ҵ���ϵ������ã�ij��ѧ��ȤС�������������ͼʵ�鷽�����ú�����������ͭ�ĺϽ���ȡ�Ȼ������̷�����(FeSO4��7H2O)�͵������塣
��ش�
��1��������о�����е�ʵ�������?���ò����г��õ��ձ��Ͳ������⣬�������õ��IJ���������?��
��2����ҺA�е�������Ҫ��Na����OH����?���Լ�X��?��
��3�����в����ʱ����С����������ͼ��ʾװ�ü��Լ����Ƶõ�CO2����ͨ����ҺA�С�һ��ʱ���
�۲쵽�ձ��в����İ�ɫ�������٣���ԭ����(�����ӷ���ʽ��ʾ)?��Ϊ�˱������C���٣��Ľ��Ĵ�ʩ����װ�â�֮������һ��ʢ�б���?��Һ��ϴ��ƿ��
��4������ҺE�л���̷������ʵ���������Ϊ����������ƣ�?����ȴ�ᾧ������ϴ�ӡ�
�ο��𰸣���1������?©��?��2��AlO2-?ϡ����
��3��Al(OH)3��3H����Al3����3H2O? NaHCO3?��4��������Ũ��
�����������1����������ͼ��֪��������о��õ���Һ���壬��˵��������е�ʵ������ǹ��ˡ��ڹ��˲����г��õ��ձ��Ͳ������⣬�������õ��IJ���������©����
��2����������ͭ�ĺϽ���ֻ�н��������Ժ�ǿ�Ӧ����ƫ�����ƺ�������������ҺA�ijɷ���ƫ�����ƺ������������ƣ���˺��е�������Na����OH����AlO2-��ͭ���ܺ�ϡ���ᷴӦ�������Ժ����ᷴӦ��������ҺF������������ϡ����Ļ��Һ������F�ǽ���ͭ��Cu�м���ϡ�����H2O2�����Ʊ��������壬��Ӧ����ʽΪCu+H2SO4+3H2O+H2O2��CuSO4?5H2O��
��3��Ӧ��Ũ�����ӷ����������ɵ�CO2�����к����Ȼ������壬�������������ܽ��������У���˹���C���٣���Ӧ�����ӷ���ʽΪAl(OH)3��3H����Al3����3H2O��Ϊ�˱������C���٣��ͱ����ȥCO2�����л��е��Ȼ������壬���ԸĽ��Ĵ�ʩ����װ�â�֮������һ��ʢ�б���NaHCO3��Һ��ϴ��ƿ��
��4�������Һ���Ʊ��̷�ʱӦ�Ƚ���Һ����Ũ����Ȼ����ȴ�ᾧ�����ɵõ��̷���
�����Ѷȣ�һ��
4��ѡ���� ������������ϩ�����Ȼ�̼�����ķ�����
A���ǻ���Ӧ
B����ˮ
C��Һ��
D��������Ӧ
�ο��𰸣�B
�����������ϩʹ��ˮ��ɫ�����Ȼ�̼�м�����ˮ���ֲ㣬�²���ɫ����м�����ˮ�ֲ㣬�ϲ���ɫ��������ʵ����������ͬ���ʿ�����ˮ���������ǡ���ȷѡ��ΪB��
�����Ѷȣ�һ��
5��ѡ���� ����ƿʧȥ��ǩ����Һ�����Ƿֱ�Ϊ����Ba(NO3)2��KCl��NaOH��CuSO4��Na2SO4��������������κ��Լ���������ֽ����������ķ���������һһ���������������еļ���˳���У����������(? )
A���ۢܢ٢ݢ�? B���ܢڢۢݢ�? C���٢ݢۢܢ�? D�ܢۢ٢ݢ�
�ο��𰸣�D
���������������ƿ��Һ�У�ͭ����������ɫ�ģ����������������������ͭ�������������ơ�ֻ��ѡD��
�����Ѷȣ�һ��