微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下,纯水中存在电离平衡:H2O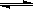 H++OH-。欲使水的电离平衡向正方向移动,并使c(OH-)增大,应加入的物质是
H++OH-。欲使水的电离平衡向正方向移动,并使c(OH-)增大,应加入的物质是
A.H2SO4
B.AlCl3
C.NaHCO3
D.NaOH
参考答案:C
本题解析:加入酸、碱将抑制水的电离,排除AD;
BC两物质水解促进水的电离,AlCl3使溶液呈酸性,c(OH-)减少,而NaHCO3将使溶液呈碱性,c(OH-)增大,故答案为C
本题难度:简单
2、选择题 甲、乙两个容器内都在进行A→B的反应,甲中每分钟减少4 mol A,乙中每分钟减少2 mol A,则两容器中的反应速率
[? ]
A.甲快
B.乙快
C.相等
D.无法确定
参考答案:D
本题解析:
本题难度:简单
3、选择题 1mol X气体跟a mol Y气体在体积可变的密闭容器中发生如下反应: X(g)+a Y(g) b Z(g)反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是
b Z(g)反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是
[? ]
A.a=1,b=1
B.a=2,b=1
C.a=2,b=2
D.a=3,b=2
参考答案:AD
本题解析:
本题难度:一般
4、填空题 根据反应:mA(g) + nB(g) pC(g)?△H,结合图中所给的信息填空。
pC(g)?△H,结合图中所给的信息填空。
(填“>”、“=”或“<”)

 ______
______ ?
? ______
______ ?
?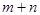 ______
______
参考答案:>? <? >
本题解析:对比曲线T2P2和T1P2,相同压强条件下,曲线T1P2先达到平衡状态,故 >
> ;对比曲线T1P1和T1P2,相同温度下,曲线T1P2先拐,即先达到平衡状态,故
;对比曲线T1P1和T1P2,相同温度下,曲线T1P2先拐,即先达到平衡状态,故 <
< ;由曲线T1P1到曲线T1P2,增大压强,生成物C的体积分数增大,则反应正向进行,由增大压强,反应向气体分子数减小的方向移动,故?
;由曲线T1P1到曲线T1P2,增大压强,生成物C的体积分数增大,则反应正向进行,由增大压强,反应向气体分子数减小的方向移动,故?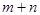 >
> 。
。
点评:化学平衡图像是化学平衡的一个重要知识点,历年高考经常考查,考生在备考过程中应学会分析图像。
本题难度:一般
5、选择题 在一定温度,固定体积的密闭容器中,下列叙述不是可逆反应A(g)+3B(g)? ?2C(g)达到平衡标志的是(?)
?2C(g)达到平衡标志的是(?)
①C的生成速率与C的分解速率相等;②单位时间生成amol A,同时生成3amolB;③A、B、C的浓度不再变化;④A、B、C的压强不再变化;⑤混合气体的密度不再变化;⑥混合气体的物质的量不再变化;⑦单位时间消耗amol A,同时消耗2amol C;⑧A、B、C的分子数目比为1:3:2;⑨混合气体的平均相对分子质量不再变化?
A. ②⑤⑧? B. ⑦④? C. ①③? D. ⑤⑥⑨
参考答案:A
本题解析:在一定条件下,当可逆反应中正反应速率和逆反应速率相等时(但不为0),各种物质的浓度或含量均不再发生变化的状态,是化学平衡状态。所以①③正确。②中反应速率的方向是相同的,速率之比是相应的化学计量数之比,因此②中的关系始终是成立,不正确。该反应是体积减小的可逆反应,即压强和物质的量也是减小的,所以当压强和物质的量不再发生变化时,可以说明,④⑥正确。密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,⑤不正确。⑦中反应速率的方向相反,且能满足速率之比是相应的化学计量数之比,⑦正确。平衡时浓度不再发生变化,但物质之间的浓度不一定相等或满足某种关系,⑧不正确。混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,质量不变,但物质的量是变化的,所以⑨可以说明,答案选A。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,主要是考查学生对可逆反应平衡状态的了解掌握程度,以及灵活运用基础知识判断平衡状态的能力,有利于培养学生的逻辑推理能力和抽象思维能力,提高学生的应试能力和学习效率。该题的关键是明确可逆反应平衡状态的含义,以及判断依据,并能结合题意灵活运用即可。
本题难度:简单