��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� п�̵��������������ҺΪ���Һ������ܷ�ӦʽΪ��Zn��s��+2MnO2��s��+H2O��l��=Zn��OH��2��s��+Mn2O3��s��������˵��������ǣ�������
A����·��ÿͨ��0.2mol���ӣ�п�����������ϼ�С6.5g
B����ظ����ĵ缫��ӦʽΪZn-2e-+2?OH-=Zn��OH��2
C����ع���ʱ������������ͨ�����·����
D������п�̵���Ƕ��ε��
�ο��𰸣�A����Zn��s��+2MnO2��s��+H2O��l���TZn��OH��2��s��+Mn2O3��s����֪��65gZn��Ӧת�Ƶ���Ϊ2mol����6.5gZn��Ӧת��0.2mol���ӣ���A��ȷ��
B������ʧ���ӣ�����������Ӧ�����Ը����ĵ缫��ӦʽΪ��Zn-2e-+2OH-=Zn��OH��2����B��ȷ��
C����ع���ʱ�������ɸ�����������������������ͨ�����·��������C��ȷ��
D������п�̵����һ�ε�أ�������������ŵ磬��D����
��ѡD��
���������
�����Ѷȣ���
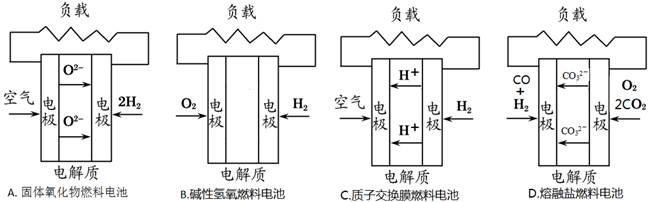
2��ѡ���� ������4��ȼ�ϵ�صĹ���ԭ��ʾ��ͼ������������Ӧ�IJ���Ϊˮ����
�ο��𰸣�C
���������ԭ����нϻ��õĽ����Ǹ�����ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ�������������Һ�е��������������ƶ��������õ����ӣ�������ԭ��Ӧ���ݴ˿����жϡ�A���ڹ���������ȼ�ϵ���У�������Ӧʽ��O2+4e-��2O2-����A���������⣻B������ȼ�ϵ���У�������ӦʽO2+2H20+4e-��4OH-����B���������⣻C�����ӽ���Ĥȼ�ϵ�أ�������Ӧʽ4H++O2+4e-��2H20����C��ȷ��D��������ȼ�ϵ���У�������Ӧʽ��2CO2+O2+4e-��2CO32-����D���������⣬��ѡC��
�����Ѷȣ�һ��
3�������� ��ͭƬ��пƬ��100mLϡ������Һ��ɵ�ԭ����У���ͭƬ�ϲ���2.24L(��̬)����ʱ������ǡ�������꣬�Լ��㣺
��пƬ����������?��?��ԭϡ������Һ�����ʵ���Ũ����?
�ο��𰸣�(4�֣�ÿ��2��)?(1)? 6.5g? (2)? 1.0 mol�ML
�����������
�����Ѷȣ�һ��
4������� ��10�֣���1����п��ͭ�õ������Ӻ����2mol/L��ϡ�����У������缫��ӦʽΪ_____________________________������ ��Ӧ����������ԭ�������Ӵ�
�����·�� ����п��ͭ������Һ��H+ �� �ƶ����������������ŵ�һ��ʱ���������pHֵ ������С�䣩��
��2����ͭƬ����Ƭ�õ������Ӻ�������Ȼ�����Һ�У�Ҳ�е���ͨ����������
�����缫��ӦʽΪ_________________��
�ܷ�Ӧ�����ӷ���ʽΪ______ ��
��3������Ƭ��ʯī�缫�õ������Ӻ�����Ȼ�����Һ��¶���ڿ����У�Ҳ�е���ͨ������������д�������缫��Ӧʽ____________�������缫��ӦʽΪ_____________��
�ο��𰸣���1��2H++2e-=H2�� ��ԭ п ͭ ���� ���
��2�� Fe��2e��= Fe2+ Fe+2Fe3+=3Fe2+
��3��������2Fe-4e��=2Fe2+ ������ O2+4e��+2H2O=4OH��
�����������1����ԭ����нϻ��õĽ�����������ʧȥ���ӱ�����������������Ӧ�����Ӿ������ߴ��ݵ������ǣ�������Һ�е��������������ƶ����������õ����ӣ�������ԭ��Ӧ��
��2����ͭƬ����Ƭ�õ������Ӻ�������Ȼ�����Һ�У���ʱ���Ǹ�����ʧȥ���ӱ��������ܽ⡣ͭ����������Һ�е������ӵõ����ӣ�����ԭ�����������ӡ�
(3) ����Ƭ��ʯī�缫�õ������Ӻ�����Ȼ�����Һ��¶���ڿ����У���ʱ����������������ʴ������������ʯī���������ܽ�����Һ�е������õ����ӡ�
�����Ѷȣ�һ��
5��ѡ���� ����������ȼ�ϵ�ص�������Ʊ�����Һ��װ����ͼ��ʾ?��a��bΪͭ�缫��������˵���в���ȷ���ǣ�������
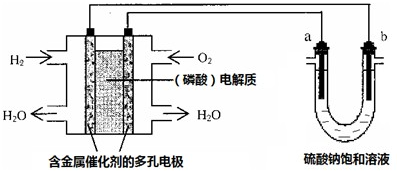
A����ع���ʱ��������ӦʽΪ��O2+4H++4e-=2H2O
B�����ʱ���������ݳ�amol���壬ͬʱ��W��Na2SO4�q10H2O�����������¶Ȳ��䣬ʣ����Һ�е������Ƶ�����������
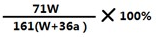
C�����ʱ����������·���ǣ����������·����������Һ������������
D������������ģ������������0.02gH2ʱ��b����Χ�����0.02gH2
�ο��𰸣�A�����װ��������ȼ�ϵ�أ�������ԭ��أ�ԭ��طŵ�ʱ���������������õ��ӷ�����ԭ��Ӧ���������õ��Ӻ������ӷ�Ӧ����ˮ���缫��ӦʽΪO2+4H++4e-=2H2O����A��ȷ��
B�����ʱ�����������������������������ݳ�amol�������ˮ������Ϊ��
2H2O?���?.?O2��+2H2����
36g? 2mol
18ag?amol
���Ե������ݳ�amol�������ˮ������Ϊ18ag���������Һ��Ϊ������Һ����Һ����������Ϊ��142142+180��100%��WW+18a��100%=71W161(W+18a)��100%����B����
C�������ڵ������ƶ�����������Һ���ƶ�����C����
D��ȼ�ϵ�غ͵�����ת�Ƶĵ���������ȵģ������������0.02gH2�����ݵ缫��Ӧ��H2��2H++2e-������ת�Ƶ���0.02mol��b���ĵ缫��ӦΪ��2H++2e-��H2��ת�Ƶ���0.02mol�������0.02gH2����D��ȷ��
��ѡBC��
���������
�����Ѷȣ���