微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 相同pH等体积的氨水和NaOH溶液,各加入5mL 0.2mol・L-1AlCl3溶液。下列判断正确的是
A.氨水中沉淀一定比NaOH溶液中的多
B.氨水中沉淀一定比NaOH溶液中的少
C.氨水中沉淀可能比NaOH溶液中的多
D.氨水中和NaOH溶液中的沉淀不可能一样多
参考答案:C
本题解析:因氨氨水为弱电解质,部分电离,氢氧化钠为强电解质,完全电离,相同体积、相同pH的氨水和NaOH溶液中的溶质一水合氨的物质的量大于氢氧化钠的物质的量,当两者都不足量时,生成的氢氧化铝沉淀的量由一水合氨和氢氧化钠来决定,一水合氨的物质的量大于氢氧化钠的物质的量,所以甲中沉淀比乙中的多;?当氨水过量,氢氧化钠不足时,甲中生成的氢氧化铝的物质的量=10mL×10-3L/mL×0.1mol?L-1=0.001mol,乙中生成的氢氧化铝的物质的量小于0.001mol,所以甲中沉淀比乙中多;当氨水过量,氢氧化钠恰好时,生成的沉淀取决于氯化铝,氯化铝的量相等,所以甲和乙中生成的沉淀一样多;当氨水和氢氧化钠都过量时,因氢氧化铝能溶于氢氧化钠但不溶于氨水,甲中生成的氢氧化铝为0.001mol,乙中生成的0.001mol氢氧化铝溶于过量的氢氧化钠,所以甲中沉淀比乙中多,故C项正确。
本题难度:一般
2、选择题 下列有关金属铝及其化合物的叙述正确的是
[? ]
A.铝在常温下不能与氧气反应
B.铝不能与氯气反应
C.铝既能溶于酸,又能溶于碱
D.氧化铝只能与酸反应,不能与碱反应
参考答案:C
本题解析:
本题难度:简单
3、选择题 下列关于铝的叙述正确的是( )
A.铝在空气中生成一层氧化物薄膜,从而光泽更好
B.铝锅煮水有大量氢气生成
C.铝片加入烧碱溶液中有氢气生成
D.浓硫酸越浓,与铝反应越剧烈
参考答案:A.铝属于亲氧元素,在空气中极易被氧化生成氧化铝,从而使铝表面失去金属光泽,故A错误;
B.铝表面有一层致密的氧化物薄膜而阻止铝被氧化,所以铝锅煮水不会有大量氢气生成,故B错误;
C.铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,也能和盐酸反应生成盐和氢气,故C正确;
D.常温下,浓硫酸与铝发生氧化还原反应生成一层致密的氧化物薄膜而阻止进一步被氧化,从而发生钝化现象,故D错误;
故选C.
本题解析:
本题难度:简单
4、填空题 物质A、B、C、D、E、F、G、H、I、J、K有下图转化关系,其中气体D、E为单质,试回答:
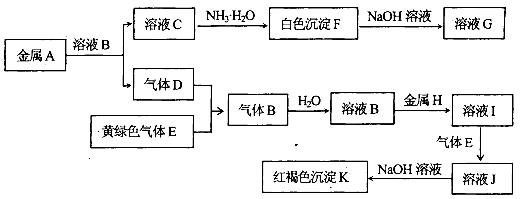
(1)写出下列物质的化学式:气体B是_____________,H是_______________,
(2)写出A与NaOH溶液反应的离子方程式:______________________________________;
(3)写出反应“I→J”的离子方程式:_____________________________________________;
(4)写出反应“F→G”的离子方程式:____________________________________________;
(5)在溶液I中滴入NaOH溶液,可观察到的现象是:_______________________________;
其反应的原理是(化学方程式)_________________________________________________.
(6)检验溶液J中的金属阳离子,用______________________试剂(填化学式),其现象是
_________________________________.
参考答案:
(1)HCl ,? Fe?
(2)2Al+2OH-+2H2O=2 AlO2-+3H2↑
(3)2Fe2++Cl2=2Fe3++2Cl-
(4)Al(OH)3+OH-=AlO2-+2H2O
(5) 先出现白色沉淀,随即变成灰绿色,最后变成红褐色。
(6) KSCN, 溶液变为血红色,
本题解析:K为红褐色沉淀,则应为Fe(OH)3,则溶液J中含有Fe3+,气体E是黄绿色气体判断为Cl2,D应为H2,E应为氧化性气体Cl2,B应为HCl,H为Fe,则I为FeCl2,J为FeCl3,白色沉淀F能溶于过量NaOH溶液,则F为Al(OH)3,G为NaAlO2,A为Al,C为AlCl3,
(1)由以上分析可知B应为HCl? H为Fe?
(2)A与NaOH溶液反应的离子方程式:2Al+2OH-+2H2O=2 AlO2-+3H2↑
(3)反应“I→J”是FeCl2和Cl2发生反应生成氯化亚铁,反应离子方程式为2Fe2++Cl2=2Fe3++2Cl-,
(4)“F→G”的离子方程式:Al(OH)3+OH-=AlO2-+2H2O
(5)在溶液I中滴入NaOH溶液,可观察到的现象是:先出现白色沉淀,随即变成灰绿色,最后变成红褐色。4Fe(OH)2+O2+2H2O=4Fe(OH)3
(6)检验溶液J中的金属阳离子即Fe3+,可取溶液加入KSCN溶液,溶液变为血红色,证明有Fe3+。
本题难度:一般
5、选择题 下列物质中既能与稀硫酸反应,又能与氢氧化钠溶液反应是
[? ]
(1)NaHCO3?(2)?(NH4)2S?(3)?Al2O3?(4)?Al?(5)?Al?(OH)3
A.(3)?(4)?
B.(3)?(4)?(5)?
C.(1)?(3)?(4)?(5)?
D.全部
参考答案:D
本题解析:
本题难度:一般