微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 某学生课外活动小组利用下图所示装置分别做如下实验
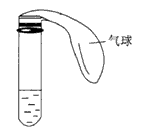
(1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是____溶液;加热时溶液由红色逐渐变浅的原因是____。
(2)在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是___溶液;加热时溶液由无色变为红色的原因是___ 。
参考答案:(1)稀氨水和酚酞 ;稀氨水中的NH3逸出,所以溶液的颜色变浅
(2)溶有SO2的品红 ;SO2气体逸出,品红溶液恢复红色
本题解析:
本题难度:一般
2、选择题
A.NO2
B.NO
C.N2O
D.N2?
参考答案:C
本题解析:由题意知,2个金属原子失去的电子,将被 1 个 HNO3分子中+5 价的 N 原子得到,由于 2 个金属原子失去的电子数一定是偶数,所以得到偶数个电子的这个+5 价的 N 原子反应后化合价一定是奇数。与备选项对照,可知 C项可选。
本题难度:一般
3、选择题 关于硝酸叙述正确的是
A.硝酸不稳定,见光或受热就会分解
B.稀硝酸是弱酸,浓硝酸是强酸
C.铜与稀硝酸反应生成二氧化氮
D.稀硝酸是弱氧化剂,浓硝酸是强氧化剂
参考答案:A
本题解析:硝酸是强酸,B不正确;铜和稀硝酸反应生成NO,C不正确;硝酸是强氧化剂,D不正确,所以答案选A。
本题难度:一般
4、填空题 (16分)现有某金属硝酸盐的化学式为M(NO3)2,为了探究其热分解产物,某化学小组开展探究性学习:
【查阅资料】金属活泼性不同,其硝酸盐分解产物不同。如,2KNO3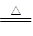 2KNO2+O2↑,
2KNO2+O2↑,
2Cu (NO3)2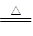 2CuO+4NO2↑+O2↑,? 4AgNO3
2CuO+4NO2↑+O2↑,? 4AgNO3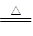 4Ag+4NO2↑+2O2↑
4Ag+4NO2↑+2O2↑
【提出猜想】猜想1? M(NO3)2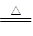 ?M(NO2)2+O2↑?
?M(NO2)2+O2↑?
猜想2? 2 M(NO3)2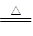 2MO+4NO2?↑+O2↑
2MO+4NO2?↑+O2↑
猜想3??。
【设计实验】为了探究上述猜想,设计如下实验装置:
【实验步骤】①连接仪器;②检查装置气密性;③取一定量样品装入大试管中,并重新连接好仪器;④加热;⑤……
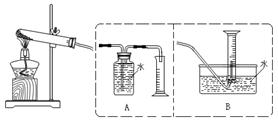
⑴写出猜想3的化学方程式:???;
⑵测定气体体积应选择?(填A或B);不选另一个装置的理由是?
?;
⑶实验收集到一定量气体是?,量筒读数前应注意?;
为了检验收集气体的成分,其操作方法是?
?;
⑷在实验后量筒里的水中加入适量碳酸氢钠粉末,溶液中产生大量气体,说明?正确(填“猜想1”、“猜想2”或“猜想3”);
⑸该小组测得两组数据:①实验前样品质量为Wg,收集到气体体积为V L;②实验前
样品质量为Wg,完全分解后测得固体产物质量为m g;
请你选择其中一组数据,计算元素M的相对原子质量为?。
参考答案:⑴M(NO3)2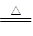 M+2NO2↑+O2↑(2分)
M+2NO2↑+O2↑(2分)
⑵B (1分)?装置A不应长导管进气,这样不能排水集气;(2分)
⑶氧气(2分)调整量筒内外液面相平(2分)用玻璃片在水槽里盖好量筒口,用食指摁紧玻璃片,将量筒从水槽里拿出来,正放在实验台上,移开玻璃片,用带火星木条接近量筒口,若木条燃烧更旺,说明收集到的气体是氧气(2分)
⑷猜想3 (2分)
⑸ (3分)
(3分)
本题解析:(1)活泼性不同的金属的硝酸盐受热分解产物不同,可能有三种固体产物:亚硝酸盐、金属氧化物、金属单质,猜想3的化学方程式为M(NO3)2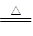 M+2NO2↑+O2↑,
M+2NO2↑+O2↑,
(2)A装置存在压强差,且导管中的气体不能被测量,存在误差,而B装置则避免了这些误差,收集气体时导水管口应伸入量筒中下部,故答案为:B;装置A不应长导管进气,这样不能排水集气;导水管口应伸入量筒中下部,以便读数前调平液面;
(3)收集到的气体是氧气,量筒读书前调整量筒内外液面相平;检验氧气用带火星的木条,操作方法为用玻璃片在水槽里盖好量筒口,用食指摁紧玻璃片,将量筒从水槽里拿出来,正放在实验台上,移开玻璃片,用带火星木条接近量筒口,若木条燃烧更旺,说明收集到的气体是氧气,
(4)在实验后的水里加入适量碳酸氢钠粉末,溶液中产生大量气体,说明溶液呈酸性,猜想2中两种气体完全反应生成硝酸,不能收集到气体,猜想3氧气过量,反应后可以收集到气体,溶液呈酸性,符合实验现象;
(5)设M的相对原子质量为A,根据反应可知固体质量减少的量为NO2和O2的质量,利用差量法计算,
M(NO3)2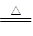 M+2NO2↑+O2↑△m
M+2NO2↑+O2↑△m
A?g?124g
m?(W-m)g

点评:本题考查实验的设计及评价,以及物质的组成及含量的测定,本题难度较大,学习中注意基础知识的积累,本题注意差量法计算的运用。
本题难度:一般
5、选择题 如图,利用培养皿探究氨气的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面。下表中对实验现象所做的解释正确的是

选项
| 实验现象
| 解释
|
A
| 浓盐酸附近产生白烟
| NH3与浓盐酸反应产生了NH4Cl固体
|
B
| 浓硫酸附近无明显现象
| NH3与浓硫酸不发生反应
|
C
| 氯化物溶液变浑浊
| 该溶液一定是AlCl3溶液
|
D
| 干燥红石蕊试纸不变色,湿润红石蕊试纸变蓝
| 氨气有碱性
参考答案:A
本题解析:考查氯气的性质
A:正确
B:碱性气体氨气可与浓硫酸生成硫酸铵
C:只要是可溶性氯化物即可
D:石蕊试纸在使用前必须湿润
答案为A
本题难度:一般
|