��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� һ���¶��£�1 molX��n mol Y�����Ϊ2L���ܱ������з������·�Ӧ��X��g��+Y��g��=2Z��g��+M��s����5min��ﵽƽ�⣬��ʱ����2a mol Z������˵����ȷ���ǣ�������
A����X��ʾ�˷�Ӧ�ķ�Ӧ�����ǣ�0.1-0.2a��mol?��L?min��-1
B�������������������ٷ����仯ʱ��˵����Ӧ�ﵽƽ��״̬
C����ƽ������ϵ�м���1mol M��ƽ�����淴Ӧ�����ƶ�
D��������ƽ����ϵ���ٳ���1mol X��v����������v���棩��С��ƽ�������ƶ�
�ο��𰸣�A��5min��ﵽƽ�⣬����2amolZ����μӷ�Ӧ��X�����ʵ���Ϊ2amol��12=amol����v��X��=amol2L5min=0.1amol/��L?min������A����
B���淴Ӧ���У���Ӧ��������������С�����������������䣬˵������ƽ�⣬��B��ȷ��
C�������ʹ�Һ��ı��������ʵ���������ı�����Ũ�ȣ���˻�ѧƽ�Ⲣ���ƶ�����C����
D��������ƽ����ϵ���ٳ���1molX����Ӧ���Ũ�������������Ũ�Ȳ��䣬����v����������v���棩���䣬ƽ��������Ӧ�ƶ�����D����
��ѡB��
���������
�����Ѷȣ���
2������� ������Ȼ���ϳɰ��Ĺ�������ʾ��ͼ��ͼ1��ʾ��
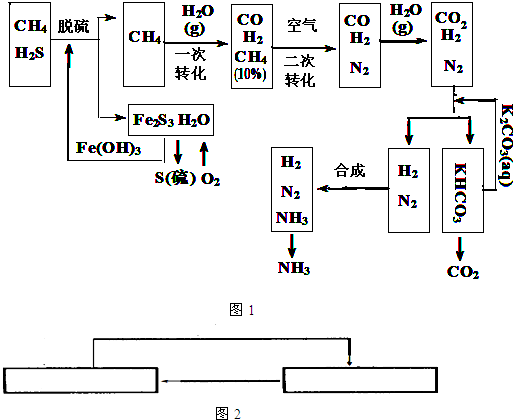
�����������̣����������գ�
��1����Ȼ������ʱ�Ļ�ѧ����ʽ��______��
��2��K2CO3��aq����CO2��Ӧ�ڼ�ѹ�½��У���ѹ������������______����ѡ�۷֣���
��a����������ԭ��?��b����ɳ����ԭ��?��c������к�ԭ��
��3����KHCO3�ֽ�õ���CO2��������______��д��CO2��һ����Ҫ��;����
��4����������������ѭ����һ��Fe��OH��3ѭ��������K2CO3��aq��ѭ��������ͼ2�б����������ͼ������ѭ����ѭ������ѭ�����ʣ���
��5����һ���¶Ⱥ�ѹǿ���ܱպϳɷ�Ӧ���У�H2��N2�������ƽ����Է�������Ϊ8.5�����÷�Ӧ�ﵽƽ��ʱ�����ƽ��������ƽ��ʽ��Ϊ10��������ʱH2��ת���ʣ�д��������̣���______��
�ο��𰸣���1���������������壬���Ժͼ��������������кͷ�Ӧ��3H2S+2Fe��OH��3��Fe2S3+6H2O��
�ʴ�Ϊ��3H2S+2Fe��OH��3�TFe2S3+6H2O��
?��2��K2CO3��aq����CO2��Ӧ����̼����أ�����ѹǿ����ѧƽ�����ҽ��У����ϻ�ѧƽ���ƶ�ԭ�����ʴ�Ϊ��b��
��3��������̼���Ժ��������Ʒ�Ӧ��̼���ƣ����������̼�ɱ���������������������ʴ�Ϊ�������������������ȣ���
��4����������ͼ������ѭ��ʹ�õ������ǵ�������������

���ʴ�Ϊ��

��
��5���������������Ϊ1mol������Ϊx��������Ϊ��1-x����
���У�28x+2��1-x��=8.5��ã�N2��x=0.25mol?H2��1mol-0.25mol=0.75mol
����ƽ��ʱN2ת��y����
?N2 +3H2?2NH3
��ʼ?0.25mol? ?0.75mol? ?0
�仯?y? ?3y? ?2y
ƽ��?��0.25-y��mol?��0.75-3y��mol?2ymol
����28��(0.25-y)mol+2��(0.75-3y)mol+17��2ymol(0.25-y)mol+(0.75-3y)mol+2ymol=10
��ã�y=0.075mol
��������ת����Ϊ��3��0.075mol0.75mol��100%=30.0%��
�𣺴�ʱH2��ת����Ϊ30%��
���������
�����Ѷȣ�һ��
3��ѡ���� ij�¶��£����ݻ��̶�������ܱ������н������¿��淴Ӧ��X(g)��Y(g)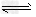 Z(g)��W(s)����H>0 һ��ʱ��ﵽ��ѧƽ��״̬������������ȷ����
Z(g)��W(s)����H>0 һ��ʱ��ﵽ��ѧƽ��״̬������������ȷ����
[? ]
A��ͨ��ϡ�����壬ƽ��������Ӧ�����ƶ�
B����������W���淴Ӧ��������
C�������¶ȣ�����Ӧ���������淴Ӧ���ʼ�С
D�������¶ȣ�ƽ�����淴Ӧ�����ƶ�
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4��ѡ���� һ�������£����Ϊ5L���ܱ������У�0��5molX��0��5molY���з�Ӧ��2X(g)��Y(g) 2Z(g)����60s�ﵽƽ�⣬����0��2molZ������˵����ȷ����
2Z(g)����60s�ﵽƽ�⣬����0��2molZ������˵����ȷ����
[? ]
A�������������Ϊ10L��Z��ƽ��Ũ�ȱ�Ϊԭ����1/2
B���ڸ��¶��£��÷�Ӧ��ƽ�ⳣ��K=0��011
C���ﵽƽ��ʱ�������������ѹǿ��ԭ����90%
D���������¶ȣ�X���������������÷�Ӧ�ġ�H��0
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5������� N2O5��һ�������������������ʺ��Ʊ��ܵ����ǵĹ�ע��
��1��N2O5�뱽����������Ӧ���ɵ��������Ľṹ��ʽ��________________
��2��2N2O5��g����4NO2��g��+O2��g��;��H��0
�ٷ�Ӧ��ƽ�������ͨ��һ������������N2O5��ת���ʽ�_______�����������С���������䡱��
���±�Ϊ��Ӧ��T1�¶��µIJ���ʵ�����ݣ�
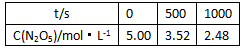
��500 s��N2O5�ķֽ�����Ϊ_________
����T3�¶��£���Ӧ1000 sʱ���NO2��Ũ��Ϊ4.98 mol��L-1����T2______T1
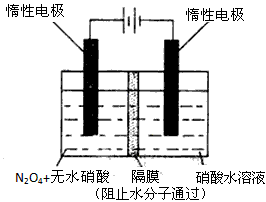
��3����ͼ��ʾװ�ÿ������Ʊ�N2O5����N2O5�ڵ��ص�_________�����ɣ���缫��ӦʽΪ
_______________
�ο��𰸣���1�����ԡ�
��2���ٲ��䣻��0.00296 mol��L-1��s-1���ۡ�������С�ڡ�
��3��������N2O4+2HNO3-2e-=2N2O5+2H+
���������
�����Ѷȣ�һ��