微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (13分)试根据下表填空:
A
| ?
| ?
|
?
| B
| ?
| ?
| C
| D
| E
| F
| ?
|
G
| H
| I
| J
| ?
| L
| K
| M
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| N
| ?
| ?
| Q
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
| | | | | | | | | | | | | | | | | |
|
(1)请写出元素Q的基态原子电子排布式?;元素N在周期表中的位置?周期?族。
(2)基态D原子核外有?个未成对电子;D2分子中分别有?个,?个π键。
(3)化合物DA5中既含离子键,又含共价键和配位键,请写出它的电子式??。
(4)表四中的元素能形成XY2型的共价分子有CE2、CL2、BK2、LE2四种,其分子的空间构型中有一种与其他三种不同,它是?(填化学式);而形成XY3型的共价分子也有四种,它们分别是DA3、DF3、DK3、LE3,其分子的空间构型中也有一种与其他三种不同,它是?(填化学式),它是由_?键(填“极性”或“非极性”,下同)构成的?分子。
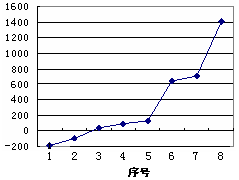
(5)第三周期8种元素按单质熔点高低的顺序如右图所示,其中序号“8”所代表的元素是?(填元素符号);其中气态氢化物稳定性最强的元素是?(填下图中的序号)。
(6)科学家证实,IK3属于共价化合物,分子式为I2K6,其结构式为下列四种中的一种,你认为正确的结构式是____________。

(7)向Q的硫酸盐溶液中加入足量的DA3的水溶液过程中,请写出发生反应的离子方程式?;最后生成配离子的结构式为?。
参考答案:(1)(2分)1s22s22p63s23p63d104s1;?第4周期? VIII族。
(2) 3;?1?, ?2。
(3)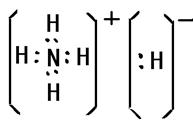
(4)? SO2;? SO3?;?极性;?非极性
(5) Si 、 2 ;(6) ③ 。(7)Cu2++2NH3?H2O= Cu(OH)2↓+2NH4+?
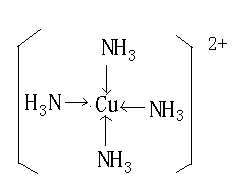
Cu(OH)2 +4NH3 =〔Cu(NH3)4〕2+? + 2OH-。
本题解析:根据所给的部分周期表可以确定元素分别是:A:? H? B: Be? C:? C? D: N? E: O? F:? F? G:? Na? H:? Mg? I: Al?J: Si? K: Cl? L: S? M:? Ar? N:Fe? Q: Cu
出元素Q即铜的基态原子电子排布式1s22s22p63s23p63d104s1;元素N即铁在周期表中的位置四周期VIII族;基态D即氮原子核外有3个未成对电子;D2分子中分别有1个,2个π键;化合物DA5即NH5是离子化合物其中既含离子键,又含共价键和配位键,它的电子式是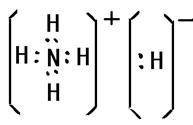
;表四中的元素能形成XY2型的共价分子有CE2即二氧化碳、CL2二硫化碳、BK2即氯化铍、LE2即二氧化硫四种,其分子的空间构型中有一种与其他三种不同,它是SO2;而形成XY3型的共价分子也有四种,它们分别是DA3即氨气、DF3即三氟化氮、DK3即三氯化氮、LE3即三氧化硫,其分子的空间构型中也有一种与其他三种不同,它是SO3,它是由极性键构成的非极性键分子;第三周期8种元素按单质熔点高低的顺序如右图所示,其中序号“8”所代表的元素是Si ,?其中气态氢化物稳定性最强即非金属性最强的元素是2;科学家证实,IK3即氯化铝属于共价化合物,分子式为Al2Cl6,会形成配位键,所以其结构式是?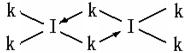
;向Q即铜的硫酸盐即硫酸铜溶液中加入足量的DA3的水溶液即氨水的过程中,请写出发生反应的离子方程式Cu2++2NH3?H2O= Cu(OH)2↓+2NH4+;Cu(OH)2 +4NH3 =〔Cu(NH3)4〕2+? + 2OH-。
最后生成配离子的结构式为 。
。
点评:对于此类题目,要求学生对元素周期表一定要熟悉,能根据元素的位置关系准确找出元素。
本题难度:一般
2、选择题 若某原子的外围电子排布式为4d15s2,则下列说法正确的是
A.该元素在元素周期表中的位置为第五周期IIIB
B.该元素位于s区
C.该元素原子为非金属
D.该元素原子N能层共有8个电子
参考答案:A
本题解析:某原子在处于能量最低状态时,外围电子排布为4d15s2,应为钇(Y)元素,位于周期表第五周期第ⅢB族,第N层的电子排布为4s24p64d1。A、外围电子排布为4d15s2,应为钇(Y)元素,位于周期表第五周期第ⅢB族,故A正确;B、区的名称来自于按照构造原理最后填入电子的轨道名称,因此根据外围电子排布为4d15s2可知,处于d区,故B错误;C、该元素属于过渡元素,为金属元素,故C错误;D、第N层的电子排布为4s24p64d1,有9个电子,故D错误,答案选A。
本题难度:一般
3、选择题 若某ⅡB族元素原子序数为x,那么原子序数为x+1的元素位于
A.ⅢA族
B.ⅢB族
C.ⅠB族
D.ⅠA族
参考答案:A
本题解析:在周期表中,第ⅡB族的右侧应该是第ⅢA族。
本题难度:简单
4、填空题 (17分)

Ⅰ.上表中的实线是元素周期表部分边界,请在表中用实线补全元素周期表边界,并画出金属和非金属的分界线,用阴影画出铁元素所在的族。
Ⅱ. A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子层多3个。E是地壳中含量最高的金属元素。根据以上信息回答下列问题:
(1)D元素在周期表中的位置是?,画出B元素简单离子结构示意图?,乙物质的电子式是?
(2)A、B、C、D、E五种元素的原子半径由小到大的顺序是(用元素符号填写)?
(3)E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是?
(4)简述比较D与E金属性强弱的实验方法:?
(5)E的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的两种化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用)其反应方程式为?
参考答案:(17分,除标注外每空2分)
Ⅰ(每项2分,共6分)
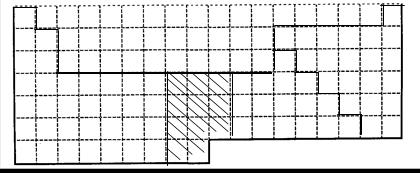
Ⅱ(1)第三周期 IIA族(1分)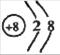 (1分)? Na2O2电子式(1分)
(1分)? Na2O2电子式(1分)
(2)O<? N < Al < Mg<? Na
(3)2 Al + 2OH― + 2H2O = 2AlO2― +? 3H2↑
(4)镁与热水可以反应生成氢氧化镁和氢气,但铝和热水不反应。(其他答案合理也可以给分)。
(5)4Al + 3C +3TiO2="=" 2Al2O3 +3TiC (条件:高温)
本题解析:略
本题难度:一般
5、填空题 已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,1mol该配合物能与3molAgNO3恰好完全沉淀 。请用对应的相关元素的化学用语规范填空:
(1)A、B、C的第一电离能由小到大的顺序为___________________________。
(2)B的氢化物(B2H4)的分子中心原子采取_______杂化。
(3)写出化合物AC2的电子式________________;一种由B、C组成的化合物与AC2互为等电子体,其化学式为____________________。
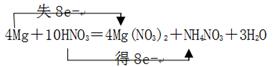
(4)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学
方程式是?(并标出双线桥表示电子转移的方向和数目)。
(5)E3+的核外电子排布式是______________?,ECl3形成的配合物的化学式为___________?。
参考答案:(10分)(1)C<O<N (1分) (2)? sp3(1分) (3)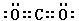 (1分)? N2O(1分)
(1分)? N2O(1分)
(4) (3分)
(3分)
(5)1s22s22p63s23p63d3(或[Ar] 3d3)? (1分)? [Cr(NH3)4(H2O)2]Cl3?(2分)
本题解析:化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构,因此C是第ⅥA族元素。又因为B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高,这说明B是氮元素,C氧元素,所以D是镁元素。AC2为非极性分子,则A是碳元素。E的原子序数为24,则E是Cr元素。
(1)非金属性越强,第一电离能越大。由于氮元素的2p轨道电子处于半充满状态,稳定性强,所以氮元素的电源电路大于氧元素的,因此A、B、C的第一电离能由小到大的顺序为C<O<N。
(2)B的氢化物(B2H4)是乙烯,乙烯分子是平面型结构,所以乙烯分子中心原子碳原子采取的是sp2杂化。
(3)CO2分子中含有2个双键,所以电子式是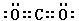 。原子数和价电子数分别都相等的分子是等电子体,则和CO2互为等电子体的是N2O。
。原子数和价电子数分别都相等的分子是等电子体,则和CO2互为等电子体的是N2O。
(4)B的最高价氧化物对应的水化物是硝酸,具有强氧化性。其稀溶液与D的单质反应时,B被还原到最低价,所以该反应的化学方程式是4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O。
(5)根据构造原理可知,E3+的核外电子排布式是1s22s22p63s23p63d3(或[Ar] 3d3)。ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,1mol该配合物能与3molAgNO3恰好完全沉淀,这说明该化合物中氯离子不是配体,因此该配位化合物的化学式应该是[Cr(NH3)4(H2O)2]Cl3。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和应试能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力。该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。
本题难度:一般