微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法不正确的是
A.硅、二氧化硅、硅酸钠是工业上制造光导纤维的主要原料
B.复合材料是将两种或两种以上性质不同的材料经特殊加工而制成的
C.浓硫酸、氯化钙、五氧化二磷、碱石灰等常用作干燥剂
D.氧化铝、碳酸氢钠既能与盐酸反应又能与氢氧化钠反应
参考答案:A
本题解析:A.用来制造光导纤维的主要原料是二氧化硅。硅主要是用来做半导体材料。故不正确;B.复合材料,是由两种或两种以上不同性质的材料,通过物理或化学的方法,在宏观上组成具有新性能的材料。正确。C.浓硫酸、氯化钙、五氧化二磷、碱石灰等能够吸水可常用作干燥剂,正确。D.氧化铝、碳酸氢钠能与盐酸反应生成对应的盐和水,又能与氢氧化钠反应生成对应的盐和水,正确。
点评:性质决定用途,根据物理或化学性质方面的差异,不同的物质可以在不同方面得以利用。
本题难度:简单
2、选择题 下列叙述中能说明A的金属性比B强的是( )
A.A原子的最外层电子数比B原子的最外层电子数少
B.A最高价氧化物的水化物的碱性比B最高价氧化物的水化物的碱性强
C.1molA从酸中置换出的H2比1molB从酸中置换的H2多
D.A的阳离子的氧化性比B阳离子的氧化性强
参考答案:A.比较金属性的强弱不能从最外层电子的多少来判断,例如Ca的最外层有2个电子,Li的最外层有1个电子,但Ca的金属性比Li强,故A错误;
B.元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,故B正确;
C.从酸中置换出氢气的多少取决于金属最外层电子数的多少,与金属的活泼性无关,如1molAl与酸反应生成的氢气比1molMg与酸反应生成的氢气多,但Mg的金属性强,故C错误;
D.金属越强的金属对应的阳离子的氧化性越弱,A的阳离子的氧化性比B阳离子的氧化性强,则B的金属性强,故D错误.
故选B.
本题解析:
本题难度:一般
3、选择题 短周期金属元素甲~戊在元素周期表中的相对位置如下表所示,下面判断正确的是
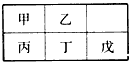
[? ]
A.氢氧化物碱性:丙<丁<戊
B.金属性:甲>丙
C.原子半径:丙>丁>戊
D.最外层电子数:甲>乙
参考答案:C
本题解析:
本题难度:简单
4、选择题 砷为第4周期第ⅤA族元素,根据它在元素周期表中的位置推测,砷不可能具有的性质是( ? )
A.砷在通常情况下是固体
B.可以存在-3、+3、+5等多种化合价
C.As2O5对应水化物的酸性比H3PO4弱
D.AsH3的稳定性比PH3强
参考答案:D
本题解析:
本题难度:一般
5、选择题 下列说法正确的是( )
A.热稳定性:H2O>NH3>HF
B.酸性:HClO>H2SO4>H3PO4
C.碱性:KOH>NaOH>Mg(OH)2
D.金属性:Al>Mg>Ba
参考答案:A.非金属性:F>O>N,元素的非金属性越强,对应的氢化物越稳定,则热稳定性:HF>H2O>NH3,故A错误;
B.非金属性:Cl>S>P,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,但HClO不是Cl的最高价含氧酸,应为HClO4>H2SO4>H3PO4,故B错误;
C.金属性:K>Na>Mg,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,则碱性:KOH>NaOH>Mg(OH)2,故C正确;
D.Mg和Ba同主族,金属性:Ba>Mg,Mg和Al同周期,金属性:Mg>Al,则有金属性:Ba>Mg>Al,故D错误.
故选C.
本题解析:
本题难度:一般