微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 漂白粉在生活、工业生产中用途广泛,漂白粉除了具有漂白作用外,还能杀菌消毒。2003年抗“非典”期间,各商场漂白粉及其他漂白产品曾一度脱销。
(1)1998年,我国长江流域和松花江流域都发生了百年不遇的特大洪水。灾区人们的饮用水,必须用漂白粉等药品消毒后才能饮用,以防传染病发生,但瓶装漂白粉久置空气中会失效。试用化学方程式表示漂白粉在空气中易失效的原因:①?;②?。
(2)已知浓盐酸和次氯酸钙能发生如下反应:
Ca(ClO)2+4HCl(浓)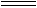 CaCl2+2Cl2↑+2H2O
CaCl2+2Cl2↑+2H2O
用贮存很久的漂白粉与浓盐酸制得的氯气中,可能含有的杂质气体是()
①CO2?②HCl?③H2O?④O2
A.①②③?B.②③④?C.②③?D.①④
(3)用Cl2和石灰乳制作漂白粉的目的是()
A.转变为较HClO稳定且易储运的物质
B.转变为更易溶于水的物质
C.提高氯气的利用率
D.增强漂白能力
参考答案:(1)①Ca(ClO)2+CO2+H2O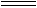 CaCO3↓+2HClO?②2HClO
CaCO3↓+2HClO?②2HClO 2HCl+O2↑
2HCl+O2↑
(2)A? (3)AB
本题解析:(1)漂白粉的成分是Ca(ClO)2和CaCl2,而能起漂白作用的是Ca(ClO)2,所以漂白粉的有效成分是Ca(ClO)2,它在空气中失效的化学方程式为:
①Ca(ClO)2+CO2+H2O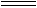 CaCO3↓+2HClO
CaCO3↓+2HClO
②2HClO 2HCl+O2↑
2HCl+O2↑
所以,漂白粉应密闭保存,避免与空气接触。
(2)漂白粉久置后可能会失去漂白作用,因为发生以下反应:
Ca(ClO)2+CO2+H2O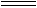 CaCO3↓+2HClO;2HClO
CaCO3↓+2HClO;2HClO 2HCl+O2↑
2HCl+O2↑
因此当贮存很久的漂白粉与浓盐酸反应时会有CO2气体产生,而反应过程中产生的水及浓盐酸中氯化氢的外逸,也是不可避免的。因此本题选A。
(3)HClO容易分解,Ca(ClO)2等盐较稳定且为固体,便于储运;Ca(ClO)2溶解度要比Cl2大得多。所以选A、B。
本题难度:简单
2、实验题 如图是某研究性学习小组设计制取氯气并以氯气为反应物进行特定反应的装置。

(1)要将C装置接入B和D之间,正确的接法是:a→?→?→d。
(2)实验开始先点燃A处的酒精灯,打开阀K,让Cl2充满整个装置,再点燃D处的酒精灯。Cl2通过C装置后进入D,D装置内盛有碳粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为?。
(3)D处反应完毕后,关闭阀K,移去两个酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是?,B的作用是?。
(4)在A、B、C、D、E装置中有一处需要改进,说明需要改进的理由并画出改进后的装置图。
参考答案:(1)c b
(2)2Cl2+C+2H2O 4HCl+CO2
4HCl+CO2
(3)瓶中液面下降,长颈漏斗内液面上升 贮存少量Cl2,避免Cl2对环境造成污染
(4)D中反应生成的HCl气体极易溶于水,易发生倒吸

本题解析:正确连接的关键是C装置的作用,由于D中反应生成了CO2和HCl,有氢元素存在,说明有水参加反应,反应方程式为2Cl2+C+2H2O 4HCl+CO2,C装置的作用是提供水蒸气,而且Cl2从C中出来带出水蒸气,因此应该是长进短出。阀K关闭,此时B相当于量气装置,生成的气体将B中水压入漏斗中。由于D中反应生成了极易溶于水的HCl,E装置不正确,会造成E中水倒吸,可以用一个倒置的小漏斗防止倒吸。
4HCl+CO2,C装置的作用是提供水蒸气,而且Cl2从C中出来带出水蒸气,因此应该是长进短出。阀K关闭,此时B相当于量气装置,生成的气体将B中水压入漏斗中。由于D中反应生成了极易溶于水的HCl,E装置不正确,会造成E中水倒吸,可以用一个倒置的小漏斗防止倒吸。
本题难度:一般
3、选择题 下列实验现象的描述错误的是
A.氢气在氯气中燃烧产生苍白色火焰
B.红热的铁丝在氯气中燃烧,火星四射,生成黑色固体颗粒
C.红热的铜丝在氯气中燃烧,产生棕黄色烟
D.钠在空气中燃烧,发出黄色的火焰,生成淡黄色固体
参考答案:B
本题解析:铁在氯气中燃烧,反应非常剧烈,但是生成的不是黑色固体,是产生大量棕褐色的烟,所以B项错误,其余均正确。
本题难度:一般
4、选择题 将新制氯水分别滴加到AgNO3溶液、加有酚酞的NaOH溶液、石蕊溶液、品红溶液和Na2CO3溶液中至过量,依次观察到的现象描述合理的一组是( )
A.产生沉淀、无明显变化、变红、溶液褪色、有气泡
B.无明显变化、溶液褪色、变红、无明显变化、产生沉淀
C.产生沉淀、溶液褪色、先变红后褪色、溶液褪色、有气泡
D.产生沉淀、无明显变化、先变红后褪色、无明显变化、产生沉淀
参考答案:新制氯水滴加到AgNO3溶液溶液中新制氯水,发生反应,Ag++Cl-=AgCl↓出现白色沉淀;
加有酚酞的NaOH溶液呈红色,新制氯水滴加到溶液中至过量,发生反应H++OH-=H2O,氢氧根离子浓度减少,则溶液变为无色;
新制氯水滴加到石蕊溶液中至过量,盐酸使石蕊变红,且HClO具有漂白性,次氯酸的存在使红色褪去;
新制氯水滴加到品红溶液中至过量,由于次氯酸具有漂白性,品红褪色;
新制氯水滴加到Na2CO3溶液中至过量,发生反应CO32-+2H+=CO2↑+H2O,有气体生成;
综合上述分析,依次观察到的现象描述为产生沉淀、溶液褪色、先变红后褪色、溶液褪色、有气泡;
故选C.
本题解析:
本题难度:简单
5、实验题 下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。
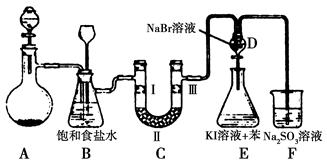
(1)制备氯气选用的药品为漂粉精固体和浓盐酸,相关的化学反应方程式为________。
(2)装置B中饱和食盐水的作用是________;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:__________________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入物质的组合是________(填编号)。
编号
| a
| b
| c
| d
|
Ⅰ
| 干燥的有色布条
| 干燥的有色布条
| 湿润的有色布条
| 湿润的有色布条
|
Ⅱ
| 碱石灰
| 硅胶
| 浓硫酸
| 无水氯化钙
|
?Ⅲ
| 湿润的有色布条
| 湿润的有色布条
| 干燥的有色布条
| 干燥的有色布条
|
?
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是________该现象________(填“能”或“不能”)说明溴的非金属性强于碘,原因是__________________________。
(5)有人提出,装置F中可改用足量的NaHSO3溶液吸收余氯,试写出相应的离子反应方程式:__________________。请判断改用NaHSO3溶液是否可行?________(填“是”或“否”)。
参考答案:(1)Ca(ClO2)+4HCl(浓)=CaCl2+2Cl2↑+2H2O
(2)除去Cl2中的HCl B中长颈漏斗中液面上升,形成水柱
(3)d
(4)E中溶液分为两层,上层(苯层)为紫红色 不能 过量的Cl2也可将I-氧化为I2
(5)HSO3―+Cl2+H2O=SO42―+2Cl-+3H+(或4HSO3―+Cl2=SO42―+2Cl-+3SO2+2H2O) 否
本题解析:(1)漂粉精中的次氯酸钙与浓盐酸反应生成氯气。(2)由于浓盐酸具有挥发性,从A装置出来的氯气中含有氯化氢气体,故用B中的饱和食盐水除去其中的氯化氢。(3)若验证氯气是否有漂白性,则应该先验证氯气是否能够使湿润的有色布条褪色。(4)读图可知,D中通入氯气后生成单质溴,加入E中后又生成了单质碘,故E中现象是溶液分层,且上层即苯层显紫红色,但是由于D中可能有过量的氯气,故E中生成的单质碘不一定是溴与KI反应置换出来的,故不能说明溴的非金属性一定比碘强。(5)由于氯气具有氧化性,与NaHSO3发生氧化还原反应HSO3―+Cl2+H2O=SO42―+2Cl-+3H+,由于NaHSO3溶液显酸性,会抑制氯气的吸收,故不能选用NaHSO3溶液吸收氯气。
点拨:本题考查氯气的制备及相关性质,考查考生综合分析问题和解决问题的能力。难度较大。
本题难度:一般