微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关金属腐蚀与防护的说法正确的是
A.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
C.纯银器表面在空气中因电化学腐蚀渐渐变暗
D.金属腐蚀的电化学腐蚀,是利用了原电池原理,但原电池原理不能用于金属防护
参考答案:A
本题解析:因为锌比铁活泼,形成原电池时锌为负极,铁为正极而被保护,称作牺牲阳极的阴极保护法,A项正确;镀锡铁制破损时,因铁比锡活泼,形成原电池时铁作负极,反而加快了铁的腐蚀,B项不正确;纯银能与硫等化合形成硫化物,发生化学腐蚀而变暗,C项不正确;牺牲阳极的阴极保护法也是利用了原电池原理,D项不正确。故答案为A项。
本题难度:简单
2、选择题 如右图两个电解槽中,A、B、C、D均为石墨电极。若电解过程中共有0.02mol电子通过,正确的是(?)
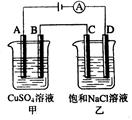
A.甲烧杯中A极上最多可析出铜0.64g
B.甲烧杯中B极上电极反应式4OH--4e-=2H2O+O2↑
C.乙烧杯中滴入酚酞试液,D极附近先变红
D.烧杯中C极上电极反应式为4H++4e-=2H2↑
参考答案:C
本题解析:A为电解池的阳极,发生氧化反应:4OH--4e=2H2O ,故A错
D极为电解池的阴极发生还原反应:2H2O+4e+O2="4OH-" ,所以滴入酚酞D极附近先变红,C对
故B极发生还原反应Cu2++2e=Cu? C极发生氧化反应2Cl--2e=Cl2故B、D错
点评:该题考查串联电解池,比简单的电解池较为复杂,在解题过程中注意分析电子的流动方向,确定电极反应式。
本题难度:一般
3、选择题 下列金属防腐措施中,利用原电池原理的是( )
A.在金属表面喷漆
B.在金属中加入一些铬或镍制成合金
C.在轮船的壳体水线以下部分装上锌块
D.使金属表面生成致密稳定的氧化物保护膜
参考答案:A、在金属表面喷漆,只是阻止了金属和电解质溶液接触,不能构成原电池,所以不是利用原电池原理,故A错误.
B、在金属中加入一些铬或镍制成合金,改变了金属的结构,不是原电池原理,故B错误.
C、在轮船的壳体水线以下部分装上锌块,锌、铁和海水能构成原电池,较活泼的金属锌作负极,锌在反应中失去电子被氧化,从而铁被保护,所以是利用原电池原理,故C正确.
D、使金属表面生成致密稳定的氧化物保护膜,阻止了金属和其它物质的反应,但没有构成原电池,所以不是利用原电池原理,故D错误.
故选C.
本题解析:
本题难度:简单
4、选择题 已知某镍镉(Ni-Cd) 可充电电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O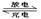 Cd(OH)2 + 2Ni(OH)2有关该电池的说法正确的是
Cd(OH)2 + 2Ni(OH)2有关该电池的说法正确的是
A.放电时Cd电极发生氧化反应
B.放电时电解质溶液中的OH-向负极移动
C.放电时负极附近溶液的碱性不变
D.充电时阳极反应:Ni(OH)2+OH―+e―=NiOOH+H2O
参考答案:AB
本题解析:从化合价分析,放电时Cd从0价升高为+2价,被氧化,发生氧化反应,A正确;放电时Cd失去电子形成Cd2+,做电源负极,因此吸引溶液中阴离子OH-往负极移动,碱性增强,形成Cd(OH)2 ,B正确,C错误;充电时,阳极发生氧化反应失去电子,所以D项错误。故选AB。
本题难度:一般
5、选择题 下列装置中(杯中均盛有海水)能使铁受到保护不被腐蚀的是( )
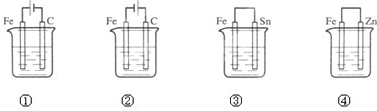
A.①③
B.②④
C.①②
D.③④
参考答案:①该装置是电解池,铁作电解池的阳极,所以加速铁的腐蚀,故不选;
②该装置是电解池,铁作电解池的阴极而被保护,属于外加电流的阴极保护法,故选;
③该装置是原电池,铁作负极,加速铁的腐蚀,故不选;
④该装置是原电池,铁作正极而被保护,属于牺牲阳极的阴极保护法,故选;
故选B.
本题解析:
本题难度:简单