微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 1991年我国首创以铝-空气-海水为能源的新型“海水电池”,该电池以海水为电解质溶液,靠空气中的氧使铝不断氧化而产生电流。它比干电池能量高20~50倍。其总反应式表示为:4Al+3O2+6H2O===4Al(OH)3。
(1)该电源的负极材料为?,(2)写出正极反应式为 :?。
参考答案:(1)铝 ?(2) O2+2H2O+4e-===4OH-
本题解析:(1)原电池中,负极发生氧化反应;根据题意知,该电池以海水为电解质溶液,靠空气中的氧使铝不断氧化而产生电流,则负极材料为铝;(2)原电池工作时,正极上氧气得电子发生还原反应,电极反应式为O2+2H2O+4e-=4OH-。
本题难度:简单
2、选择题 质子交换膜燃料电池(proton exchange membrane fuel cell,英文简称PEMFC)是燃料电池的一种。如图是质子交换膜氢氧燃料电池,下列有关该电池的原理的描述正确的是
A.溶液中H+透过质子交换膜从右向左迁移
B.b极发生氧化反应
C.电子从a极流出经溶液流到b极
D.该电池在使用过程中,H+的物质的量保持不变
参考答案:D
本题解析:A、从图示当中可以看到,a极通入的是氢气,电极反应是H2―2e = 2H+, 溶液中H+透过质子交换膜从左向右迁移,错误;B、b极通入的是氧气,发生还原反应,错误;C、a极是原电池的负极,电子从a极流出经外电路流到b极,错误;D、在此燃料电池中发生的总反应为2H2+O2=2H2O,所以H+的物质的量保持不变,正确。
本题难度:一般
3、选择题 下图各容器中盛有稀硫酸,能形成原电池且铁为正极的是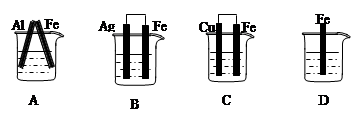
参考答案:A
本题解析:原电池的形成条件:1、有两种活泼性不同的金属(或其中一种为非金属导体)作电极;2、电极均插入电解质溶液中;3、两极相互连接(或接触);4、能自发的发生氧化还原反应。据此可知选项ABC均能形成原电池。其中金属性是Al>Fe>Cu>Ag,所以在ABC中铁分别是正极、负极、负极,答案选A。
点评:该题是高考中的常见题型,属于基础性试题的考查,难度不大。掌握原电池的工作原理、原电池的构成条件是答题的关键。
本题难度:简单
4、选择题 铜―锌―稀硫酸组成的原电池,放电一段时间后,溶液的pH将(? )
A.不变
B.升高
C.降低
D.无法确定
参考答案 :B
本题解析:此原电池放电时,反应消耗硫酸,使溶液的酸性降低。
本题难度:一般
5、填空题 (14分)美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如下图:
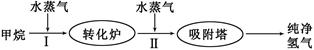
(1)此流程的第II步反应为:CO(g)+H2O(g) H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表:
H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表:
从上表可以推断:此反应是?(填“吸”或“放”)热反应。在830℃下,若开始时向恒容密闭容器中充入1mo1CO和2mo1H2O,则达到平衡后CO的转化率为?。
(2)在500℃,以下表的物质的量(按照CO、H2O、H2、CO2的顺序)投入恒容密闭容器中进行上述第II步反应,达到平衡后下列关系正确的是
实验编号
| 反应物投入量
| 平衡时H2浓度
| 吸收或放出的热量
| 反应物转化率
|
A
| 1、1、0、0
| c1
| Q1
| α1[来源:]
|
B
| 0、0、2、2
| c2
| Q2
| α2
?
|
C
| 2、2、0、0
| c3
| Q3
| α3
|
A.2c1= c2 =c3? B.2Q1=Q2=Q3? C.α1 =α2 =α3? D.α1 +α2 ="1"
(3)在一个绝热等容容器中,不能判断此流程的第II步反应达到平衡的是?。
①体系的压强不再发生变化?②混合气体的密度不变
③混合气体的平均相对分子质量不变?④各组分的物质的量浓度不再改变
⑤体系的温度不再发生变化?⑥v(CO2)正=v(H2O)逆
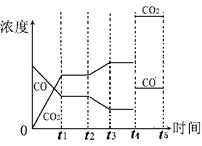
(4)下图表示此流程的第II步反应,在t1时刻达到平衡、在t2时刻因改变某个条件浓度发生变化的情况:图中t2时刻发生改变的条件是?、?
(写出两种)。若t4时刻通过改变容积的方法将压强增大为原先的两倍,在图中t4和t5区间内画出CO、CO2浓度变化曲线,并标明物质(假设各物质状态均保持不变)。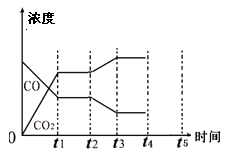
参考答案:(1)放;66.7%(2)AD (3)②③(4)降低温度,或增加水蒸汽的量,或减少氢气的量;(每格2分)

本题解析:(1)温度越高,平衡常数越小,所以正反应是放热反应。
CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g)
起始量(mol)? 1? 2? 0? 0
转化量(mol)? x? x? x? x
平衡量(mol)? 1-x? 2-x? x? x
根据平衡常数知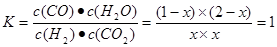
解得x=2/3,所以平衡后CO的转化率为是66.7%。
(2)因为反应前后体积,即改变压强平衡不会发生移动,根据所给的反应物投入量来看ABC就是等效的,虽然氢气的含量,但氢气的浓度不同,其中BC相等且都是A的2倍。根据500℃平衡常数可计算出A中反应物的转化率均是75%【计算方法同(1)】,即平衡时A中CO、H2O、H2、CO2分别是0.25mol、0.25mlol、0.75mol、0.75mol,则平衡时B、C中CO、H2O、H2、CO2分别都为0.5mol、0.5mol、1.5mol、1.5mol。即B、C中转化率分别是25%和75%。A中放热Q1,所以反应热是-2Q1kJ・mol-1。则C中放热2Q1,B中吸热Q1。答案AD正确。
(3)因为体系绝热,而反应是放热反应,所以压强会发生变化,①⑤可以。反应前后气体质量和容器的体积均不发生变化,所以密度不变,②不可以。反应前后气体质量和物质的量均不发生变化,所以相对分子质量不变,③不可以。④⑥符合化学平衡的概念正确。答案是②③。
(4)由图像可知t2时刻CO浓度减小,CO2浓度增大,因此改变的条件是降低温度,或增加水蒸汽的量。t4时刻通过改变容积的方法将压强增大为原先的两倍,平衡不移动,但物质的浓度均增大,都变为原来大2倍,如图所示:
本题难度:一般