微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 以下实验能获得成功的是(?)
A.要检验某溴乙烷中的溴元素,可以加入NaOH溶液共热,冷却后滴入AgNO3溶液,观察有无浅黄色沉淀生成
B.用氨水清洗试管壁附着的银镜
C.苯和硝基苯采用分液的方法分离
D.将铜丝在酒精灯上加热变黑后,立即伸入无水乙醇中,铜丝恢复成原来的红色
参考答案:D
本题解析:A项中加入AgNO3溶液前必须加入稀硝酸酸化才能观察到有无浅黄色沉淀生成,B项氨水不与Ag反应,C项苯和硝基苯互溶不能用分液的方法分离。答案选D。
点评:本题非常基础简单重点考查学生的有机实验基本操作知识。
本题难度:一般
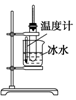
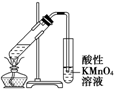
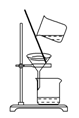
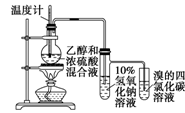
2、选择题 用下列实验装置进行相应的实验,能够达到实验目的的是(? )
| 
| 
| 
|
A.实验室制取少量的硝基苯
| B.证明溴乙烷、NaOH、乙醇溶液共热生成乙烯
| C.分离乙酸乙酯、碳酸钠和水的混合物
| D.证明乙醇、浓硫酸共热生成乙烯
|
?
参考答案:D
本题解析:A项,反应条件应为水浴加热;B项,乙醇也能使酸性KMnO4溶液褪色,干扰乙烯的检验;C项,分离乙酸乙酯和Na2CO3溶液的混合物应使用分液操作。
本题难度:一般
3、选择题 将等体积的苯、汽油和水在试管中充分混合后静置。下列图示现象正确的是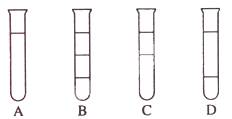
参考答案:D
本题解析:苯和汽油互溶,不溶于水,且密度小于水的,所以正确的答案选D。
点评:该题是高考中的常见题型,属于基础性试题的考查。该题的关键是熟练记住常见有机物的溶解性和密度,然后灵活运用即可,难度不大。
本题难度:简单
4、实验题 某校化学课外兴趣小组的学生为了验证乙醇的分子结构,设计如下实验程序:乙醇组成元素的测定、分子式的测定、分子结构的测定。
(1)他们决定用燃烧乙醇分析产物来确定乙醇中含有C、H两种元素。简要说明他们的具体操作:①证明含有氢元素的操作是________________________________________________________?_
________________________________________________________________________________________;
②证明含有碳元素的操作是________________________________________________
_______________________________________________________________________
(2)要用燃烧分析产物证实乙醇中还含有氧元素时,需取得一些实验数据,这些数据应该是________________________。
(3)为确定乙醇的分子式,除(2)中数据外,还需不需要测定乙醇的相对分子质量?
_______________________________________________________________________
(4)为测定乙醇分子结构,他们用了无水乙醇和金属钠反应收集生成氢气的方法,选用了如下图所示的仪器(有的仪器配用双孔橡皮塞)。
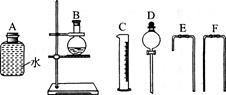
①装置的连接顺序是______接______接______接______接_______接_______。
②已知无水酒精的密度为0.789 g・cm一3,移取2.0mL酒精,反应完全后(钠过量),收集390 mL气体。则乙醇分子中能被钠取代出的氢原子数为_______,由此可确定乙醇的结构为______________________而不是______________。
(5)实验所测定的结果偏高,可能引起的原因是(填写编号)。______________
A.本实验在室温下进行
B.无水酒精中混有微量甲醇
C.无水酒精与钠反应不够完全
参考答案:(1)①用一干燥的小烧杯倒置在乙醇燃烧的火焰的上方,烧杯内壁有水珠生成?
②将内壁用澄清石灰水润湿的小烧杯倒置在火焰的上方,石灰水变浑浊
(2)乙醇、二氧化碳及水三种物质的质量?(3)不需要
(4)① D B E A F C?② 1;CH3CH2OH;CH3―O―CH3
(5)AB
本题解析:(1)①有机物中的H元素燃烧时生成H2O,所以用一干燥的小烧杯倒置在乙醇燃烧的火焰的上方,烧杯内壁有水珠生成可证明物质含氢元素。
②有机物中的C元素燃烧时生成CO2,所以将内壁用澄清石灰水润湿的小烧杯倒置在火焰的上方,石灰水变浑浊,可证明物质含碳元素。
(2)根据二氧化碳和水的质量。可求出C、H元素的质量,与乙醇的质量对比,即可判断出乙醇还含有碳元素。
(3)根据乙醇、二氧化碳及水三种物质的质量可求出C、H、O原子的个数比为:2:6:1,根据C、H、O的成键情况可知,乙醇的分子式只能为C2H6O,所以不需要测定乙醇的相对分子质量,即可确定乙醇的分子式。
(4)①分液漏斗与烧瓶相连为反应装置,气体通过E短导管进入A,A中的水沿F进入量筒,所以仪器的连接想、顺序为: D B E A F C
②乙醇的物质的量为:2.0mL×0.789g?cm-3÷46g/mol=0.034mol;生成的氢气为:0.39L÷22.4L/mol=0.017mol,所以 乙醇分子中能被钠取代出的氢原子数为1;可确定乙醇的结构为CH3CH2OH,而不是CH3―O―CH3
(5)A、本实验在室温下进行,气体摩尔体积大于22.4L/mol,造成结果偏高,正确;B、因为相同质量的甲醇反应生成的氢气更多,无水酒精中混有微量甲醇会造成结果偏高,正确;C、无水酒精与钠反应不够完全,生成的氢气偏少,则结果偏低,错误。
本题难度:一般
5、选择题 形成化合物种数最多的元素在周期表中处于
A.第四周期ⅧA族
B.第二周期ⅣA族
C.第三周期ⅣA族
D.第三周期ⅦA族
参考答案:B
本题解析:略
本题难度:简单