��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��373K ʱ����0.5 mol N2O4����ͨ�����Ϊ5 L������ܱ������У��������ֺ���ɫ����Ӧ���е�2 sʱ��NO2��Ũ��Ϊ0.02 mol/L����60 sʱ����ϵ�Ѵﵽƽ�⣬��ʱ������ѹǿΪ��Ӧǰ��1.6��������˵����ȷ���ǣ�?��
A����2 sʱ����ϵ��ѹǿΪ��Ӧǰ��1.1����
B��ǰ2 s����N2O4Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ0.01 mol��L-1��s-1
C��ƽ��ʱ����ϵ�ں�N2O4 0.25 mol
D��ƽ��ʱ�����������ڳ��뵪����������N2O4��ת����
�ο��𰸣�A
�����������Ӧ���е�2 sʱ��NO2��Ũ��Ϊ0.02 mol/L��������NO2��0.1mol���������N2O4��0.05mol��������2 sʱ����ϵ��ѹǿΪ��Ӧǰ��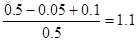 ��A��ȷ��ǰ2 s����N2O4Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ
��A��ȷ��ǰ2 s����N2O4Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ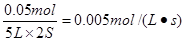 ��B����ȷ��ƽ��ʱ������ѹǿΪ��Ӧǰ��1.6������ƽ��ʱ��������ʵ�����0.5mol��1.6��0.8mol�����ݷ�ӦʽN2O4
��B����ȷ��ƽ��ʱ������ѹǿΪ��Ӧǰ��1.6������ƽ��ʱ��������ʵ�����0.5mol��1.6��0.8mol�����ݷ�ӦʽN2O4 2NO2��֪������N2O4��0.3mol��ʣ����0.2mol��C����ȷ�����뵪����ѹǿ����Ũ�Ȳ��䣬����ƽ�ⲻ�ƶ���D����ȷ����ѡA��
2NO2��֪������N2O4��0.3mol��ʣ����0.2mol��C����ȷ�����뵪����ѹǿ����Ũ�Ȳ��䣬����ƽ�ⲻ�ƶ���D����ȷ����ѡA��
�����Ѷȣ�һ��
2��ѡ���� ������ʵ��������������ԭ�����͵���
A�����Ƶ���ˮ�ڹ�����������ɫ��dz
B��ʹ�ô�������ߺϳɰ��IJ���
C��������أ�KMnO4����Һ��ˮϡ�ͺ���ɫ��dz
D��H2��I2��HIƽ���������ѹ����ɫ����
�ο��𰸣�A
�����������
�����Ѷȣ���
3��ѡ���� ���ڿ��淴Ӧ��2A(g)��B(g) 2C(g)?��H��0�����и�ͼ��ȷ����
2C(g)?��H��0�����и�ͼ��ȷ����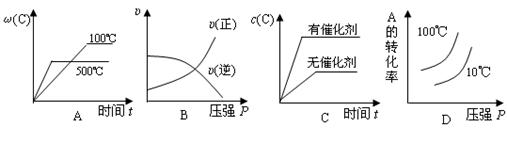
�ο��𰸣�A
�������������Ӧ�Ƿ��ȷ�Ӧ���¶�Խ�ߣ�C����������ԽС��A��ȷ������ѹǿ�������淴Ӧ���ʶ��ӿ죬B��������ƽ���ƶ���Ӱ�죬���ԼӴ����벻�Ӵ���c(C)��ͬ��C��������ѹǿ��ƽ��������Ӧ�����ƶ���A��ת�������������¶ȣ�ƽ�����淴Ӧ�����ƶ���A��ת���ʼ�С��D����
���������������ɳ����ԭ����
�����Ѷȣ�һ��
4��ѡ���� ���и������ʵ���ɫ�仯��������������ԭ�����͵���?
A�����Ƶ���ˮ�ڹ�����������ɫ��dz
B��H2��I2��HIƽ��������ѹ����ɫ����
C��KI��Һ����ˮ����ɫ����
D��������������ڰ������ķ�Ӧ
�ο��𰸣�A
�����������
�����Ѷȣ���
5��ѡ���� ��һ�ܱ������г���1mol N2��3mol H2����һ�������·�����ӦN2��3H2 2NH3,�����й�˵����ȷ���ǣ�?��
2NH3,�����й�˵����ȷ���ǣ�?��
A���ﵽ��ѧƽ��ʱ������Ӧ���淴Ӧ�����ʶ�Ϊ��
B��������3u��(N2)��u��(H2)ʱ����Ӧ�ﵽƽ��״̬
C���ﵽ��ѧƽ��ʱ����λʱ������amolN2��ͬʱ����3amolH2
D����N2��H2��NH3�ķ�������Ϊ1��3��2����Ӧ�ﵽƽ��״̬
�ο��𰸣�C
�����������һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0������Ӧ��ϵ�и������ʵ�Ũ�Ȼ������ٷ����仯��״̬����Ϊ��ѧƽ��״̬������ѡ��A����ȷ��B�з�Ӧ���ʵķ�������ͬ�ģ�����֮������Ӧ�Ļ�ѧ������֮�ȣ����B�еĹ�ϵʼ���dz�����B����ȷ��ƽ��ʱ�������ʵ�Ũ�Ȳ��ٷ����仯�������ֵ�Ũ��֮�䲻һ������ij�ֹ�ϵ��D����ȷ��C�з�Ӧ���ʵķ����෴������������֮������Ӧ�Ļ�ѧ������֮�ȣ���ȷ����˴�ѡC��
�������������е��Ѷȵ����⣬Ҳ�Ǹ߿��еij������ͺͿ��㡣���������ǿ���������У����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ��������������ѧ���������������ͷ�ɢ˼ά����������Ĺؼ�����ȷƽ��״̬���ص㣬Ȼ���Ͼ���Ŀ��淴Ӧ����ʽ������ü��ɡ�
�����Ѷȣ�һ��