��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� A��MΪ����Ԫ�أ���֪Aλ�ڶ����ڣ���A2+��M+�ĵ�����֮��Ϊ8��������˵����ȷ����
[? ]
A��A��Mԭ�ӵĵ�������֮�Ϳ�����11
B��A��M��ԭ������֮��Ϊ8
C��A��Mԭ�ӵ�����������֮��Ϊ8
D��A��Mԭ�ӵ�����������֮��Ϊ7
�ο��𰸣�A
���������
�����Ѷȣ�һ��
2��ѡ���� ��C��N��O��F��˳�����еݱ������ȷ���ǣ�������
A��ԭ�Ӱ뾶������
B��Ԫ��ԭ�ӵõ�����������
C����̬�⻯���ȶ�������ǿ
D������ϼ�������
�ο��𰸣�C��N��O��F�����ڱ���ͬ���ڣ�������ԭ��������������
A��ͬ����Ԫ�ش�����ԭ�Ӱ뾶��С����A����
B��ͬ����Ԫ�ش�����Ԫ�صķǽ���������ǿ���õ�����������ǿ����B����
C��ͬ����Ԫ�ش�����Ԫ�صķǽ���������ǿ����Ӧ����̬�⻯���ȶ�������ǿ����C��ȷ��
D��F������ϼ�Ϊ0�ۣ������ۣ���D����
��ѡC��
���������
�����Ѷȣ�һ��
3������� 2001��������ѧ���������Ƿ����˺˵����Ϊ116��Ԫ�أ����ƶϸ�Ԫ����Ԫ�����ڱ��е�λ��____������֪��Ԫ��ԭ�Ӻ�����155�����ӣ�����������Ϊ____��
�ο��𰸣��������ڵڢ�A��? ��271
���������
�����Ѷȣ�һ��
4�������
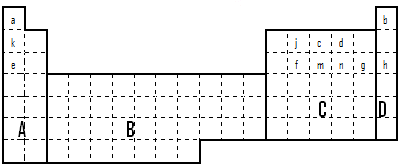
��1��������Ԫ�����ڱ���ȫ���ǽ���Ԫ�ص�����Ϊ______��
��a��A?��b��B?��c��C?��d��D
��2�����мס������ֶ�����Ԫ�أ������£���Ԫ�ص��������Ũ�����Ũ�����У����涼�������ܵ�����Ĥ����Ԫ��ԭ�Ӻ���M���Ӳ���K���Ӳ��ϵĵ�������ȣ�
��Ԫ�ط��Ž��ס�����Ԫ����д������Ԫ�����ڱ��ж�Ӧ��λ�ã�
��3����������Сд��ĸ�ֱ����һ�ֻ�ѧԪ�أ���f��m��n��g���γɵ��⻯����ȶ��Ի�ԭ����ǿ������˳��Ϊ______���ѧʽ����
�ڼס��ҡ�c��d��e�γɵļ����ӵİ뾶��С�����˳��Ϊ______����������ʵ�����ӷ��ű�ʾ��
��f������������Ʊ���Ӧ��ˮ����Ļ�ѧ����ʽ______
��cԪ�صĵ�����;______����һ������
�ο��𰸣���1�������ڱ��У����еĹ���Ԫ�ؾ��ǽ���Ԫ�أ�����Ԫ��λ�ڸ�ͼ�е�B���ʴ�Ϊ��b��
��2�������£����ڶ����ڵļ�Ԫ�ص��������Ũ�����Ũ�����У����涼�������ܵ�����Ĥ��ֻ�н���������Ҫ�����Լ���Al���ڵ������ڵڢ�A�壬ԭ�Ӻ���M���Ӳ���K���Ӳ��ϵĵ�������ȵ�Ԫ����Mg���ڵ������ڣ��ڢ�A�壬�ʴ�Ϊ��
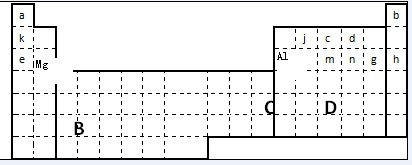
��3���پ�Ԫ�����ڱ��Ľṹ��Ԫ�صķֲ�����֪f��m��n��g�ֱ��ǣ�Si��P��S��Cl��ͬ����Ԫ�ش����ң��⻯����ȶ�������ǿ����HCl��H2S��PH3��SiH4��
�ڸ���Ԫ�����ڱ��Ľṹ��Ԫ�صķֲ�����֪�ס��ҡ�c��d��e�γɵļ����ӷֱ�Ϊ��Al3+��Mg2+��N3-��O2-��Na+�����Ǻ����������ͬ�������������Խ��뾶ԽС�������ӵİ뾶��С�����˳��Ϊ��Al3+��Mg2+��Na+��O2-��N3-��
�ʴ�Ϊ��Al3+��Mg2+��Na+��O2-��N3-��
����������費����ˮ��Ӧ����˶�����������Ӧ���ɹ����ƣ�Ȼ������������ᷴӦ�Ƶù��ᣬ�ʴ�Ϊ��SiO2+2NaOH=Na2SiO3+H2O��Na2SiO3+2HCl�T2NaCl+H2SiO3����
�ܵ�����һ����Ҫ�Ĺ�ҵԭ�ϣ���ѧ�����ȶ����������������ʴ�Ϊ��������һ����Ҫ�Ĺ�ҵԭ�ϣ���ѧ�����ȶ���������������
���������
�����Ѷȣ�һ��
5��ѡ���� ��˵��AԪ�صķǽ����Ա�BԪ�صķǽ�����ǿ���ǣ�������
A��Aԭ�ӵõ����ӵ���Ŀ��Bԭ����
B��AԪ�ص�������۱�BԪ�ص��������Ҫ��
C����̬�⻯����ȶ��ԣ�A��Bǿ
D��A��������B���⻯��ˮ��Һ��Ӧ������B����
�ο��𰸣�A���õ�����Ŀ���ٲ���ȷ���ǽ����Ե�ǿ������A����
B��������۲��ܱȽϷǽ����ԣ���ǽ�����F��Cl����Fû�����ۣ���B����
C����̬�⻯���ȶ��ԿɱȽϷǽ�����ǿ������̬�⻯��Խ�ȶ��ǽ�����Խǿ����̬�⻯����ȶ��ԣ�A��Bǿ�����Էǽ����ԣ�A��Bǿ����C��ȷ��
D��A��������B���⻯�ﷴӦ����B���ʣ���A�õ�������ǿ���ǽ�����A��B����D��ȷ��
��ѡCD��
���������
�����Ѷȣ���