微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 实验室可用下列方法制取气体,其中必须用排水法收集的是( )
A.锌与稀硫酸反应
B.碳酸钙与稀盐酸反应
C.铜片与稀硝酸反应
D.二氧化锰与双氧水混合
参考答案:A、氢气在空气中能稳定存在且密度明显小于空气的密度,所以可用排空气集气法收集;氢气不易溶于水,和水不发生化学反应,所以可用排水法收集,故A错误.
B、二氧化碳在空气中能稳定存在且密度明显大于空气的密度,所以可用排空气集气法收集;二氧化碳能和水反应生成碳酸,溶解度较大,所以不能用排水法收集,故B错误.
C、一氧化氮能和空气中的氧气发生生成二氧化氮,即一氧化氮不能在空气中稳定存在,所以不能用排空气集气法收集;一氧化氮不易溶于水,和水不反应,所以能用排水集气法收集,故C正确.
D、氧气能够在空气中稳定存在且密度明显大于空气的密度,所以能用排空气集气法收集;氧气在水中的溶解度较小,和水不反应,所以能用排水集气法收集,故D错误.
故选C.
本题解析:
本题难度:简单
2、实验题 (13分)下表是实验室制备气体的有关内容:
编号
| 实验内容
| 实验原理
| 气体发生装置
|
①[
| 制备氧气
| H2O2→O2
| ?
|
②
| 制备氨气
| NH4Cl→NH3
| ?
|
③
| 制 备氯气 备氯气
| HCl→Cl2
| ?
|
(1)上述气体中:从制备过程看,必须选择合适的氧化剂才能实现的是?(填气体名称,下同);从反应原理看,明显不同于其他两种气体的是?。
(2)根据表中所列实验原理,从下列装置中选择合适的气体发生装置,将其编 号填入上表中的空格中。
号填入上表中的空格中。
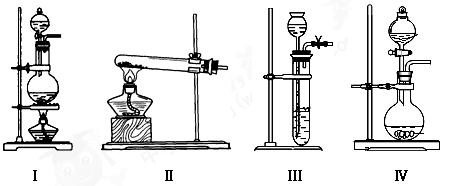
(3)某学习小组设计了如下图实验,将氯气依次通过下列装置以验证氯气的性质:
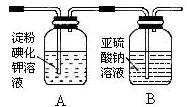 ?
?
①通入氯气后,A中的现象是?,整套实验装置存在的明显缺陷是?。
②请你帮该小组同学设计一个实验,证明洗气瓶B中的Na2SO3已被氧化:
?
(4)若用排空气法收集Cl2,在下边方框内画出气体收集装置图。?

(5)若将多余的Cl2用100 mL 1.7mol/L的NaOH溶液完全吸收。对吸收后的溶液进行分析化验,测知其pH等于13 (不考虑反应前后溶液的体积变化),ClO-和ClO3-的物质的量浓度之比为5∶1。则在整个过程中被氧化的氯气的物质的量为 ?mol。
?mol。
参考答案:(13分)?(1)Cl2(1分), NH3?(1分)
(2)①Ⅳ(1分)②Ⅱ(1分)③Ⅰ或Ⅳ(1分)
(3)①溶液变蓝色(1分);无尾气吸收装置(1分)
②取少量溶液于试管中,向其中滴加稀盐酸至不再产生气体,再 向其中滴加氯化钡溶液,若产生白色沉淀,则证明亚硫酸钠被氧化。(其他合理答案也给分)(2分)
向其中滴加氯化钡溶液,若产生白色沉淀,则证明亚硫酸钠被氧化。(其他合理答案也给分)(2分)
(4)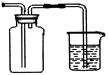 (2分)?(5)0.03?(2
(2分)?(5)0.03?(2 分)
分)
本题解析:略
本题难度:一般
3、选择题 下图是实验室制备CO2的简易装置,用该装置制备CO2可有随时使反应发生、也可以随时使反应停止的效果。下图中的装置与右图装置具有相同效果的是( )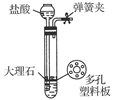

参考答案:D
本题解析:A、B、C均无法随时停止,D可以随用随制备,也能够随时停止。
本题难度:简单
4、实验题 (13分)(1)如图所示装置,为实现下列实验目的,其中y端适合于作入口的是_____多项)
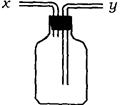
A 瓶内盛液体干燥剂,用以干燥气体
B 瓶内盛液体洗涤剂,用以除去某气体中的杂质
C 瓶内盛水,用以测量某难溶于水的气体的体积
D 瓶内贮存气体,加水时气体可被排出
E 收集密度比空气大的气体
F 收集密度比空气小的气体
(2) 浓H2SO4和木炭在加热时发生反应的化学方程式是_______________________。
图中虚线框中的装置可用来检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物,

填写下列空白。
①A中无水硫酸铜的作用_____________。
②证明SO2一定存在的现象是_____________。
③C中酸性KMnO4溶液的作用_____________。
④证明CO2一定存在的现象是_____________。
参考答案:(1)? A B E? (2) C+2H2SO4 CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
①检验水蒸气? ②B中品红褪色? ③除去SO2? ④D中品红不退色,E中变浑浊
本题解析:(1)由图可以看出y导管插入到试剂瓶的底部,因此可用来干燥某些气体,也可用来除去气体中的某些杂质,或者用来收集密度大于空气的某些气体。若瓶内盛水,用以测量某难溶于水的气体的体积,则进气口应是x导管。同样瓶内贮存难溶于水的气体,加水时气体可被排出,进气口同样应是x导管。收集密度比空气小的气体,进气口应是x导管。故正确的答案是A B E。
(2)浓硫酸具有强氧化性,在加热的条件下可氧化单质碳,方程式为C+2H2SO4 CO2↑+2SO2↑+2H2O。产物有三种水蒸气、CO2和SO2,验证水蒸气用无水硫酸铜,CO2用饱和石灰水,SO2用品红溶液。由于后两者都需要通过溶液,因此首先验证水蒸气。因为SO2也可以使石灰水变混浊,因此在检验CO2之前,需要先检验SO2,并且还要完全除去SO2,以避免干扰CO2的检验。
CO2↑+2SO2↑+2H2O。产物有三种水蒸气、CO2和SO2,验证水蒸气用无水硫酸铜,CO2用饱和石灰水,SO2用品红溶液。由于后两者都需要通过溶液,因此首先验证水蒸气。因为SO2也可以使石灰水变混浊,因此在检验CO2之前,需要先检验SO2,并且还要完全除去SO2,以避免干扰CO2的检验。
本题难度:一般
5、实验题 (13分)某研究性学习小组查阅资料得知:漂白粉与硫酸溶液反应可制取氯气,化学方程式为:Ca(C1O)2+CaCl2+H2SO4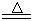 2CaSO4+2Cl2↑+2H2O,该组学生针对上述反应设计如下装置来制取氯气并验证其性质。
2CaSO4+2Cl2↑+2H2O,该组学生针对上述反应设计如下装置来制取氯气并验证其性质。
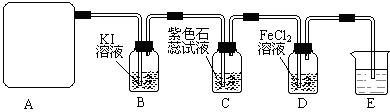
试回答下列问题:
(1)每生成1 mol Cl2,上述化学反应中转移的电子个数为______? (NA表示阿伏加德罗常数)。
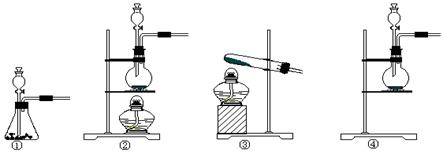
(2)该实验中A处可选用装置__________? _____ (填写装置的序号)。
(3)装置B中发生反应的离子方程式为________________________________________。
(4)装置C中的现象为___________________________________________________,
试结合反应方程式解释其原因 __________________________________?_
_________________________________?。
(5)装置E中的试剂是______________(任填一种合适试剂的名称),其作用是________
_______________________________? ______。
(6)请帮助该学习小组同学设计一个实验,证明装置D中有FeCl3生成(请简述实验 步骤)
步骤)
_________________________________________________________________________
_________________________ __________________________? ______________
__________________________? ______________
参考答案:(13分) (1) NA?(2分) ?
? ?(2) ②? (1分)? (3) Cl2+2I-=I2+2Cl-?(2分)
?(2) ②? (1分)? (3) Cl2+2I-=I2+2Cl-?(2分)
(4)紫色石蕊试液先变红后褪色(1分)? Cl2通入石蕊试液中发生反应Cl2+H2O=HC1+HC1O ,H+使石蕊试液变红,又因为HC1O具有强氧化性,使红色褪去(2分)
(5)氢氧化钠溶液(1分)? ?吸收多余的氯气,防止污染空气(2分)
?吸收多余的氯气,防止污染空气(2分)
(6)取装置D中的溶液于一支洁净试管中,滴加适量的KSCN溶液,溶液变成血红色,则证明有FeCl3生成(2分)
本题解析:略
本题难度:简单