微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
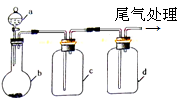
1、实验题 纳米碳酸钙广泛应用于橡胶、塑料、造纸、化学建材、油墨、涂料、密封胶与胶粘剂等行业。在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙。某校学生实验小组设计下图所示装置,制取该产品。D中装有蘸稀硫酸的脱脂棉,图中夹持装置已略去。
Ⅰ.可选用的药品有:
a.石灰石;b.饱和氯化钙溶液;c.6 mol/L盐酸;d.氯化铵;e.氢氧化钙
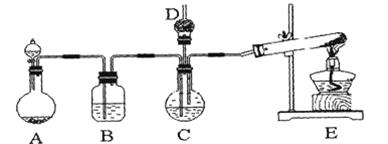
(1)A中制备气体时,所需药品是(选填字母序号)?;
(2)B中盛有饱和碳酸氢钠溶液,其作用是?;
(3)写出制取氨气的化学方程式?;
(4)在实验过程中,向C中通入气体是有先后顺序的,应先通入气体的化学式?;
(5)检验D出口处是否有氨气逸出的方法是?;
(6)写出制纳米级碳酸钙的化学方程式?。
(7)若实验过程中有氨气逸出,应选用下列?装置回收(填代号)。
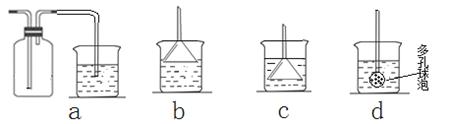
Ⅱ.经分析在上述氯化铵样品中含有杂质碳酸氢钠。为了测定氯化铵的质量分数,该学生实验小组又设计了如下实验流程:
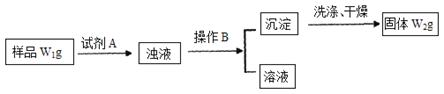
试回答:
(1)所加试剂A的化学式为?
(2)B操作方法是?
(3)样品中氯化铵的质量分数为?。
参考答案:Ⅰ.(1)ac(1分)(2)除去CO2中的HCl(1分)?
(3)2NH4Cl + Ca(OH)2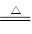 CaCl2 + 2NH3↑+ 2H2O?(4)NH3(1分)
CaCl2 + 2NH3↑+ 2H2O?(4)NH3(1分)
(5)将湿润的红色石蕊试纸放在D出口处,若试纸变蓝,则证明有氨气逸出;若试纸不变蓝,则证明没有氨气逸出。(或用蘸有浓盐酸的玻璃棒靠近D出口处,若有白烟,则证明有氨气逸出;若没有白烟,则证明没有氨气逸出。)(2分)
(6)CaCl2 + H2O + CO2 + 2NH3 = CaCO3 + 2NH4Cl(2分)
(7)b(1分)
Ⅱ.(1)Ca(OH)2或Ba(OH)2或AgNO3和HNO3(1分)?
(2)过滤(1分)
(3)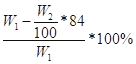 或
或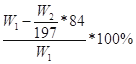 或53.5W2/143.5W1×100%
或53.5W2/143.5W1×100%
本题解析:Ⅰ.(1)分析题意知,装置A为碳酸钙与盐酸反应制二氧化碳,所需药品是石灰石和6mol/L盐酸,答案为:ac;(2)饱和NaHCO3溶液可除去二氧化碳中的氯化氢;(3)实验室制取氨气采用氯化铵和氢氧化钙加热,生成氯化钙、氨气和水,方程式为:2NH4Cl + Ca(OH)2 CaCl2 + 2NH3↑+ 2H2O;(4)氨气极易溶于水,先通入氨气利于二氧化碳的吸收,所以应先通入NH3;(5)氨气是碱性气体,能使红色石蕊试纸变蓝;氨气能和浓盐酸反应生成白烟,答案为:将湿润的红色石蕊试纸放在D出口处,若试纸变蓝,则证明有氨气逸出;若试纸不变蓝,则证明没有氨气逸出。(或用蘸有浓盐酸的玻璃棒靠近D出口处,若有白烟,则证明有氨气逸出;若没有白烟,则证明没有氨气逸出。);(6)制纳米级碳酸钙的化学方程式为:CaCl2+CO2+2NH3+H2O=CaCO3+2NH4Cl;(7)氨气极易溶于水要防止倒吸,答案为:b;
CaCl2 + 2NH3↑+ 2H2O;(4)氨气极易溶于水,先通入氨气利于二氧化碳的吸收,所以应先通入NH3;(5)氨气是碱性气体,能使红色石蕊试纸变蓝;氨气能和浓盐酸反应生成白烟,答案为:将湿润的红色石蕊试纸放在D出口处,若试纸变蓝,则证明有氨气逸出;若试纸不变蓝,则证明没有氨气逸出。(或用蘸有浓盐酸的玻璃棒靠近D出口处,若有白烟,则证明有氨气逸出;若没有白烟,则证明没有氨气逸出。);(6)制纳米级碳酸钙的化学方程式为:CaCl2+CO2+2NH3+H2O=CaCO3+2NH4Cl;(7)氨气极易溶于水要防止倒吸,答案为:b;
Ⅱ.(1)根据题目信息可知:碳酸氢钠能与氢氧化钡或氢氧化钙反应生成碳酸钡或碳酸钙沉淀,根据沉淀的质量求出碳酸氢钠的质量,最后求出氯化铵的质量以及质量分数;氯化铵能与硝酸酸化的硝酸银反应生成氯化银沉淀,根据沉淀的质量求出氯化铵的质量,最后求出氯化铵的质量分数;所以A为Ca(OH)2或Ba(OH)2或AgNO3和HNO3;(2)操作B为不溶物和溶液分离操作,用过滤的方法;(3)若试剂为Ca(OH)2溶液,根据碳守恒得关系式:NaHCO3――CaCO3,计算得NaHCO3的质量为84W2/100g,则氯化铵的质量为(W1―84W2/100)g,氯化铵的质量分数为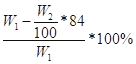 ,若试剂为Ba(OH)2溶液,同理可计算氯化铵的质量分数为
,若试剂为Ba(OH)2溶液,同理可计算氯化铵的质量分数为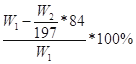 ,若试剂为AgNO3和HNO3,由关系式NH4Cl――AgCl计算得氯化铵的质量分数为53.5W2/143.5W1×100%。
,若试剂为AgNO3和HNO3,由关系式NH4Cl――AgCl计算得氯化铵的质量分数为53.5W2/143.5W1×100%。
本题难度:一般
2、实验题 (8分)在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如下图:
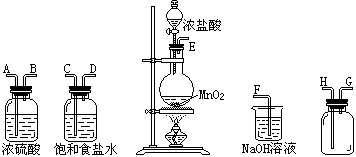
(1)?(2)?(3)?(4)?(5)
(1)连接上述仪器的正确顺序是(填各接口处的字母):?接?,_____接?,_____接?,?接?。
(2)在装置中:
①饱和食盐水起的作用是?,
②浓硫酸起的作用是?;
(3)该实验中收集氯气用的是?法,若图(2)装满饱和食盐水,也可以用来收集氯气,则收集时氯气应从?(填“C”或“D”)通入。
参考答案:(1)E接C,D接A,B接H,G接F
(2)洗气?干燥
(3)向上排空气? D
本题解析:略
本题难度:简单
3、选择题 用如图所示装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是
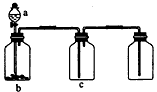
[? ]
气体
a
b
c
A.
NO2
浓硝酸
?铜片
NaOH溶液
B.
SO2
浓硝酸
Cu
酸性KMnO4溶液
C.
NH3
?浓氨水
生石灰
碱石灰
D.
CO2
?稀盐酸
CaCO3
?浓硫酸
参考答案:D
本题解析:
本题难度:一般
4、简答题 图Ⅰ是化学实验室中常用制备、干燥气体的部分仪器装置.某学校同学利用中学常用试剂及仪器设计下列实验.
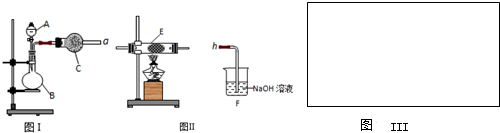
(1)图Ⅰ中仪器B的名称:______.
(2)同学甲利用图Ⅰ装置制备并收集干燥的NO2气体,请在方框内画出用集气瓶收集NO2的装置图______.B中发生反应的离子方程式为______.
(3)同学乙利用图Ⅰ装置通过称量反应前后C的质量,确定Na2CO3和NaCl固体混合物中Na2CO3的质量.A中加入稀硫酸,B中加入Na2CO3和NaCl固体混合物,C中加入碱石灰.该装置存在较多缺陷,从而导致实验误差较大,请你说出其中的两点缺陷:
①______;
②______.
(4)同学丙利用图Ⅰ装置制取氨气和氧气的混合气体,并且利用图Ⅱ装置验证氨的某些性质.A中加入浓氨水,C中加入碱石灰,E内放置催化剂(铂石棉),按气流方向连接各仪器a→b→c→h.
①B内需加入固体试剂的名称为______,B中能产生氨气和氧气混合气体的原因是______.
②实验中观察到E内有红棕色气体出现,证明氨气具有______性,E中发生反应的化学方程式为______.
参考答案:(1)图Ⅰ中仪器B是圆底烧瓶,故答案为:圆底烧瓶;
(2)二氧化氮气体易溶于水,所以不能用排水法收集;二氧化氮的密度大于空气的密度且和氧气不反应,所以可以采用向上排空气法收集,如图:
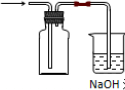
;
铜和稀硝酸反应生成硝酸铜、一氧化氮和水,离子方程式为:3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑,故答案为:

;3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑;
(3)CO2中混有的水蒸气也会被C吸收;干燥管与空气相通,空气中的CO2和水蒸气也会被吸收,从而导致实验误差较大,故答案为:CO2中混有的水蒸气也会被C吸收;干燥管与空气相通,空气中的CO2和水蒸气也会被吸收;
(4)①过氧化钠与H2O反应生成氢氧化钠和氧气,同时放出大量热,温度升高使浓氨水中氨的溶解度减小而逸出;氢氧化钠电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出;故答案为:过氧化钠;过氧化钠与浓氨水中的H2O反应生成氢氧化钠和氧气,同时放出大量热,温度升高使氨的溶解度减小而逸出,氢氧化钠电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出;
②氨气中氮元素的化合价是-3价,二氧化氮中氮元素的化合价是+4价,反应前后氮元素的化合价升高,所以氨气作还原剂,体现其还原性;氨气和氧气在一定条件下反应生成一氧化氮和水,一氧化氮和氧气能反应生成二氧化氮,反应方程式为:4NH3+5O2?催化剂?.加热4NO+6H2O、2NO+O2=2NO2,
故答案为:还原;4NH3+5O2?催化剂?.加热4NO+6H2O、2NO+O2=2NO2.
本题解析:
本题难度:一般
5、选择题 实验室中某些气体的制取、除杂及收集装置如图所示。仅用此装置和表中提供的物质完成相关实验,最合理的是
选项
| a中物质
| b中物质
| c中物质
| d中收集的气体
|
A
| 浓氨水
| CaO
| 浓H2SO4
| NH3
|
B
| 浓硫酸
| Na2SO3
| 浓H2SO4
| SO2
|
C
| 饱和食盐水
| 电石
| CuSO4溶液
| CH≡CH
|
D
| 浓盐酸
| MnO2
| 饱和NaCl溶液
| Cl2
|
?
参考答案:B
本题解析:A项中浓H2SO4吸收NH3。C项中CH≡CH的相对分子质量是26,不能用向上排气法;D项中发生装置需要加热。
本题难度:一般