微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 摩托罗拉公司研发了一种由甲醇和氧气以及强碱作电解质溶液的新型手机电池,电量可达现在使用的镍氢或锂电池的十倍,可连续使用一个月才充一次电,其电池反应式为
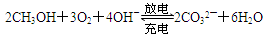 ,则下列有关说法错误的是( )
,则下列有关说法错误的是( )
A.放电时CH3OH参与反应的电极为正极
B.充电时电解质溶液的pH逐渐增大
C.放电时负极的电极反应式为CH3OH-6e-+8OH-===CO32―+6H2O
D.充电时每生成1 mol CH3OH转移6 mol电子
参考答案:A
本题解析:放电相当于原电池,所以甲醇在负极通入,电极反应式为CH3OH-6e-+8OH-===CO32―+6H2O。氧气在正极通入,电极反应式为O2+4e-+2H2O=4OH-。充电相当于电解,电极反应式相当于是原电池的逆反应,所以只有选项A是错误的,其余都是正确的,答案显A。
本题难度:一般
2、选择题 出土的锡青铜(铜锡合金)文物常有Cu2(OH)3Cl覆盖在其表面。下列说法正确的是
A.锡青铜的熔点比纯铜高
B.在自然环境中,锡青铜中的锡对铜起保护作用
C.锡青铜文物在潮湿环境中的腐蚀比干燥环境中慢
D.生成Cu2(OH)3Cl覆盖物是电化学腐蚀过程,但不是化学反应过程
参考答案:B
本题解析:合金的熔点一般低于各成分金属的熔点,A不正确。锡金属性强于铜,所以即使发生电化学腐蚀,锡也是负极,失去电子。铜是正极,被保护,B正确。潮湿的环境更溶液被腐蚀,C不正确。电化学腐蚀也是化学变化,D不正确。答案选B。
本题难度:一般
3、选择题 下列有关钢铁腐蚀与防护的说法正确的是
A.钢管与电源正极连接,钢管可被保护
B.铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀
C.钢管与铜管露天堆放在一起时,钢管不易被腐蚀
D.钢铁发生析氢腐蚀时,负极反应是Fe-3e-=Fe3+
参考答案:B
本题解析:A、电解时,阳极被腐蚀,阴极被保护;连接电源正极的电极为阳极,所以将地下输油钢管与外加直流电源的负极相连以保护它不受腐蚀,故A错误;
C、钢管中含有铁,和铜形成原电池,加速钢管的腐蚀,故C错误;
D、析氢腐蚀和吸氧腐蚀,负极上铁失电子发生氧化反应,所以负极均是Fe发生氧化反应Fe-2e-=Fe2+,故D错误。
故选B。
点评:本题考查了金属的腐蚀与防护,难度不大,会运用化学知识解决生产、生活问题,学以致用。
本题难度:简单
4、选择题 下列装置中,a5是铁电极,其余为石墨电极,烧杯中液体体积均为100 mL,放置一段时间后,有关叙述不正确的是(不考虑溶液体积变化)(?)
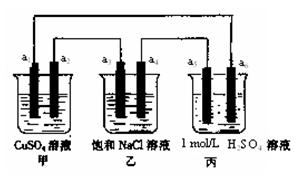 ?
?
A.a2电极上有亮红色固体
B.a1、a3电极上产生的物质,物质的量比是1:2
C.丙中的SO42-向a6电极移动
D.当装置电路中有6.02×1021个电子通过时,乙中溶液的pH是13
参考答案:C
本题解析:略
本题难度:一般
5、选择题 关于下图所示各装置的叙述中,正确的是?(?)
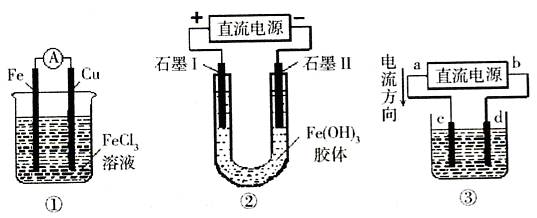
A.装置①是原电池,总反应是:Cu+2Fe3+=Cu2++2Fe2+
B.装置①中,铁做负极,电极反应式为:Fe3++e-=Fe2+
C.装置②通电一段时间后石墨Ⅱ电极附近溶液红褐色加深
D.若用装置③精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液
参考答案:
C
本题解析:
本题考查电化学知识;装置①为原电池,铁为负极,电极反应式为:Fe-2e-=Fe2+,铜为正极,总反应是Fe+2Fe3+=3Fe2+,A、B错误;装置②中,Fe(OH)3胶粒带正电,向阴极移动,阴极附近溶液颜色加深,C正确;粗铜精制,精铜做阴极,粗铜做阳极,电解质溶液为CuSO4溶液,D错误。
本题难度:一般