微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质中,与0.1molH2O含相同氢原子数的物质是
A.0.3molHNO3
B.0.1NA个H3PO4分子
C.2.4gCH4
D.标准状况下4.48LHCl
参考答案:D
本题解析:分析:根据N=nNA可知,H原子的物质的量相同,则H原子数目相同,结合各物质的量化学式计算含有的H原子数目,
解答:0.1molH2O含氢原子的物质的量0.2mol.
A、0.3molHNO3含氢原子的物质的量0.3mol,故A错误;
B、0.1NA个H3PO4分子中含有氢原子的物质的量0.3mol,故B错误;
C、2.4gCH4含氢原子的物质的量 ×4=0.6mol,故C错误;
×4=0.6mol,故C错误;
D、标准状况下4.48LHCl含有氢原子的物质的量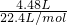 ×1=0.2mol,故D正确.
×1=0.2mol,故D正确.
故选:D.
点评:考查物质的量的有关计算,难度较小,注意公式的利用,加强基础知识的掌握.
本题难度:简单
2、选择题 将4.8gCO和H2的混合气体与足量O2充分燃烧后,立即通入足量的Na2O2固体中,固体的质量增加
A.2.1g
B.3.6g
C.4.8g
D.无法确定
参考答案:C
本题解析:试题分析:CO和氢气燃烧的化学方程式分别是2CO+O2=2CO2、2H2+O2=2H2O,生成的水和CO2分别和过氧化钠反应的化学方程式是2H2O+2Na2O2=4NaOH+O2、2CO2+2Na2O2=2Na2CO3+O2,即反应前消耗的氧气,在和过氧化钠的反应中又重新产生,因此反应可以看作是H2+Na2O2=2NaOH、CO+Na2O2=2Na2CO3,所以固体增加的质量就是原混合气的质量,答案选C。
考点:考查过氧化钠的有关计算
点评:本题属于常见的高考题型,属于中等难度的试题。如果将固体进一步拓展,则凡是符合通式(H2)n(CO)m的,只要是完全燃烧后,其产物通过足量的过氧化钠后,固体增加的质量就是原物质的质量,抓住该规律,这类试题即可迎刃而解。
本题难度:困难
3、选择题 物质的体积一定是22.4L的是
A.1?mol氧气
B.标准状况下44?g二氧化碳
C.0℃、2×105?Pa时2?g氢气
D.17?g氨气
参考答案:B
本题解析:分析:标准状况下1mol气体的体积约为22.4L,依据概念进行分析计算判断.
解答:A、1mol氧气,在标准状况下体积是22.4L,但温度压强不知,体积不一定是22.4L,故A错误;
B、标准状况下44g二氧化碳,为1mol,所以标准状况下气体体积为22.4L,故B正确;
C、0℃、2×105Pa时2g氢气物质的量是1mol,但不是标准状况下,所以体积不一定为22.4L,故C错误;
D、17g氨气物质的量为1mol,但具体温度和压强不知,无法判断,故D错误;
故选B.
点评:本题考查了气体摩尔体积的概念和应用条件,注意物质的状态必须是气体.题目较简单.
本题难度:一般
4、选择题 某NaOH溶液的溶质质量分数是10%,则此溶液中Na+与H2O的个数比为
A.1:10
B.1:20
C.1:11.5
D.1:23
参考答案:B
本题解析:分析:令溶液的质量为100g,则氢氧化钠的质量为10g,水的质量为100g-10g=90g,根据n= 计算氢氧化钠、水的物质的量,钠离子的物质的量等于氢氧化钠的物质的量,物质的量之比等于分子数之比,据此计算判断.
计算氢氧化钠、水的物质的量,钠离子的物质的量等于氢氧化钠的物质的量,物质的量之比等于分子数之比,据此计算判断.
解答:令溶液的质量为100g,则氢氧化钠的质量为10g,水的质量为100g-10g=90g.
10g氢氧化钠的物质的量为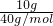 =0.25mol,所以钠离子的物质的量为0.25mol.
=0.25mol,所以钠离子的物质的量为0.25mol.
90g水的物质的量为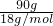 =5mol.
=5mol.
所以此溶液中Na+与H2O的个数比为0.25mol:5mol=1:20.
故选:B.
点评:考查常用化学计量的有关计算、质量分数,难度不大,关键清楚溶液的组成,注意基础知识的掌握.
本题难度:困难
5、选择题 用NA代表阿伏加德罗常数值.下列说法正确的是
A.2.3g钠在空气中加热反应时,失去的电子数为0.2NA
B.标准状况下,1.12L的HCHO所含的原子数为0.2NA
C.28g?C2H4和C4H8混合物中所含的分子数为3NA
D.1mol?FeCl3与沸水反应生成胶体后,含有NA个Fe(OH)3胶粒
参考答案:B
本题解析:分析:A、质量换算物质的量,计算失去电子数,钠加热反应生成过氧化钠;
B、根据气体摩尔体积的条件应用计算判断;
C、依据质量和摩尔质量换算物质的量计算分子数;
D、胶体微粒是氢氧化铁的集合体;
解答:A、2.3g钠物质的量为0.1mol,完全反应转移电子数为0.1NA,故A错误;
B、标准状况下,甲醛是气体,1.12L的HCHO物质的量为0.05mol,含原子数为0.05mol×4×NA=0.2NA,故B正确;
C、28g C2H4和C4H8混合物中含分子数,若全是C2H4分子数= ×NA=NA,若全是C4H8分子数=
×NA=NA,若全是C4H8分子数= =0.5mol,所以28g C2H4和C4H8混合物中含分子数在0.5NA-NA间,故C错误;
=0.5mol,所以28g C2H4和C4H8混合物中含分子数在0.5NA-NA间,故C错误;
D、Fe(OH)3胶粒是氢氧化铁的微粒集合体,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的应用,质量换算物质的量计算微粒数,气体摩尔体积的条件应用,胶体微粒的组成,熟练掌握概念和计算,即可解决.
本题难度:简单