��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
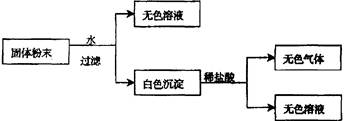
1���ж��� (4��)��һ�������ĩ����CaCO3��Na2SO4��KNO3��BaCl2��CuSO4�е�����������ɣ�ȡ��Ʒ��������ʵ�飺
��ʵ������жϣ��ù����ĩ��
��1��һ��������?��
��2��д����ɫ����ķ���ʽ?��
�ο��𰸣���1��CuSO4����2�� CO2
�������������ͼ��֪�������ĩ����ˮ�õ���ɫ��Һ������һ��û��CuSO4���õ��İ�ɫ������ȫ������ϡ���ᣬ����һ����CaCO3��������������CO2��
���������⿼��ѧ�����������������������
�����Ѷȣ���
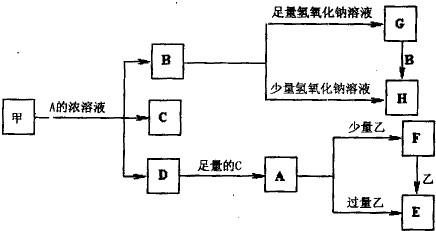
2������� ��ѧ��ѧ�г����ļ������ʴ������¹�ϵ�����м��Ǻ�ɫ�ǽ������ʣ����������г����Ľ������ʣ�D�Ǻ���ɫ���壮��ͼ�в��ֲ���ͷ�Ӧ��������ȥ��
�ش��������⣺
��1��д������A��Ũ��Һ��Ӧ�Ļ�ѧ����ʽ______��
��2�����������Ũ�ȵ�G��Һ��H��Һ��Ϻ�õ�����Һ�е�����Ũ�ȴ�С��ϵΪ______��
��3����ȥG�����к���H���ʲ��õķ�����______��
��4��A��Һ��һ����ʹʪ��ĺ�ɫʯ����ֽ����ɫ�����巴Ӧ������һ���Σ����ε���Һ�����ԣ���ԭ���ǣ������ӷ���ʽ��ʾ��______��
��5��д����E��Һ�м�������ϡ�����Ӧ�����ӷ���ʽ______������ҺF�������ɡ����յ��������ټ���ʱ���ù������ʵĻ�ѧʽΪ______��
��6��ȷ��E��������ʵ��ķ���Ϊ______��
�ο��𰸣�D�Ǻ���ɫ���壬˵��D�Ƕ������������Ǻ�ɫ�ǽ������ʣ��Һ�A��Ũ��Һ��Ӧ���ɶ���������˵������̼��A��Һ��Ũ���ᣬ��B�Ƕ�����̼��C��ˮ��������̼����������������Һ��Ӧ����̼���ƺ�ˮ����������̼����������������Һ��Ӧ����̼�����ƺ�ˮ������G��̼���ƣ���H��̼�����ƣ�����������ˮ��Ӧ�������������������ҷ�Ӧ����F�������ҷ�Ӧ����E��F�����ֿ�����E����֪��Ϊ����������FΪ��������EΪ����������
��1��D�Ǻ���ɫ���壬˵��D�Ƕ����������ɼ��Ǻ�ɫ�ǽ������ʣ��Һ�A��Ũ��Һ��Ӧ���ɶ���������˵������̼��A��Һ��Ũ���ᣬ��B�Ƕ�����̼��C��ˮ����Ӧ�Ļ�ѧ����ʽΪ��C+4HNO3��Ũ��?��?.??CO2��+4NO2��+2H2O���ʴ�Ϊ��C+4HNO3��Ũ��?��?.??CO2��+4NO2��+2H2O��
��2��̼���ƺ�̼�����ƵĻ��Һ�У�̼�����ˮ��̶ȴ���̼�������ˮ��̶ȣ���Һ��ʾ���ԣ�����Ũ�ȴ�С��ϵ�ǣ�c��Na+����c��HCO3-����c��CO32-����c��OH-����c��H+�����ʴ�Ϊ��c��Na+����c��HCO3-����c��CO32-����c��OH-����c��H+����
��3��̼���������ȷֽ�Ϊ̼���ơ�ˮ�Լ�������̼����̼���������ȶ��������ü��ȷ���ȥ̼�����е�̼�����ƣ��ʴ�Ϊ�����ȣ�
��4����ʹʪ��ĺ�ɫʯ����ֽ����ɫ�����巴Ӧ�ǰ���������Ͱ�����Ӧ��������泥�����笠�ˮ�����Һ��ʾ���ԣ��ʴ�Ϊ��NH4++H2O

NH3?H2O+H+��
��5�������������м������ᣬ����ڴ������ᣬ������Խ���������������ʵ���ǣ�3Fe2++NO3-+4H+=3Fe3++NO��+2H2O�����������ױ���������Ϊ��������������ˮ�������������������ȷֽ�Ϊ���������ʴ�Ϊ��3Fe2++NO3-+4H+=3?Fe3++NO��+2H2O��Fe2O3��
��6�����������ױ�����Ϊ���������������������������ʾ��ɫ���������ӵļ��鷽�����ȼ���KSCN��Һ�ޱ仯�ټ�����ˮ��������ȣ���Һ���ɫ���ʴ�Ϊ���ȼ���KSCN��Һ�ޱ仯���ټ�����ˮ��������ȣ���Һ���ɫ��
���������
�����Ѷȣ���
3������� ��8�֣���ͼ�и����ʾ�Ϊ��ѧ��ѧ�г��������ʣ�����֮������ͼת����ϵ������A��C��Ϊ�������ʣ�D����ɫ��Ӧ�ʻ�ɫ��C��ˮ��Ӧ��������D������������Ȼ����������壻E��һ��������������ܸ�NaOH��Ӧ���ܸ����ᷴӦ������Ӧ���������ɵ�ˮ��������������ȥ��

��ش��������⣺
��1��B��_________��E��_________�����ѧʽ��
��2��д��Eת��ΪG�����ӷ���ʽ?��
��3��д��C��ˮ��Ӧ�Ļ�ѧ����ʽ??��
�ο��𰸣�
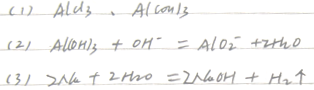
�����������
�����Ѷȣ�һ��
4������� ����A��B��C��D��E�������ʣ�A��B?�����ֳ����ĵ��ʣ�C��D��E�����ֳ����Ļ��������֮����ת����ϵ��ͼʾ��
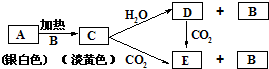
��1��д��A��B��C��D��E�Ļ�ѧʽ��
A______?B______?C______D______?E______
��2��д��Cת��ΪD�Ļ�ѧ����ʽ��______д��Dת��ΪE�����ӷ���ʽ��______��
�ο��𰸣�����A��B����ɫ�仯����֪AΪNa��CΪNa2O2��BΪO2����DΪNaOH��EΪNa2CO3����
��1�������Ϸ�����֪AΪNa��BΪO2��CΪNa2O2��DΪNaOH��EΪNa2CO3���ʴ�Ϊ��Na��O2��Na2O2��NaOH��Na2CO3��
��2��Na2O2��ˮ��Ӧ����NaOH��O2����Ӧ�ķ���ʽΪ2Na2O2+2H2O=4NaOH+O2����
CO2��NaOH��Ӧ�����ӷ���ʽΪCO2+2OH-=CO32-+H2O��
�ʴ�Ϊ��2Na2O2+2H2O=4NaOH+O2����CO2+2OH-=CO32-+H2O��
���������
�����Ѷȣ�һ��
5������� A��B��C��D����ѧ��ѧ�������������ʣ����ǵ�ת����ϵ���£�A+B=C+D
��1����A��B��C���Ƿǽ����������C�ڿ������ױ��A����A�з���Ԫ�ص���̬�⻯��M�ĵ���ʽΪ______�����ӵ��ȶ���B______M�����������������=������
��2����A��D�����ֵ��ʣ�B�Ǻ�ɫ�д��Ե������B�����ᷴӦ������ҺN������N��Һ�еͼ۽��������ӵķ�����______����D�ķ�ĩ������ҺN�У�����28gD��ȫ�ܽ�ʱ���÷�Ӧת�Ƶĵ�����______mol��
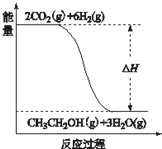
��3����A��B��C��D������Ӧ��2CO2��g��+6H2��g���TCH3CH2OH��g��+3H2O��g����������ͼ��ʾ��Ϣ��
�ٷ�Ӧ��______��Ӧ������ȡ������ȡ������ж�������______��
������H=aKJ/mol�������ı����5.6LCO2ʱ�ķ�Ӧ�ȡ�H=______KJ/mol��
���ں��¡����ݵ��ܱ������У�����������˵��������Ӧ�Ѵﻯѧƽ��״̬����______������ĸ��ţ���
A������1molCH3CH2OH��ͬʱ������3molH2OB�������и���ݵ����ʵ���Ũ�Ȳ���ʱ����仯
C�������л��������ܶȲ���ʱ����仯 D������������ķ�����������ʱ����仯��
�ο��𰸣���1����A��B��C���Ƿǽ����������C�ڿ������ױ��A��A��CΪͬ��Ԫ�������Ӧ�Ƕ���������ˮ��Ӧ����������NO��AΪNO2��BΪH2O��CΪNO��DΪ���ᣬ��A�з���Ԫ�ص���̬�⻯��MΪNH3��NH3������Nԭ����Hԭ��֮���γ�1�Թ��õ��Ӷԣ������ʽΪ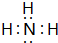 ���ǽ�����O��N�����⻯���ȶ���H2O��NH3��
���ǽ�����O��N�����⻯���ȶ���H2O��NH3��
�ʴ�Ϊ��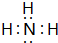 ������
������
��2��B�Ǻ�ɫ�д��Ե������BΪFe3O4����A��D�����ֵ��ʣ�Ϊ�û���Ӧ����DΪFe��Fe3O4�����ᷴӦ����FeCl3��FeCl2��Һ��ȡ������Һ���Թ��У�����K3Fe��CN��6��Һ����������ɫ������˵����Fe2+����Fe����������Һ�У�������ӦFe+2Fe3+=3Fe2+��28gFe�����ʵ���=28g56g/mol=0.5mol����Ӧ��FeԪ�ػ��ϼ���0������Ϊ+2����ת�Ƶ������ʵ���=0.5mol��2=1mol��
�ʴ�Ϊ��ȡ������Һ���Թ��У�����K3Fe��CN��6��Һ����������ɫ������˵����Fe2+��1��
��3������ͼ��֪����Ӧ���������������������������÷�ӦΪ���ȷ�Ӧ��
�ʴ�Ϊ�����ȣ���Ӧ��������������������������
��5.6L������̼�����ʵ���=5.6L22.4L/mol=0.25mol��ͼ�С�H=aKJ/mol����ʾ2mol������̼��Ӧʱ�ķ�Ӧ�ȣ���5.6LCO2ʱ�ķ�Ӧ�ȡ�H=aKJ/mol��0.25mol2mol=0.125aKJ/mol��
�ʴ�Ϊ��0.125a��
��A������1molCH3CH2OH��ͬʱ������3molH2O����Ӧʼ�հ��˱������У�����˵������ƽ�⣬��A����
B��ƽ��ʱ����Ӧ��������ֵ����ʵ���Ũ�Ȳ���ʱ����仯����B��ȷ��
C���������ݻ����䣬�����������������䣬��������ܶ�ʼ�ղ��䣬�ܶȲ���ʱ����仯������˵������ƽ�⣬��C����
D������ӦΪ�������ʵ�����С�ķ�Ӧ������������ķ�����������ʱ����仯��˵������ƽ�⣬��D��ȷ��
��ѡBD��
���������
�����Ѷȣ�һ��