微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在一量筒中充入1/4体积的Cl2气、1/4体积的N2气和1/2体积的H2气,让日光照射一段时间,待混合气体完全变成无色后,立即将其倒立于盛水的水槽中,则在相同条件下进入量筒中水的体积占量筒容积的
A.1/2
B.1/3
C.1/4
D.3/4
参考答案:A
本题解析:日光照射后1/4体积的Cl2气会和1/4体积的H2气反应生成1/2体积的HCl气,再倒置水槽,1/2体积的HCl气会溶于水中,此时只剩下1/4体积的H2气和1/4体积的N2气,所以选择A项。
点评:分清参与反应的物质以及反应的量,很容易就得到正确答案,属于简单题型
本题难度:一般
2、填空题 二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂。
(1)氯化钠电解法是一种可靠的工业生产ClO2方法。
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO42-等杂质。其次除杂操作时,往粗盐水中先加入过量的________(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO42-,其原因是___________【已知:Ksp(BaSO4)= 1.1 ×10-10 Ksp(BaCO3)= 5.1 ×10-9】
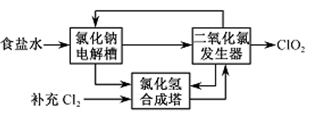
②该法工艺原理如右。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。
工艺中可以利用的单质有____________(填化学式),发生器中生成ClO2的化学方程式为___________。
(2)纤维素还原法制ClO2是一种新方法,其原理是:纤维素水解得到的最终产物D与NaClO3反应生成ClO2。完成反应的化学方程式:
□?(D)?+24NaClO3+12H2SO4=□ClO2↑+□CO2↑+18H2O+□_________
(3)ClO2和Cl2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-。处理含CN-相同量得电镀废水,所需Cl2的物质的量是ClO2的_______倍
参考答案:
(1)①BaCl2
BaSO4和BaCO3的Ksp相差不大,当溶液中存在大量CO32-时,BaSO4(s)会部分转化为BaCO3(s)(或其它合理答案)
②H2、Cl2
2NaClO3 + 4HCl  ?2ClO2↑ + Cl2↑ + 2NaCl + 2H2O
?2ClO2↑ + Cl2↑ + 2NaCl + 2H2O
(2)1C6H12O6+ 24 NaClO3 + 12H2SO4 24 ClO2↑ + 6 CO2↑ + 18H2O + 12 Na2SO4
24 ClO2↑ + 6 CO2↑ + 18H2O + 12 Na2SO4
(3)2.5
本题解析:
(1)①在除杂的过程中每步加入的试剂必须是过量的,使离子除尽;过量的离子在下一步中必须出去,故先加入BaCl2,除去硫酸根,过量的钡离子,加入Na2CO3除去。根据提供的Ksp数据,在后面加入碳酸钠时,发生BaSO4(s)+ CO32- (aq)= BaCO3(s)+SO42- (aq)。②电解饱和食盐水生成H2、Cl2和NaOH;故可以利用的单质为H2、Cl2,合成HCl。根据流程图可知加入物质为NaClO3和HCl,生成ClO2;可以写出方程式,并用化合价升降法配平得到。
(2)纤维素为多糖,水解最终产物为葡萄糖(C6H12O6),具有还原性,可将NaClO3还原得到ClO2。Cl从+5到+4价,降低1价,葡萄糖(C6H12O6)C均价为0,到+4价,升高4价,然后配平得到。
(3)每摩尔Cl2得到2mol电子,而没摩尔ClO2得到5mol电子,故为2.5倍。
【考点定位】考查化学工艺流程,涉及氧化还原反应相关概念、配平及计算,化学实验基本方法(除杂)等相关知识。
本题难度:一般
3、选择题 实验室用浓盐酸与二氧化锰反应制取氯气,下列说法中正确的是(气体体积均在标准状况下测定)
A.若提供0.4molHCl,MnO2不足量,则可制得氯气2.24L
B.若提供0.4molHCl,MnO2过量,则可制得氯气2.24L
C.若有0.4molHCl参与反应,MnO2不足量,则可制得氯气2.24L
D.若有0.4molHCl被氧化,MnO2不足量,则可制得氯气2.24L
参考答案:C
本题解析:A错,HCL不能完全反应;B错,随反应的不断进行,浓盐酸会变为稀盐酸,稀盐酸不能与二氧化锰反应生成氯气;C正确;D错,若有0.4molHCl被氧化,MnO2不足量,则可制得氯气4.48L
本题难度:一般
4、选择题 湿润的蓝色石蕊试纸放入盛有氯气的集气瓶中,对观察到的现象描述正确的是
A.变红
B.先变红后褪色
C.变白
D.不变色
参考答案:B
本题解析:略
本题难度:简单
5、选择题 下列说法正确的是
A.在漂白粉中滴入70%的硫酸,立刻产生黄绿色气体,说明硫酸具有还原性
B.粗锌与稀硫酸反应比纯锌快,说明粗锌反应时形成了原电池
C.硬水含有Ca2+、Mg2+、HCO3-、SO42-,煮沸可以完全除去其中的Ca2+、Mg2+
D.pH相同的两种一元酸HA溶液和HB溶液与足量Zn反应,HA比HB反应速率快,说明HA酸性更强
参考答案:B
本题解析:漂白粉中滴入70%的硫酸,立刻产生黄绿色气体次氯酸受热分解产生氯气。硬水煮沸无法完全除去其中的Ca2+、Mg2+,只是将其软化。pH相同的两种一元酸HA溶液和HB溶液与足量Zn反应,HA比HB反应速率快,说明HA酸性更强或者浓度高。
本题难度:简单