微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在用Zn片、Cu片和稀硫酸组成的电池装置中,经过一段时间工作后,下列说法中正确的是
A.锌片是正极,铜片上有气泡产生
B.电流方向是从锌片流向铜片
C.溶液中的阳离子向正极移动,阴离子向负极移动
D.电解液的PH值逐渐减少
参考答案:C
本题解析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。锌比铜活泼,则锌是负极,铜是正极,溶液中的氢离子在正极得到电子,因此选项C正确,A、B不正确,D不正确,溶液中的pH增大,D不正确,答案选C。
点评:该题是基础性试题的考查,也是高考中的常见题型和考点,有利于培养学生的逻辑推理能力。该题的关键是明确原电池的工作原理,然后结合题意和装置图灵活运用即可。
本题难度:一般
2、选择题 在盛有稀硫酸的烧杯中放入导线连接的锌片和铜片,下列叙述正确的是( )
A.正极有O2逸出
B.铜片上有H2逸出
C.正极附近的SO42-离子浓度逐渐增大
D.电子通过导线由铜片流向锌片
参考答案:A、正极上氢离子得电子生成氢气,有H2逸出故A错误;
B、铜片作正极,正极上氢离子得电子生成氢气,故B正确;
C、原电池放电时,溶液中阴离子向负极移动,所以阴极附近的SO42-浓度逐渐增大,故C错误;
D、原电池放电时,电子从负极沿导线流向正极,即电子通过导线由锌片流向铜片,故D错误.
故选B.
本题解析:
本题难度:简单
3、选择题 下图为某兴趣小组制作的番茄电池,下列说法正确的是
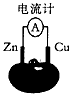
[? ]
A.电子由锌通过导线流向铜
B.该装置将电能转化为化学能
C.锌电极发生还原反应
D.铜电极上无气泡产生
参考答案:A
本题解析:
本题难度:一般
4、选择题 一学生欲通过实验判断X,Y,Z,W四块金属的活泼性,做了如下实验并得结论:当X,Y组成原电池时,Y为负极;当Z,W组成原电池时,W为正极;W能将Y从其盐溶液中置换出来,据此可知它们的活泼性顺序是( )
A.Z>W>X>Y
B.X>Y>Z>W
C.X>Y>W>Z
D.Z>W>Y>X
参考答案:当X,Y组成原电池时,Y为负极,说明活泼性Y>X,当Z,W组成原电池时,W为正极,说明Z做原电池的负极,所以活泼性Z>W,W能将Y从其盐溶液中置换出来,说明活泼性W>Y,综上可知金属的活泼性顺序是Z>W>Y>X.
故选D.
本题解析:
本题难度:一般
5、选择题 如图是某固体酸燃料电池基本结构示意图,其中以Ca(HSO4)2固体为电解质传递H+,电池总反应式为:2H2+O2=2H2O,下列有关说法不正确的是(? )
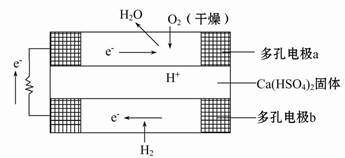
A.H2通过多孔电极时能增大H2的接触面积,加快反应
B.a极上的电极反应式为:O2+2H2O+4e-=4OH-
C.每转移0.1 mol电子,消耗标准状况下的H2 1.12 L
D.H+由b极通过固体酸电解质传递到a极
参考答案:B
本题解析:由电极反应式可知,氢气通入的一极为负极,氧气通入的一极为正极,故a为正极、b为负极,因此b电极产生的H+通过固体电解质流向a极,故D选项是正确的;a极上的电极反应式应为O2+4e-+4H+=2H2O,故B选项是错误的;根据电池的反应式可以得出转移0.1 mol电子,消耗H2的物质的量为0.05 mol,在标准状况下的体积为1.12 L,故C选项是正确的;b电极的材料是多孔物质,能够增大H2反应的接触面积,加快反应的速率,故A选项是正确的
本题难度:一般