| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学必备知识点《原电池原理》答题技巧(2017年最新版)(十)
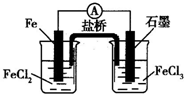 参考答案:A、装置图是原电池反应,石墨电极上是铁离子得到电子发生还原反应,故A错误; 本题解析: 本题难度:一般 2、选择题 如图为铜锌原电池示意图,下列说法正确的是( ) |
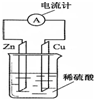
参考答案:A、因Zn作负极,则Zn失去电子而逐渐溶解,故A正确;
B、由发生电池反应为Zn+H2SO4═ZnSO4+H2↑,Cu不反应,则烧杯中溶液为无色,故B错误;
C、Zn作负极,Cu作正极,则电子由锌片通过导线流向铜片,故C错误;
D、该装置通过化学反应将化学能转变为电能,故D错误;
故选A.
本题解析:
本题难度:简单
3、填空题 (14分)(Ⅰ)如图所示:
(1)若开始时开关K与a连接,则铁发生电化学腐蚀中的________腐蚀。请写出正极反应式 。
(2)若开始时开关K与b连接时,两极均有气体产生,则N端是电源的 极(填正或负)则总反应的离子方程式为 。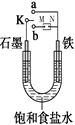
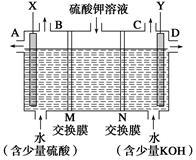
(Ⅱ)用如图装置电解硫酸钾溶液来制取氧气、氢气、硫酸和氢氧化钾。
(1)X极与电源的_____(填“正”或“负”)极相连,氢气从_____(填“A、B、C或D”)口导出。
(2)已知离子交换膜只允许一类离子通过,则M为________(填“阴离子”或“阳离子”)交换膜。
(3)若制得标准状况下5.6 L氧气,则生成氢氧化钾的质量是____________。
参考答案:(1)吸氧(2分) O2 + 4e- +2H2O =4OH-(2分)
(2)负(2分) 2Cl- + 2H2O Cl2↑+2OH-+H2↑(2分) (3)正 C (2分)
Cl2↑+2OH-+H2↑(2分) (3)正 C (2分)
(4)阴离子 (2分) (5)56g (2分)
本题解析:(Ⅰ)(1)若开始时开关K与a连接,则构成原电池,铁是负极,石墨是正极,由于是氯化钠溶液,因此铁发生电化学腐蚀中的吸氧腐蚀,其中正极反应式为O2 + 4e- +2H2O =4OH-。
(2)若开始时开关K与b连接时,两极均有气体产生,这说明此时是电解池,铁是阴极,溶液中的氢离子放电,而石墨是阳极,溶液中的氯离子放电,实验N端是电源的负极,总反应的离子方程式为2Cl- + 2H2O Cl2↑+2OH-+H2↑。
Cl2↑+2OH-+H2↑。
(Ⅱ)(1)题图中左边加入含硫酸的水,右侧加入含KOH的水,说明左边制硫酸,右边制备KOH溶液,氢氧根离子在阳极放电,同时电解后溶液呈酸性,氢离子在阴极放电,同时电解后溶液呈碱性,则X为阳极,Y为阴极,所以X连接电源正极;Y电极上氢离子放电生成氢气,所以氢气从C口导出。
(2)OH-在阳极发生氧化反应,使左边溶液中H+增多,为了使溶液呈电中性,硫酸钾溶液中的SO42-通过M交换膜向左边迁移,即M为阴离子交换膜。
(3)标准状况下5.6L氧气的物质的量是5.6L÷22.4L/mol=0.25mol,则根据电极反应式4OH--4e-
本题难度:一般
4、选择题 根据反应为 2Cu+O2+CO2+H2O=Cu2(OH)2CO3,
设计如下图所示原电池,下列说法错误的是 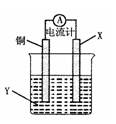
A.X可以是银或石墨
B.电子从铜电极经外电路流向X电极
C.Y是硫酸铜溶液
D.X极上的电极反应式为 O2+2H2O+4e- = 4OH-
参考答案:C
本题解析:略
本题难度:一般
5、选择题 下列不属于化学电源的是( )
A.碱性锌锰干电池
B.铅蓄电池
C.氢氧燃料电池
D.太阳能电池
参考答案:常见的电源:蓄电池、干电池、燃料电池,可以将化学能转化为电能,而太阳能电池是太阳能转化为电能的装置,
故选:D.
本题解析:
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学必备知识点《化学基本理.. | |