微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
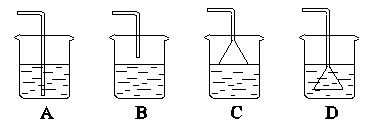
1、选择题 为了使HCl气体被水溶解,最合适的实验装置是(图4-4)()
 ?
?
图4-4
参考答案:C
本题解析:因为HCl气体极易溶于水,如果用导管直接插入水中,会引起水的倒流,所以必须用倒置的漏斗,且漏斗应刚接触水面,不应插入太深,否则还会引起倒吸,故答案为C。
本题难度:简单
2、选择题 下列氯化物中,不能用金属和氯气直接反应制得的是( )
A.CuCl2
B.NaCl
C.FeCl2
D.MgCl2
参考答案:Cl2有强氧化性,与金属反应化合生成相应的盐(氯化物),当与变价金属反应时将金属氧化成高价态,故A、B、D正确;与Fe反应生成FeCl3,故C错.
故选C
本题解析:
本题难度:简单
3、选择题 下列对有关反应现象的描述正确的是( )
A.将Cl2和SO2分别通入石蕊试液中,先变红后褪色
B.将CO2和SO2分别通入CaCl2溶液中,先变浑浊后变澄清
C.将氨水分别滴入AlCl3和AgNO3溶液,先变浑浊后变澄清
D.将湿润的KI淀粉试纸分别伸入盛NO2和O3试管中,试纸变蓝
参考答案:A.SO2只能使酸碱指示剂变色,通入石蕊试液中,溶液变红,故A错误;
B.CO2和SO2与CaCl2溶液都不反应,不能生成沉淀,故B错误;
C.氨水分别滴入AlCl3溶液中生成Al(OH)3,Al(OH)3不溶于氨水,溶液只变浑浊,故C错误;
D.NO2和O3都可氧化KI生成碘单质,淀粉变蓝,故D正确.
故选D.
本题解析:
本题难度:一般
4、选择题 实验室常用下列三个反应制备Cl2:①MnO2?与浓盐酸反应制备氯气;②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2?+8H2O;?③KClO3+6HCl(浓)=KCl+3Cl2?+3H2O如果分别用上述方法制得等量的Cl2,下列说法中正确的是? ( ?)
A.参加反应的HCl的物质的量相等
B.转移电子的总数相等
C.消耗氧化剂的物质的量相等
D.被氧化的氯离子数不相等
参考答案:D
本题解析:A错,MnO2?与浓盐酸反应制备氯气方程式为: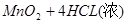 ====
====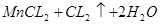 ;每生成1mol氯气参加反应的HCL的物质的量为4mol;2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2?+8H2O;每生成1mol氯气参加反应的HCL的物质的量为3.2mol;③KClO3+6HCl(浓)=KCl+3Cl2?+3H2O;每生成1mol氯气参加反应的HCL的物质的量为2mol;
;每生成1mol氯气参加反应的HCL的物质的量为4mol;2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2?+8H2O;每生成1mol氯气参加反应的HCL的物质的量为3.2mol;③KClO3+6HCl(浓)=KCl+3Cl2?+3H2O;每生成1mol氯气参加反应的HCL的物质的量为2mol;
B错,反应①中每生成1mol氯气转移的电子总数为2mol;反应②中每生成1mol氯气转移的电子总数为2mol;反应③中中每生成1mol氯气转移的电子总数为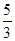 mol;C错,反应①中每生成1mol氯气消耗氧化剂MnO2?的物质的量为1mol;反应②中每生成1mol氯气消耗氧化剂KMnO4的物质的量为0.4mol;反应③中中每生成1mol氯气消耗氧化剂KClO3的物质的量为
mol;C错,反应①中每生成1mol氯气消耗氧化剂MnO2?的物质的量为1mol;反应②中每生成1mol氯气消耗氧化剂KMnO4的物质的量为0.4mol;反应③中中每生成1mol氯气消耗氧化剂KClO3的物质的量为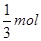 ;D正确;
;D正确;
本题难度:一般
5、计算题 (10分)(1)用氨、空气、水为原料制取硝酸铵,如果制取160 t硝酸铵至少需要多少吨氨?
(2)若用NH3制取NO转化率为96%,NO转化为硝酸的利用率为92%,问用于制取HNO3的氨占全部氨的物质的量分数是多少?
参考答案:(1)68 t
(2)53%
本题解析:工业上用氨制NH4NO3的过程是:将氨分成两部分,一部分用于合成HNO3,另一部分用于与生成的硝酸反应合成NH4NO3。如下图:
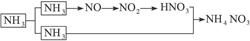
(1)NH4NO3中氮元素均来源于NH3,根据守恒原理可知,与HNO3反应的氨气量与用于合成硝酸的氨气量相等,所以有如下关系式:
NH4NO3?―? 2NH3?(即1 mol NH4NO3至少需2 mol NH3)
80? 34
160?x? 80∶160=34∶x
x="68" t
(2)由上面的分析可以看出,若每一步都100%转化,两部分氨应各占一半。但由于制HNO3的NH3未完全转化,总的转化率相当于96%×92%,所以NH3的用量肯定大于50%。设用于制HNO3的氨为1 mol
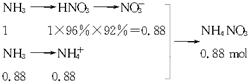
即:共用NH31.88 mol
用于制HNO3的NH3应占: ×100%=53%
×100%=53%
本题难度:简单