| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点讲解《物质的量》在线测试(2017年最新版)(二)
参考答案:A 本题解析:考查物质的量的有关计算。标准状况下,0.3mol的NH3是0.3mol×22.4L/mol=6.72L;4℃时,18克水的体积是18ml;2mol铝的质量是54g,其体积是54g÷2.7g/cm3;100g 37% (密度1.20g/cm3 )NaCl 溶液体积是100g÷1.20g/cm3,所以答案选A。 本题难度:一般 3、选择题 由CH4和O2组成的混合气体,标准状况下的密度为1g.L-1,则该混合气体中CH4和O2的体积比为 |
参考答案:D
本题解析:标准状况下的密度为1g.L-1,则混合气的平均相对分子质量是22.4,所以根据十字交叉法可知,混合气体中CH4和O2的体积比为(32-22.4)/(22.4-16)=3/2,答案选D。
本题难度:一般
4、计算题 (能力挑战题)某混合物是由氯化钠、氯化镁、氯化铝组成,已知钠、镁、铝三种元素的质量比为23∶16∶9,计算:
(1)氯化钠、氯化镁、氯化铝三种物质的物质的量之比为多少?
(2)当氯离子为1摩尔时,混合物的质量是多少?
参考答案:(1)3∶2∶1 (2)49.9 g
本题解析:(1)设氯化钠、氯化镁、氯化铝中钠、镁、铝三种元素的质量分别为23 g、16 g、9 g,则n(Na)= ="1" mol、n(Mg)=
="1" mol、n(Mg)= =
= mol、n (Al)=
mol、n (Al)=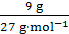 =
= mol,由氯化钠、氯化镁、氯化铝的化学式知:n(Na)=n(NaCl)=1 mol,n(Mg)=n(MgCl2)=
mol,由氯化钠、氯化镁、氯化铝的化学式知:n(Na)=n(NaCl)=1 mol,n(Mg)=n(MgCl2)= mol,n(Al)=n(AlCl3)=
mol,n(Al)=n(AlCl3)= mol,n(NaCl)∶n(MgCl2)∶n(AlCl3)=3∶2∶1。
mol,n(NaCl)∶n(MgCl2)∶n(AlCl3)=3∶2∶1。
(2)设氯化钠、氯化镁、氯化铝的物质的量分别是3n、2n、n,则3n+2×2n+3×n="1" mol,n=0.1 mol;
得n(NaCl)=0.3 mol,n(MgCl2)=0.2 mol,n(AlCl3)=0.1 mol;氯化钠、氯化镁、氯化铝的质量分别为m(NaCl)=0.3 mol×58.5 g・mol-1=17.55 g,
m(MgCl2)=0.2 mol×95 g・mol-1="19" g,
m(AlCl3)=0.1 mol×133.5 g・mol-1=13.35 g,
三物质的质量和为17.55 g+19 g+13.35 g =49.9 g。
考点:物质的量的计算。
本题难度:一般
5、选择题 下列各溶液中,c(Na+)最大的是
A.0.8 L 0.4 mol/L的NaOH溶液
B.0.2 L 0.15 mol/L的Na3?PO4
C.1 L 0.3 mol/L的NaCl溶液
D.0.1 L 0.5 mol/L的NaCl溶液
参考答案:D
本题解析:根据物质的化学式可知,四种溶液中钠离子浓度分别是(mol/L)0.4、0.45、0.3、0.5,所以正确的答案选D。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《同分异构体.. | |