微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 有4.8 g CuO、Fe2O3混合物跟足量CO充分反应后固体减少1.28 g,反应后全部气体用0.6 mol・L-1 Ba(OH)2溶液100 mL吸收。下列有关叙述中正确的是(?)
A.原混合物中CuO与Fe2O3物质的量的比为1∶2
B.原混合物中CuO与Fe2O3的质量比为2∶1
C.吸收CO2后溶液中一定有Ba(HCO3)2
D.反应中生成的CO2体积为1.792 L
参考答案:C
本题解析:设CuO、Fe2O3的物质的量分别为x、y

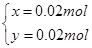 ,所以A、B均错;
,所以A、B均错;
n(CO2)=x+3y=0.08 mol,
由于 =
= =
= ,C项正确;D项未指明状况,错误。
,C项正确;D项未指明状况,错误。
本题难度:一般
2、选择题 中草药秦皮中含有的七叶树内酯结构是: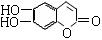 ,(C、H原子未画出,每个折点表示一个C原子)具有抗菌作用,若1 mol 七叶树内酯分别与浓Br2水和NaOH溶液完全反应,则消耗Br2和NaOH的物质的量分别是?(?)
,(C、H原子未画出,每个折点表示一个C原子)具有抗菌作用,若1 mol 七叶树内酯分别与浓Br2水和NaOH溶液完全反应,则消耗Br2和NaOH的物质的量分别是?(?)
A.3?,2? B.3?,4? C.2?,3? D.4?,4
参考答案:B
本题解析:略
本题难度:简单
3、填空题 (1)等物质的量的SO2与SO3二者的质量之比为______,所含氧原子数之比为______.
(2)在标准状况下,CO和CO2混合气体的质量为36g,体积为______,则其中CO2所占的体积为 11.2L,CO所占的质量为______.
参考答案:(1)设物质的量均为n,等物质的量的SO2与SO3二者的质量之比为n×64g/mol:n×80g/mol=4:5,氧原子个数之比等于物质的量之比,为n×2:n×3=2:3,
故答案为:4:5;2:3;
(2)标准状况下,CO和CO2混合气体的质量为36g,CO2所占的体积为 11.2L,其物质的量为11.2L22.4L/mol=0.5mol,
则设CO为xmol,所以x×28g/mol+0.5mol×44g/mol=36g,解得x=0.5mol,
即混合气体为0.5mol+0.5mol-1mol,标况下的体积为1mol×22.4L/mol=22.4L,
CO的质量为0.5mol×28g/mol=14g,
故答案为:2.24L;14g.
本题解析:
本题难度:一般
4、计算题 (7分)现有22g Mg、Al、Zn、Fe多种活泼金属粉末的混合物与200mL含有一定质量的20%硫酸溶液恰好完全反应,得到无水盐70g,求(要求写出计算过程)
(1)硫酸溶液的质量?
(2)生成的气体体积(标准状况)?
(3)硫酸物质的量浓度?
参考答案:(1)m(SO42-)=m(无水盐)-m(金属)=70-22=48g 1分
n(SO42-)=48/96=0.5mol=n(H2SO4)
m(H2SO4)=0.5×98=49g 1分
m(H2SO4溶液)=49/20%=245g 1分
(2)n(H2)=n(H2SO4)=0.5mol V(H2)=0.5×22.4=11.2L 2分
(3)c(H2SO4)=0.5/0.2=2.5mol・L-1 2分
本题解析:试题分析:金属与硫酸恰好反应生成硫酸盐与氢气,根据质量守恒可知m(SO42-)=80g-22g=48g,则n(H2SO4)=n(SO42-)=0.5mol,根据关系式H2SO4~H2↑计算氢气的体积;再根据c=n/v计算硫酸的物质的量浓度。
本题难度:一般
5、选择题 阿伏伽德罗常数约为6.02×1023mol-1,下列叙述中正确的是
A.将含有NO2和N2O4分子数共约6.02×1023个的混合气体温度降至标准状况时,其体积约为22.4L
B.在1 L 1 mol・L-1的氨水中,含有的NH3与NH3・H2O分子的总数小于6.02×1023个
C.标准状况下,等体积的HF、HCHO、CH3Cl 、SO3原子数之比为2:4:5:4
D.1 mol S和足量的铜粉反应,转移电子数目约为6.02×1023个
参考答案:
B
本题解析:略
本题难度:简单