微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 有关化学用语正确的是( )
A.Cl-的电子排布式:1s22s22p63s23p6
B.乙醇的结构简式:C2H6O
C.硫离子的结构示意图:
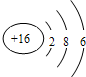
D.四氯化碳的电子式:
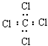
参考答案:A
本题解析:
本题难度:简单
2、选择题 下列说法正确的是( )
A.凡是金属元素跟非金属元素化合都形成离子化合物
B.离子化合物中的阳离子都是金属离子
C.离子化合物中,一个阴离子可同时与多个阳离子之间有静电作用
D.溶于水可以导电的化合物一定是离子化合物
参考答案:C
本题解析:
本题难度:简单
3、选择题 已知Zn2+的4s轨道和4p轨道可以形成sp3型杂化轨道,那么[ZnCl4]2―的空间构型为(? )
A.直线型
B.平面正方形
C.正四面体型
D.正八面体型
参考答案:C
本题解析:此配离子的中心原子采取sp3杂化,配位数为4,故空间构型为正四面体型。故选C。
点评:本题考查了离子空间构型的判断,难度较大,根据中心原子的杂化方式结合配位数判断即可。
本题难度:简单
4、选择题 某元素X的气态氢化物的化学式为H2X,则X的最高氧化物的水化物的化学式为
[? ]
A、H2XO3
B、HXO3
C、H3XO4
D、H2XO4
参考答案:D
本题解析:
本题难度:简单
5、填空题 一般认为:如果两个成键元素间的电负性差值大于1.7,它们之间通常形成离子键;如果两个成键元素间的电 负性差值小于1.7,它们之间通常形成共价键。请查阅下列化合物中元素的电负性数值,判断它们是离子化合物还是共价化合物。

①NaCl ②AlCl3 ③NO ④MgO ⑤BeCl2 ⑥CO2
共价化合物________;离子化合物_________。
参考答案:②③⑤⑥;①④
本题解析:
本题难度:一般