微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 下列三种化合物A、B、C中所含有的元素不多于三种,且分子内所含X、Y元素的质量分数及化合物的部分性质列于下表:
| 化合物 | A | B | C
w(X)
0.077?9
0.237?6
0.75
w(Y)
0.922?1
0.703
0
常压下T℃时的密度(g/cm3)
1.594?7(20℃)
2.254?5×10-3(0℃)
0.668×10-3(20℃)
沸点/℃
76.8
-23.7
-161.49
熔点/℃
-22.95
-97
-182.48
|
原子质量均大于10,且Y的相对原子质量比X的相对原子质量的两倍还要大.根据上述有关信息回答下列问题:
(1)化合物B的相对分子质量为______.
(2)确定化合物C的推理过程为:______.
(3)A与B的化学式为A______,B______.
参考答案:(1)分析表格数据可以发现B、C常温下均为气态,已知B标准状况下的密度,根据M=22.4L/mol×2.254?5×10-3?g/cm3×103=50.5g/mol,即得其相对分子质量为50.5,B中肯定含有另外一种元素,该元素在B中占有总质量为50.5×(1-0.703-0.237?6)=3,原子量小于3的只有氢,说明B中含有H.
故答案为:50.5;
(2)C中Y含量为0,X含量为75%,即C中一定含有H,且含量为25%.设C的分子式为XHn,根据nMr(X)+n=25%,Mr(X)=3n,讨论n=1、2、3、4,
n=1时,Mr(X)=3<10,不符合题意;
n=2时,Mr(X)=6<10,不符合题意;
n=3时,Mr(X)=9<10,不符合题意;
n=4时,Mr(X)=12>10,符合题意,
可得只有n=4合理.X相对原子质量为12,则X为碳,C的分子式为CH4.
故答案为:C中Y含量为0,X含量为75%,即C中一定含有H,且含量为25%.设C的分子式为XHn,根据nMr(X)+n=25%,Mr(X)=3n,讨论n=1、2、3、4,
n=1时,Mr(X)=3<10,不符合题意;
n=2时,Mr(X)=6<10,不符合题意;
n=3时,Mr(X)=9<10,不符合题意;
n=4时,Mr(X)=12>10,符合题意,
可得只有n=4合理.X相对原子质量为12,则X为碳,C的分子式为CH4.
(3)已知B标准状况下的密度,根据M=22.4L/mol×2.254?5×10-3?g/cm3×103=50.5g/mol,即得其相对分子质量;B中肯定含有另外一种元素,该元素在B中占有总质量为50.5×(1-0.703-0.237?6)=3,原子量小于3的只有氢,说明B中含有H,根据B中H总质量为3,说明B中含有3个氢原子,B的分子式设为CaH3Yb,则12a+3+bMr(Y)=50.5,由于B中X含量为0.2376,故a=1,则bMr(Y)=35.5,只有b=1合理,Y的相对原子质量为35.5,即氯元素.所以B的分子式为CH3Cl,
A中只有C、Cl两种元素,分子式应为CCl4,
故答案为:CCl4;CH3Cl.
本题解析:
本题难度:一般
2、实验题 铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与H2SO4反应)。某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究。
Ⅰ.铁矿石中含氧量的测定
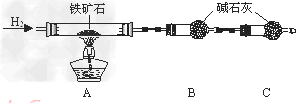
①?按上图组装仪器,检查装置的气密性;
②?将5.0g铁矿石放入硬质玻璃管中,装置B、C中的药品如图所示(夹持仪器均省略);
③?从左端导气管口处不断地缓缓通入H2,待C装置出口处H2验纯后,点燃A处酒精灯;
④?充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却。
(1)装置C的作用为_______________。
(2)测的反应后装置B增重1.35g,则铁矿石中氧的百分含量为______________。
(3)若将H2换成CO,则还需补充__________________装置。
Ⅱ.铁矿石中含铁量的测定 ?
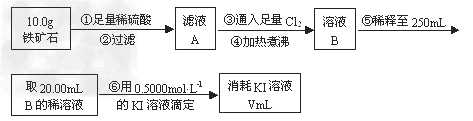
(1)步骤④中煮沸的作用是__________________。
(2)步骤⑤中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、______________。
(3)下列有关步骤⑥的操作中说法正确的是_________________。
?a.因为碘水为黄色,所以滴定过程中不需加指示剂
?b.滴定过程中可利用淀粉溶液作为指示剂
?c.滴定管用蒸馏水洗涤后可以直接装液
?d.锥形瓶不需要用待测夜润洗
?e.滴定过程中,眼睛注视滴定管中液面变化 ?
?f.滴定结束后,30s内溶液不恢复原来的颜色,再读数
(4)若滴定过程中消耗0.5000mol・L?1的KI溶液20.00mL,则铁矿石中铁的百分含量为______________。
Ⅲ.由Ⅰ、Ⅱ可以推算出该铁矿石中铁的氧化物的化学式为____________________。
参考答案:Ⅰ.(1)防止空气中的水蒸气和CO2进入B中,影响测定结果。
(2)24%?
(3)尾气处理?
Ⅱ.(1)赶走溶液中溶解的过量的Cl2?
(2)250mL容量瓶?
(3)df?
(4)70%?
Ⅲ.?Fe5O6
本题解析:
本题难度:困难
3、选择题 用下列实验装置能达到实验目的是( ? )
A.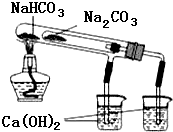
此图可比较NaHCO3和Na2CO3热稳定性大小
B.
此图可用铜和稀硝酸制取并收集少量NO
C.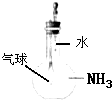
此图可验证氨气易溶于水
D.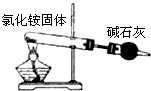
此图可用于实验室制取少量氨气
参考答案:C
本题解析:
本题难度:一般
4、简答题 某硝酸钾晶体中含有少量氯化钾,为了测定氯化钾的含量,称取一定量的样品溶解于水,逐滴加入0.1 mol/L的硝酸银溶液至沉淀完全后,过滤、洗涤、烘干、称重,然后计算样品中氯化钾的含量。回答以下问题:
(1)为什么要洗涤沉淀_______________?
(2)如何证明沉淀已经洗涤干净________________?
参考答案:(1)除去沉淀表面吸附的可溶性离子,减小测定结果的误差。
(2)取少量最后的洗涤液,滴入浓的盐酸中,如果产生白色浑浊,证明沉淀未洗涤干净;如果不出现白色浑浊,证明沉淀已洗涤干净。
本题解析:
本题难度:一般
5、选择题 下列装置所示的实验中,能达到实验目的是( )
A.

分离碘和酒精
B.

除去Cl2中的HCl
C.
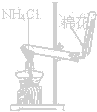
实验室制氨气
D.
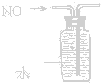
排水法收集NO
参考答案:D
本题解析:
本题难度:一般