微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 反应3A(g)+B(g)═2C(g)在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质表示为:①vA═1mol/L?min?②vC═0.5mol/L?min?③vB═0.5mol/L?min,三种情况下该反应速率大小的关系正确的是( )
A.③>①>②
B.③>②>①
C.①>②>③
D.②>①>③
参考答案:A
本题解析:
本题难度:简单
2、计算题 在一定温度下,10L密闭容器中加入5.0molSO2、4.5molO2,发生反应:2SO2 + O2  2SO3经10min后反应达平衡时O2的浓度为0.30mol/L。请计算(写出计算过程):
2SO3经10min后反应达平衡时O2的浓度为0.30mol/L。请计算(写出计算过程):
(1)10min内SO2的转化率;
(2)平衡常数K。
参考答案:(1)60%? (2)7.5L/mol
本题解析:10L密闭容器在10min内各物质浓度发生的变化如下:
2SO2?+? O2? ?2SO3
?2SO3
起始浓度(mol/L)0.50?0.45? 0
变化浓度(mol/L)0.30? 0.15? 0.30
平衡浓度(mol/L)0.20? 0.30? 0.30
则:(1)10min内SO2的转化率为:
(2)平衡常数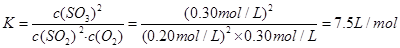
点评:对于化学平衡的相关计算,应利用“三段式法”,可以起到事半功倍的效果。另外应掌握化学平衡常数只与温度有关,温度不变,平衡常数的值不变。
本题难度:一般
3、选择题 如图是可逆反应N2(g)+3H2(g) 2NH3(g) 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是(?)
2NH3(g) 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是(?)
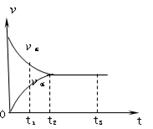
A.t1时,只有正方向反应
B.t2时,反应到达限度
C.t2-t3,反应不再发生
D.t2-t3,各物质的浓度相等且不再发生变化
参考答案:B
本题解析:A.可逆反应N2(g)+3H2(g)  2NH3(g)发生后,在任何时刻反应不仅向正反应方向进行,也向逆反应方向进行,在t1时,正方向方向的速率大于逆反应方向的速率。错误。B.任何可逆反应都是在一定的条件下进行的。在t2时,反应到达该反应条件下的限度。错误。C.在t2-t3时,反应处于该条件下平衡状态,产生反应仍然在进行,正反应速率与逆反应速率相等。错误。D.在 t2-t3内,反应处于该条件下的平衡状态,反应混合物中由于在单位时间内消耗的浓度与产生的浓度相等,因此各物质的浓度相等且不再发生变化。正确。
2NH3(g)发生后,在任何时刻反应不仅向正反应方向进行,也向逆反应方向进行,在t1时,正方向方向的速率大于逆反应方向的速率。错误。B.任何可逆反应都是在一定的条件下进行的。在t2时,反应到达该反应条件下的限度。错误。C.在t2-t3时,反应处于该条件下平衡状态,产生反应仍然在进行,正反应速率与逆反应速率相等。错误。D.在 t2-t3内,反应处于该条件下的平衡状态,反应混合物中由于在单位时间内消耗的浓度与产生的浓度相等,因此各物质的浓度相等且不再发生变化。正确。
本题难度:一般
4、选择题 NO2存在下列平衡:2NO2(g)  N2O4(g)+Q(Q>0) 在测定NO2的相对分子质量时,下列条件下测定结果最接近理论值的是
N2O4(g)+Q(Q>0) 在测定NO2的相对分子质量时,下列条件下测定结果最接近理论值的是
A.温度130℃、压强3.03×105 Pa
B.温度25℃、压强1.01×105 Pa
C.温度130℃、压强5.05×104 Pa
D.温度0℃、压强5.05×104 Pa
参考答案:C
本题解析: 测定NO2相对分子质量,应使平衡向逆反应方向移动,所以应选择高温、低压。
本题难度:一般
5、选择题 在一密闭容器中进行以下可逆反应:M(g) + N(g)  P(g) + 2L。在不同的条件下P的百分含量P%的变化情况如图,则反应
P(g) + 2L。在不同的条件下P的百分含量P%的变化情况如图,则反应
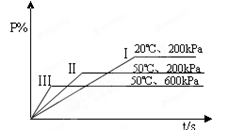
A.正反应放热,L是固体
B.正反应放热,L是气体
C.正反应吸热,L是气体
D.正反应放热,L是固体或气体
参考答案:B
本题解析:对比图像中Ⅰ、Ⅱ,同压强,不同温度,温度越高,P的百分含量P%越低,所以正反应放热;对比Ⅱ、Ⅲ同温度,不同压强,压强越大,P的百分含量P%越低,L是气体。所以答案B正确。
本题难度:一般