��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1�������� ��6�֣���100mLˮ��Ͷ������غͽ�������15g����ַ�Ӧ������ʣ�����1.8g����Ӧ�й��ų��������ٺ�����(��״��)
�ο��𰸣�8960ml
���������
2K?+ 2H2O = 2KOH + H2��
2KOH +2Al+ 6H2O = 2K[Al(OH)4] + 3H2��
��������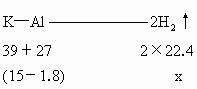
����x��8.96 V��8960ml
�����Ѷȣ���
2��ѡ���� ������ӡˢ��·��Ĺ����г�����FeCl3��Һ��Cu��Ӧ���䷴Ӧ����ʽΪ��2FeCl3+Cu�T2FeCl2+CuCl2������FeCl3��Һ�м���a?g?Cu�ۣ���ȫ�ܽ���ټ���b?g?Fe�ۣ���ַ�Ӧ������c?g������壮��c��a��������˵����ȷ���ǣ�������
A���������ȫ����Cu
B������������ΪFe��Cu�Ļ����
C�����õ�����Һ���ܺ���Fe3+
D�����������Fe����Һ��һ������Cu2+
�ο��𰸣�A
���������
�����Ѷȣ�һ��
3��ѡ���� ijͬѧ���������������Ũ����Ȥ���������Ϻ��Ƴ����¿�Ƭ:
�ڿ����а���������5000C���γ�Fe3O4���¶������ߣ����γ�Fe2O3���ڸ��ߵ��¶��¼���Fe2O3��Լ14000C��ʱ����ʧȥ�����ֵõ�Fe3O4������
|
����˵����ȷ���ǣ�?��?
A��FeO��Fe2O3��Fe3O4��Ϊ��ɫ����? B����Ӧ�ڢ۾�Ϊ������ԭ��Ӧ
C�����ȶ���˳��Ϊ��FeO>Fe2O3>Fe3O4
D����������������Ԫ�صĻ��ϼ۸��ӣ���д�����������ʽ����ѧʽ��дΪFeO��Fe2O3����������������Ϊһ���Σ����仯ѧʽ��дΪFe2(FeO2) 2
�ο��𰸣�B
���������A ����Fe2O3�Ǻ���ɫ����
B ��ȷ����Ӧ�ڢ���Ԫ�ض��л��ϼ۵ı仯�����ԣ�����������ԭ��Ӧ��
C �������ȶ���˳��Ϊ��FeO>Fe3O4>Fe2O3
D ������������������Ԫ�صĻ��ϼ۸��ӣ���������������Ϊһ���Σ����仯ѧʽ��дΪFe(FeO2) 2
�����Ѷȣ�һ��
4������� ��15�֣��ۺ��������ֳƾ�������ѧʽΪ ���㷺������ˮ������ʵ�����������᳧��������Ҫ�ɷ�Ϊ���������P����FeS��SiO2�ȣ��Ʊ��������̷���FeSO4��7H2O ���������£�
���㷺������ˮ������ʵ�����������᳧��������Ҫ�ɷ�Ϊ���������P����FeS��SiO2�ȣ��Ʊ��������̷���FeSO4��7H2O ���������£�
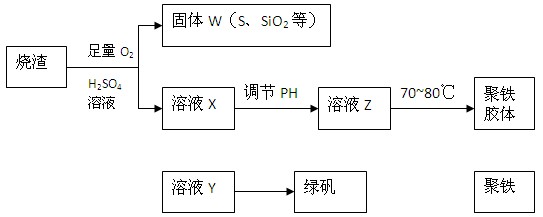
��1����֤����W���պ���������庬��SO2�ķ�����___��
��2���Ʊ��̷�ʱ������ҺX�м������___����ַ�Ӧ��_____�����õ���ҺY���پ�Ũ�����ᾧ�Ȳ���õ��̷���
��3����ҺZ��pHӰ�����������������������pH��ֽ�ⶨ��ҺpH�IJ�������Ϊ____������ҺZ��pHƫС�������¾�����������������ƫ_____��
��4���Ŵ����̷����տ����̷��ͣ�Ҳ����ˮ�������ᣩ�ͺ�ɫ���ϣ�Fe2O3������д���йصĻ�ѧ����ʽ��
??��
��5���̷����������·���������ɫ���ϣ�Fe2O3��,�������������ǣ���5560kg�̷���Ħ������Ϊ278 g/mol������ˮ�У�������������������Һǡ����ȫ��Ӧ�����������������裬�������ɫ���壻������ɫ�����м���16680 kg �̷���560 kg���ۣ����������������裬��Ӧ��ɺ��д���Fe2O3�����ڽ����������Գ�����ʽ���������˺������������յú�ɫ���ϡ���������Һ������ֻ�������ƺ����������������Ͽ�������ɫ����____________________kg��
�ο��𰸣���1��������ͨ��Ʒ����Һ�У���Ʒ����ɫ�����Ⱥ��ֱ�죬ע���ж�������
��2������?����
��3������ֽ�ŵ���������,�ò�����պȡ��Һ,�㵽��ֽ������,Ȼ�������ɫ���Ա�?��
��4��2FeSO4��7H2O Fe2O3��SO2����SO3����14H2O��SO3��H2O=H2SO4
Fe2O3��SO2����SO3����14H2O��SO3��H2O=H2SO4
��5��4000
�����������1�������������Ư���Կ���ʹƷ����Һ��ɫ������Ư�ײ��Ǻ��ȶ������Ⱥ��ֿɻָ�ԭ����ɫ��
��2����ҺX�к���Fe3��,�����ȥ,���ֲ��������µ�����,��ѡ������,����������ͨ�����˳�ȥ.
(3)������Һ��pHֵ��һ����������ʪpH��ֽ��Ҳ���ܲ��뵽��Һ�У���ȷ�ķ����ǽ���ֽ�ŵ���������,�ò�����պȡ��Һ,�㵽��ֽ������,Ȼ�������ɫ���Աȡ�����ҺZ��pHƫС��˵�����Խ�ǿ�����ǵľ�����������ƫ�٣������ƫ�࣬���������������ƫ�͡�
��4����������ɵø÷�Ӧ����������ԭ��Ӧ���ж����������ɣ�����ʽΪ
2FeSO4��7H2O Fe2O3��SO2����SO3����14H2O��SO3��H2O=H2SO4��
Fe2O3��SO2����SO3����14H2O��SO3��H2O=H2SO4��
��5�����ݷ���ʽ�ɼ�����Ҫ�������Ƶ����ʵ�����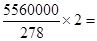 40000mol����ԭ���غ�֪�����Ƶ����ʵ�����20000mol�������������ɵ��������е�SO42��������������̷�����������̷���
40000mol����ԭ���غ�֪�����Ƶ����ʵ�����20000mol�������������ɵ��������е�SO42��������������̷�����������̷���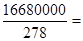 60000mol������������20000mol���ܵ���ԭ����
60000mol������������20000mol���ܵ���ԭ����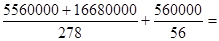 90000mol������ԭ���غ�֪Fe2O3������
90000mol������ԭ���غ�֪Fe2O3������
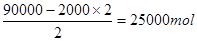 ��������4000kg��
��������4000kg��
�����Ѷȣ���
5��ʵ���� (6��)��ͼ����ʾװ�ã������ֲ�ͬ�����ֱ����ʵ�飮�ش��й����⣺
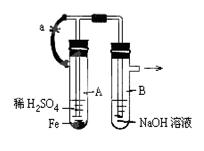
(1)��ͼʾ���Ӻ�װ�ã���ֹˮ��a����B�пɹ۲쵽��������?��
A�з�����Ӧ�Ļ�ѧ����ʽ��?��
(2)��ӦƬ�̺н�ֹˮ��a����ʱ�ɹ۲쵽�������У�__?__��B�з�����Ӧ�����ӷ���ʽ�ǣ�?��
�ο��𰸣�����1������ɫ���ݲ�����Fe+H2SO4= FeSO4+H2����
��2��A�е���Һ����B���а�ɫ����������Fe2++2OH-= Fe(OH)2��
�����������1��A�з�����ӦFe+H2SO4= FeSO4+H2������ֹˮ��a��H2����B�У���B�пɿ�������ɫ���ݲ�����
��2���н�ֹˮ��a��A������ѹǿ����FeSO4ѹ��B�����������Ʒ�Ӧ����ɿ���B���а�ɫ�������������ӷ���ʽ��Fe2++2OH-= Fe(OH)2��
������������������������Ʊ�������
�����Ѷȣ�һ��