微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
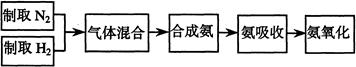
1、实验题 (16分)实验室模拟合成氨和氨催化氧化的流程如下:
(1)已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气,该反应中只有氮元素发生变价,写出该反应的化学方程式?。从下图中选择制取氮气的合适装置?。

(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有?。
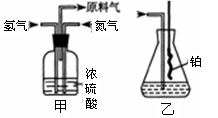
(3)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是:?,锥形瓶中还可观察到的现象是:?。
(4)反应结束后锥形瓶内的溶液中含有H+、OH-、?离子。
参考答案:(1)NaNO2 + NH4Cl NaCl + N2↑+2H2O? a
NaCl + N2↑+2H2O? a
(2)干燥气体控制氢气和氮气的流速(3)说明氨的氧化反应是一个放热反应;有红棕色气体产生
(4)NH4+、NO3-
本题解析:(1)已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气, 该反应的化学方程式为:NaNO2 + NH4Cl NaCl + N2↑+2H2O。该反应为液+液
NaCl + N2↑+2H2O。该反应为液+液 气体。所以应该选择a装置。(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有控制氢气和氮气的流速,以调节二者的混合比例及对气体进行干燥处理。(3)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是氨的氧化反应是一个放热反应。氨氧化的方程式为4NH3+5O2
气体。所以应该选择a装置。(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有控制氢气和氮气的流速,以调节二者的混合比例及对气体进行干燥处理。(3)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是氨的氧化反应是一个放热反应。氨氧化的方程式为4NH3+5O2 4NO+6H2O;产生的NO在锥形瓶上方遇空气发生反应:2NO+ O2= 2NO2产生红棕色的NO2气体。因此锥形瓶中还可观察到的现象是有红棕色气体产生。(4)产生的NO2在水中溶解发生反应3NO2+ H2O == 2HNO3+ NO得到硝酸,硝酸与氨气发生反应得到NH4NO3.因此反应结束后锥形瓶内的溶液中含有H+、OH-、NH4+、NO3-。
4NO+6H2O;产生的NO在锥形瓶上方遇空气发生反应:2NO+ O2= 2NO2产生红棕色的NO2气体。因此锥形瓶中还可观察到的现象是有红棕色气体产生。(4)产生的NO2在水中溶解发生反应3NO2+ H2O == 2HNO3+ NO得到硝酸,硝酸与氨气发生反应得到NH4NO3.因此反应结束后锥形瓶内的溶液中含有H+、OH-、NH4+、NO3-。
本题难度:一般
2、选择题 下列气体中,不能用排空气收集的是
A.NO
B.NO2
C.CO2
D.H2
参考答案:A
本题解析:NO极易被氧气氧化生成NO2,所以不能用排气法收集,而是用排水法收集。其余都可以用排气法收集,所以答案是A。
本题难度:一般
3、选择题 除去Cl2中混有的少量HCl气体,可将气体通入
A.苛性钠溶液
B.饱和NaHCO3溶液
C.澄清石灰水
D.饱和氯化钠溶液
参考答案:D
本题解析:A中的氢氧化钠、B中的碳酸氢钠、C中的澄清石灰水均能和氯气反应,随意不能用来除去氯气中的氯化氢气体。氯化氢极易溶于水,所以可用于饱和食盐水来除去氯气中的氯化氢气体,答案选D。
点评:在解答物质分离提纯试题时,选择试剂和实验操作方法应遵循三个原则: 1.不能引入新的杂质(水除外),即分离提纯后的物质应是纯净物(或纯净的溶液),不能有其他物质混入其中;2.分离提纯后的物质状态不变;3.实验过程和操作方法简单易行,即选择分离提纯方法应遵循先物理后化学,先简单后复杂的原则。
本题难度:简单
4、实验题 (10分)某化学兴趣小组利用浓盐酸、二氧化锰共热制氯气,并用氯气和消石灰制取少量漂白粉。现已知反应:2Cl2+2Ca(OH)2 = Ca(ClO)2+CaCl2+2H2O,该反应是放热反应,温度稍高即发生副反应。试回答以下问题:
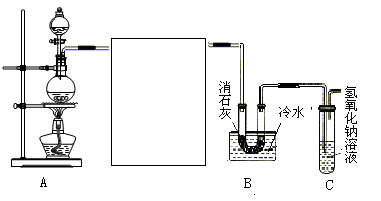
(1)制取氯气时在烧瓶中加入一定量的二氧化锰,通过?(填仪器名称)向烧瓶中加入适量的浓盐酸,写出该反应的离子方程式?。
(2)为使实验成功,A和B间需要加适当的装置,请将它画在框内(示意图),并注明其中盛放的药品。如果A产生的气体直接进入B中,实验产生的不良后果是?。
(3)实验室若用16 mol ?L-1的盐酸100 mL与足量的二氧化锰反应,理论上最终生成的Ca(ClO)2的物质的量最多不超过?mol。
参考答案:(每空2)(1)分液漏斗,MnO2 + 4H+ + 2Cl-(浓) Mn2+ + Cl2↑+ 2H2O
Mn2+ + Cl2↑+ 2H2O
(2)
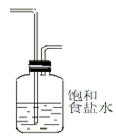
HCl会与Ca(OH)2和Ca(ClO) 2反应,影响产品质量。
(3)0.2 mol
本题解析:(1)根据装置图可知,盛放浓盐酸的仪器是分液漏斗。浓盐酸和二氧化锰反应的方程式为MnO2 + 4H+ + 2Cl-(浓) Mn2+ + Cl2↑+ 2H2O。
Mn2+ + Cl2↑+ 2H2O。
(2)由于浓盐酸具有挥发性,所以生成的氯气中混有氯化氢,而氯化氢能与Ca(OH)2和Ca(ClO) 2反应,影响产品质量,所以需要利用饱和食盐水除去氯气的氯化氢。
(3)16 mol ?L-1的盐酸100 mL的物质的量是1.6mol,所以根据方程式可知,生成氯气是0.4mol。氯气和氢氧化钙反应的方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,所以理论上可以生成次氯酸钙0.2mol。
本题难度:一般
5、实验题 下图所示为常见气体制备、分离、干燥和性质验证的部分仪器装置(加热设备及夹持固定装置均略去),请根据要求完成下列各题(仪器装置可任意选用,必要时可重复选择,a、b为活塞)。

(1)若气体入口通入CO和CO2的混合气体,E内放置CuO,选择装置获得纯净干燥的CO,并验证其还原性及氧化产物,所选装置的连接顺序为___________ (填代号)。能验证CO氧化产物的现象是___________________________________。
(2)停止CO和CO2混合气体的通入,E内放置Na2O2,按A→E→D→B→H装置顺序制取纯净干燥的O2,并用O2氧化乙醇。此时,活塞a应________,活塞b应_________,需要加热的仪器装置有___________(填代号),m中反应的化学方程式为______________________________。
(3)若气体入口改通空气,分液漏斗内改加浓氨水,圆底烧瓶内改加NaOH固体,E内放置铂铑合金网,按A→G→E→D装置顺序制取干燥氨气,并验证氨的某些性质。
①装置A中能产生氨气的原因有:____________________________。
②实验中观察到E内有红棕色气体出现,证明氨气具有___________性。
参考答案:(1)ACBECF;AB之间的C装置中溶液保持澄清,EF之间的C装置中溶液变浑浊
(2)关闭;打开;k、m;2CH3CH2OH+O2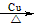 2CH3CHO+2H2O
2CH3CHO+2H2O
(3)①氢氧化钠溶于水放出大量热,温度升高,使氨的溶解度减小而放出,氢氧化钠吸水,促使氨放出,
氢氧化钠电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出;
②还原。
本题解析:
本题难度:困难