微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 反应A(g)+B(g)?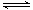 ?C(g)+D(g)过程中的能量变化如图所示,由此可判断(?)
?C(g)+D(g)过程中的能量变化如图所示,由此可判断(?)
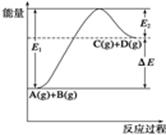
A.1molA与1molB充分反应后,能量变化为ΔE
B.加入催化剂后,反应加快,ΔE减小
C.反应物的总键能小于生成物的总键能
D.反应达到平衡时,升高温度,A的转化率增大
参考答案:D
本题解析:A、1molA(g)与1molB(g)充分反应后生成1mol?C(g)与1molD(g),能量变化为ΔE,错误;B、加入催化剂后,反应加快,E1、E2减小,ΔE不变,错误;C、由题给图像知,反应物的总键能大于生成物的总键能,错误;D、由题给图像知,该反应为吸热反应,反应达到平衡时,升高温度,平衡正向移动,A的转化率增大,正确。
本题难度:一般
2、选择题 可逆反应N2+3H2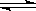 2NH3 △H<0。有甲、乙两个完全相同的容器,向甲容器中加入1molN2和3 molH2,在一定条件下,达平衡时放出的热量为Q1;在相同条件下,向乙容器加入2 molNH3,达平衡时,吸收的热量为Q2。已知Q2=3Q1,则甲容器中,H2的转化率为
2NH3 △H<0。有甲、乙两个完全相同的容器,向甲容器中加入1molN2和3 molH2,在一定条件下,达平衡时放出的热量为Q1;在相同条件下,向乙容器加入2 molNH3,达平衡时,吸收的热量为Q2。已知Q2=3Q1,则甲容器中,H2的转化率为
A.10%
B.20%
C.25%
D.40%
参考答案:C
本题解析:根据题意甲、乙两个容器中的平衡状态是等效的,设甲中氢气的转化率是x,则生成氨气的物质的量是2x,所以再乙容器中分解的氨气是2-2x,则根据Q2=3Q1可知(1-x)・△H=3x・△H,解得x=0.25,答案选C。
点评:该题是高考中的常见题型,属于中等难度的试题。试题设计新颖,综合性强,侧重对学生解题能力的培养和训练,有利于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确两种状态下平衡是等效的,然后根据题意再列式计算即可。
本题难度:简单
3、选择题 下列叙述正确的是(?)
A.生成物总能量一定低于反应物总能量
B.分解反应一定是吸热反应
C.应用盖斯定律,可计算某些难以直接测量的反应的焓变
D.同温同压下,H2(g)+Cl2(g)
参考答案:C
本题解析:A 错误,如果是放热反应,生成物总能量一定低于反应物总能量
B 错误,有的分解反应是放热反应。
C 正确,设计途径,可计算某些难以直接测量的反应的焓变
D 错误,H2(g)+Cl2(g)?2HCl(g)的起态和终态相同,△H就相同,与反应条件无关。
本题难度:一般
4、选择题 下列图象分别表示有关反应的反应过程与能量变化的关系据此判断下列说法中正确的是

[? ]
A.石墨转变为金刚石是吸热反应
B.白磷比红磷稳定
C.S(g)+O2(g)=SO2(g) ΔH1, S(s)+O2(g)=SO2(g) ΔH2,则ΔH1>ΔH2
D.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH>0
参考答案:A
本题解析:
本题难度:简单
5、填空题 (1)氯元素的最高价氧化物为无色液体,0.25 mol 该物质与一定量水混合得到一种稀溶液,并放出Q kJ 的热量。写出该反应的热化学方程式:?。
(2)已知:Fe2O3(s) + 3/2C(s) = 3/2CO2(g) + 2 Fe(s) ΔH =234.1 kJ・mol-1
C(s) + O2(g) = CO2(g)?ΔH = ―393.5 kJ・mol-1
则2 Fe(s)+ 3/2O2(g) = Fe2O3(s) 的ΔH是??kJ・mol-1。
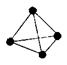
(3)意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如下图所示。已知断裂1moIN-N吸收167kJ热量,生成1molN≡N放出942kJ。根据以上信息和数据,写出N4气体转变为N2的热化学方程式:?。
(4)下图是丙烷(C3H8)、二甲醚(CH3OCH3)燃烧过程中能量变化图,其中x为各自反应中对应的系数。根据该图写出二甲醚燃烧的热化学方程式:?。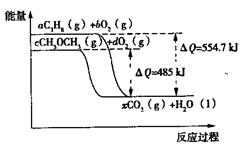
参考答案:(每空3分,共12分)
(1)Cl2O7(l)+H2O(l)==2HClO4(aq);ΔH=-4QkJ/mol
(2)-824.4
(3)N4(g)= N2(g)?ΔH=-882kJ/mol
(4)CH3OCH3(g)+3O2(g)→2CO2(g)+3H2O(l)? △H=-1455kJ・mol- 1
本题解析:(1)氯元素的最高价氧化物是Cl2O7,0.25molCl2O7与一定量水混合得到HClO4溶液时,放出QkJ的热量,则1molCl2O7与一定量水混合得到HClO4溶液时,放出4QkJ的热量,所以热化学方程式为:
Cl2O7(1)+H2O(1)=2HClO4(aq);△H=-4QkJ?mol-1。
(2)已知:(1)Fe2O2(s)+3/2C(s)=3/2CO2(g)+2Fe(s)△H=234.1kJ?mol-1
(2)C(s)+O2(g)=CO2(g)△H=-393.5kJ?mol-1
由盖斯定律(2)×(3/2)-(1),得:2Fe(s)+3/2O2(g)=Fe2O3(s)△H=(-393.5kJ?mol-1)×(3/2)-234.1kJ?mol-1
即2Fe(s)+3/2O2(g)=Fe2O3(s)△H=-824.35kJ?mol-1。
(3)1molN4气体中含有6molN-N键,可生成2molN2,形成2molN≡N键,则1molN4气体转变为N2化学键断裂断裂吸收的热量为6×167KJ=1002KJ,形成化学键放出的热量为1884KJ,所以反应放热,放出的热量为1884KJ-1002KJ=882KJ,故N4气体转变为N2的热化学方程式是N4(g)= N2(g)?ΔH=-882kJ/mol。
(4)由图象可知生成1mol水时,二甲醚燃烧放出485KJ的热量,则生成3mol水,放出的热量为3×485KJ=1455KJ,
所以热化学方程式为CH3OCH3(g)+3O2(g) 2CO2(g)+3H2O(l)△H=-1455kJ?mol-1。
2CO2(g)+3H2O(l)△H=-1455kJ?mol-1。
点评:本题考查盖斯定律的利用、反应热的计算和热化学方程式的书写,难度大,明确已知反应与目标热化学方程式的关系是关键,注意基础知识的掌握与理解。
本题难度:一般