微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 同素异形体相互转化的反应热相当小而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的“不管化学过程是一步完成还是分几步完成,这个总过程的热效应是相同的”观点来计算反应热。已知:
P4(s,白磷)+5O2(g)====P4O10(s)
ΔH="-2" 983.2 kJ・mol-1①
P(s,红磷)+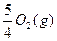 ====
====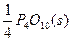 ?
?
ΔH="-738.5" kJ・mol-1②
则白磷转化为红磷的热化学方程式为_________。相同状况下,能量状态较低的是_________;白磷的稳定性比红磷_________(填“高”或“低”)。
参考答案:P4(s,白磷)====4P(s,红磷)
ΔH="-29.2" kJ・mol-1?红磷?低
本题解析:①-4×②得P4(s,白磷)=4P(s,红磷)? ΔH=ΔH1-4ΔH2="-2" 983.2 kJ・mol-1-4×(-738.5 kJ・mol-1)="-29.2" kJ・mol-1,即P4(s,白磷)====4P(s,红磷)? ΔH="-29.2" kJ・mol-1。白磷转化为红磷是放热反应,稳定性比红磷低(能量越低越稳定)。
本题难度:简单
2、选择题 根据相关化学概念和原理,下列判断正确的是?(?)
A.若某反应的生成物总能量低于反应物总能量,则该反应为吸热反应
B.若A2+2D-=2A-+D2,则氧化性:D2>A2
C.若R2-和M+的电子层结构相同,则原子序数:R>M
D.若甲、乙两种有机物具有相同的分子式,不同的结构,则甲和乙一定是同分异构体
参考答案:D
本题解析:略
本题难度:简单
3、选择题 各种能量可以相互转化。下述能量未必由化学能转化而来的是(?)
A.电解铝所需的电能
B.人的体能
C.化学电池的电能
D.燃油汽车的动能
参考答案:A
本题解析:电能不一定全部来自于化学能,例如水力发电,太阳能发电等,A正确,答案选A.
本题难度:简单
4、选择题 下图为某反应的焓变示意图,下列有关该反应的说法中正确的是
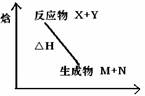
A.△H>0
B.X能量一定高于M
C.该反应一定不必加热就可以发生
D.该反应为放热反应
参考答案:D
本题解析:根据图像可知,反应物的总能量高于生成物的总能量,所以反应是放热反应,△H小于0,选项A、B不正确,D正确;反应条件与反应是放热反应或吸热反应无关系,选项C不正确,因此正确的答案选D。
本题难度:一般
5、选择题 工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g) Si(s)+4HCl(g)ΔH=+Q kJ・mol-1(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是( )。
Si(s)+4HCl(g)ΔH=+Q kJ・mol-1(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是( )。
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol,则达到平衡时,吸收热量为Q kJ
C.反应至4 min时,若HCl浓度为0.12 mol・L-1,则H2的反应速率为0.03 mol・(L・min-1)
D.当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol・L-1的NaOH溶液中恰好反应
参考答案:D
本题解析:因反应是气体体积增大的反应,所以加压会减小SiCl4的转化率,A错;因反应为可逆反应,SiCl4不可能反应1 mol,故达平衡时吸收热量应小于Q kJ,B错;列式计算v(HCl)=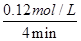 =0.03 mol・(L・min)-1,v(H2)=
=0.03 mol・(L・min)-1,v(H2)=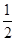 v(HCl)=0.015 mol・L-1・min-1,C错误;据热化学方程式比例关系计算,吸收0.025Q kJ能量,则有0.1 mol HCl生成,可中和0.1 mol NaOH,D正确。
v(HCl)=0.015 mol・L-1・min-1,C错误;据热化学方程式比例关系计算,吸收0.025Q kJ能量,则有0.1 mol HCl生成,可中和0.1 mol NaOH,D正确。
本题难度:一般