��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����������Ȼ�߷��ӻ��������
A.�Ҵ�
B.����ϩ
C.������
D.������
�ο��𰸣�D
���������
�����Ѷȣ�һ��
2��ѡ���� ij������FeCl3��Һ��ʴ����ͭ�ľ�Ե������ӡˢ��·������С��Ϊȷ��������ķ�Һ����ɣ���������ʵ�飺��1��ȡ20mL��Һ����������AgNO3��Һ�����ɳ���?17.22g����2����ȡ20mL��Һ����ͭƬ��ַ�Ӧ��ͭƬ����������0.32g�����й���ԭ��Һ��ɵ��жϴ������
A.һ������Fe2+��Fe3+��Cu2+��Cl-
B.c��Fe2+����c��Fe3+��=5��2
C.c��Fe2+����c��Cu2+��=2��1
D.c��Cl-��=6.0?mol?L-1��c��Fe2+��=1.5mol?L-1
�ο��𰸣�B
�����������������Һ����������AgNO3��Һ�����ɳ���17.22g������ΪAgCl������n= ����AgCl�����ʵ�����������Ԫ���غ������Һ��n��Cl�������ٸ���c=
����AgCl�����ʵ�����������Ԫ���غ������Һ��n��Cl�������ٸ���c= ����ԭ��Һ��c��Cl������
����ԭ��Һ��c��Cl������
��Һ����ͭƬ��ַ�Ӧ��ͭƬ����������0.32g��˵����Һ�к���Fe3+������ͭƬ���ٵ�������Ϸ���ʽ������Һ��Fe3+�����ʵ�������������ԭ��Һ��c��Fe?3+����
�ɷ���ʽ2FeCl3+Cu�T2FeCl2+CuCl2��֪��ԭ��Һ��c��Fe2+��=2c��Cu2+�������ݵ���غ㣬ԭ��Һ��3c��Fe?3+��+2c��Fe2+��+2c��Cu2+��=c��Cl�������ݴ˼���ԭ��Һ��c��Fe2+����c��Cu2+����
���A����Һ����ͭƬ��ַ�Ӧ��ͭƬ����������0.3g��˵����Һ�к���Fe3+����Ϸ�Ӧ2FeCl3+Cu�T2FeCl2+CuCl2��֪��ԭ��Һһ������Fe2+��Fe3+��Cu2+��Cl������A��ȷ��
B����Һ����������AgNO3��Һ�����ɳ���?17.22g������ΪAgCl����n��AgCl��= =0.12mol��ԭ��Һ��c��Cl����=
=0.12mol��ԭ��Һ��c��Cl����=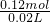 =6mol/L��
=6mol/L��
��Һ����ͭƬ��ַ�Ӧ��ͭƬ����������0.32g�����ʵ���Ϊ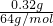 =0.005mol����20mL��Һ��Fe3+Ϊnmol����
=0.005mol����20mL��Һ��Fe3+Ϊnmol����
2FeCl3+Cu�T2FeCl2+CuCl2
2? 1
nmol?0.005mol
��n=0.010mol������ԭ��Һ��c��Fe?3+��= =0.5mol/L��
=0.5mol/L��
�ɷ���ʽ2FeCl3+Cu�T2FeCl2+CuCl2��֪��ԭ��Һ��c��Fe2+��=2c��Cu2+�������ݵ���غ㣬ԭ��Һ��3c��Fe?3+��+2c��Fe2+��+2c��Cu2+��=c��Cl������ԭ��Һ��c��Cl����=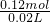 =6mol/L����3��0.5+2c��Fe2+��+c��Fe2+��=6�����c��Fe2+��=1.5mol/L����ԭ��Һ��c��Fe2+����c��Fe?3+��=1.5mol/L��0.5mol/L=3��1����B����
=6mol/L����3��0.5+2c��Fe2+��+c��Fe2+��=6�����c��Fe2+��=1.5mol/L����ԭ��Һ��c��Fe2+����c��Fe?3+��=1.5mol/L��0.5mol/L=3��1����B����
C���ɷ���ʽ2FeCl3+Cu�T2FeCl2+CuCl2��֪��ԭ��Һ��c��Fe2+��=2c��Cu2+������C��ȷ��
D����B�з�����֪��c��Cl����=6mol/L��c��Fe2+��=1.5mol/L����D��ȷ��
��ѡB��
���������⿼����ݷ���ʽ�ļ��㡢�����Һ���йؼ���ȣ��Ѷ��еȣ�ע�����غ�����ã�
�����Ѷȣ���
3��ѡ���� ��Na��Na2O��Na2O2��ɵĹ���������и���ֵ����ʵ���֮��Ϊ0.1 mol����������ˮ��������Һǡ���ܱ�150 mLŨ��Ϊ1 mol/L��HCl��Һ�кͣ������������˵������ȷ����
A.�к����ɵ�NaClΪ0.15 mol
B.0.1 mol����������ˮ��Ӧ����H2��O2������ȿ�����1��1
C.Na��Na2O��Na2O2���ʵ���֮�ȿ�����2��1��1
D.Na��Na2O��Na2O2���ʵ���֮�ȿ�����5��3��2
�ο��𰸣�B
���������
�����Ѷȣ���
4��ѡ���� ��ʯ��Ҥ��������ʯ�ң�1mo1 CuCO3��ȫ�ֽ�����Ҫ����������ȼ��0.453mo1̼���ṩ���������O2�������Ϊ0.21��N2Ϊ0.79����ʯ��Ҥ������������CO2���������������
A.0.50
B.0.46
C.0.49
D.0.52
�ο��𰸣�B
�����������������̼ȼ��C+O2 CO2��֪��0.453mol̼��ȫȼ������O20.453mol������CO20.453mol����CaCO3�ֽ�CaCO3
CO2��֪��0.453mol̼��ȫȼ������O20.453mol������CO20.453mol����CaCO3�ֽ�CaCO3 CaO+CO2 ����֪��1molCaCO3��ȫ�ֽ�����CO21mol���ʷ�Ӧ������CO2����Ϊ��1.453mol������0.453molO2���е�N2Ϊ0.453mol��
CaO+CO2 ����֪��1molCaCO3��ȫ�ֽ�����CO21mol���ʷ�Ӧ������CO2����Ϊ��1.453mol������0.453molO2���е�N2Ϊ0.453mol�� =1.70mol���ݴ˼����жϣ�ע����̼����ȫȼ���������̼���������С��
=1.70mol���ݴ˼����жϣ�ע����̼����ȫȼ���������̼���������С��
�����̼ȼ��C+O2 CO2��֪��0.453mol̼��ȫȼ������O20.453mol������CO20.453mol��
CO2��֪��0.453mol̼��ȫȼ������O20.453mol������CO20.453mol��
��CaCO3�ֽ�CaCO3 CaO+CO2 ����֪��1molCaCO3��ȫ�ֽ�����CO21mol��
CaO+CO2 ����֪��1molCaCO3��ȫ�ֽ�����CO21mol��
�ʷ�Ӧ������CO2����Ϊ��0.453mol+1mol=1.453mol������0.453molO2���е�N2Ϊ0.453mol�� =1.70mol��
=1.70mol��
������CO2���������Ϊ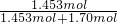 =0.46���������ֵ���粿������CO���������̼���������С��
=0.46���������ֵ���粿������CO���������̼���������С��
��ѡ��B��
������������Ҫ�������ﷴӦ�ļ��㣬�ѶȽϴ��Ƕ�ѧ��������ѧ��ѧ֪ʶ�ۺϷ����ͽ��ʵ��������������飬������ѧ�����������˼ά��ȣ�ǿ����ѧ������֪ʶ��������
�����Ѷȣ�һ��
5��ѡ���� ��5.1 gþ���Ͻ�Ͷ��500 mL 2.0 mol��L��1�������У�������ȫ�ܽ⣬�ټ���4.0 mol��L��1��NaOH��Һ����Ҫ���ɵij�����࣬��Ӧ����NaOH��Һ������� (�� ��)
A.200 mL
B.250 mL
C.425 mL
D.560 mL
�ο��𰸣�B
��������������������Ҫ���ɵij�����࣬��ǡ�÷�Ӧ����������þ����������ʱ������ࡣ��ʱ��Һ�е����ʾ�ֻ���Ȼ��ƣ������ԭ���غ��֪���Ȼ��Ƶ����ʵ�����0.5L��2.0mol/L��1.0mol�������������Ƶ����ʵ���Ҳ��1.0mol��������������Һ�������1.0mol��4.0mol/L��0.25L��250ml����ѡB��
���㣺����þ���Ͻ�����Ӧ���йؼ���
�����������Ǹ߿��еij������ͣ������е��Ѷ�����Ŀ��顣�����ۺ���ǿ����ע�ض�ѧ������֪ʶ���̺�ѵ����ͬʱ�����ض�ѧ�����������������ͷ�����ָ����ѵ����ּ�ڿ���ѧ��������û���֪ʶ���ʵ�����������������������ѧ���������������ͷ�ɢ˼ά����������Ĺؼ�����ȷ��Ӧԭ�������ú�ԭ���غ㼴�ɡ�
�����Ѷȣ�һ��