微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (6分)在KClO3 + 6HCl(浓) =" KCl" + 3Cl2↑ + 3H2O的反应中,氧化剂是___________,还原产物是_________,得电子与失电子个数比是____________,氧化产物与还原产物的质量比是______,试用双线桥标出反应电子转移的方向和数目_________________________
参考答案:
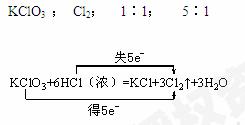
本题解析:略
本题难度:一般
2、选择题 将足量的氯气通入下列溶液中,溶质阴、阳离子的数目都明显改变的是?(?)
A.AgNO3
B.FeBr2
C.NaOH
D.Na2CO3
参考答案:B
本题解析:略
本题难度:简单
3、选择题 卤代烃A(C2H5X)是一种无色液体,为探究A的性质,设计如下实验方案。
方案一:往A中加入硝酸银溶液,充分振荡,静置。?
方案二:往A中加过量NaOH水溶液,充分振荡,静置,待液体分层后,取“水层”溶液少许,滴加硝酸银溶液。
方案三:往A中加入过量NaOH乙醇溶液,共热,充分反应后,取溶液少许,依次加入试剂B、硝酸银溶液,得白色沉淀。
根据以上信息回答问题。
(1)C2H5X中的X是?。?(写化学式)
(2)方案一中可观察到的现象是?。
(3)有人认为方案二达不到检验X-的实验目的,理由是?。
(4)方案三中,试剂B是?。写出方案三中可能发生反应的化学方程式?
参考答案:(共14分)(1)Cl?(2分)
(2)溶液分层(2分)
(3)过量的NaOH溶液会与硝酸银溶液反应生成沉淀(AgOH或Ag2O),从而干扰X-的检验。 (2分)
(4)稀硝酸(2分)CH3CH2Br+NaOH  CH2=CH2↑+NaBr+H2O?(2分)
CH2=CH2↑+NaBr+H2O?(2分)
HNO3+NaOH=NaNO3+H2O?(2分)? NaCl+AgNO3=AgCl↓+NaNO3?(2分)
本题解析:(1)根据加入硝酸银溶液,得白色沉淀,X是Cl。
(2)不反应发,但观察到溶液分层的现象。
(3)NaOH溶液会与硝酸银溶液反应生成沉淀(AgOH或Ag2O),故方案二达不到实验目的。
(4)要检验X离子,需要中和掉多余的碱性溶液,故试剂B是稀硝酸。方案三发生的反应为CH3CH2Br+NaOH  CH2=CH2↑+NaBr+H2O,HNO3+NaOH=NaNO3+H2O,NaCl+AgNO3=AgCl↓+NaNO3。
CH2=CH2↑+NaBr+H2O,HNO3+NaOH=NaNO3+H2O,NaCl+AgNO3=AgCl↓+NaNO3。
点评:本题是有关实验方案的设计和评价的考查,要求学生熟悉所实验的内容及原理,能够考查同学们进行分析问题、解决问题的能力。
本题难度:简单
4、选择题 被誉为"太空金属"的钛,在室温下,不跟水、稀盐酸、稀硫酸和稀硝酸等作用,但易溶于氢氟酸,你认为其原因可能是
A.氢氟酸的酸性比其他酸强
B.氢氟酸的氧化性比其他酸强
C.氢氟酸的还原性比其他酸强
D.钛离子易与氟离子形成可溶性难电离物质
参考答案:D
本题解析:
正确答案:D
氟原子半径小,电负性大,与其它原子间作用力大,决定了氟有许多特殊的性质。D符合。
A.不正确,氢氟酸是弱酸,酸性比其他酸弱? B.不正确,氢氟酸是非氧化性酸,氧化性不比其他酸强; C.不正确,氢氟酸中的-1价的氟,很难失电子,还原性比极弱。
本题难度:简单
5、实验题 某研究性学习小组欲利用下列装置制取少量次氯酸钠,并进一步探究次氯酸钠的化学性质。

相关资料:反应Cl2+2NaOH=NaClO+NaCl+H2O属于放热反应,温度稍高时便发生副反应3Cl2+6NaOH=NaClO3+5NaCl+3H2O。
(1)制取氯气时,在烧瓶中加入一定量的二氧化锰,通过____________(填写仪器名称)向烧瓶中加入适量的浓盐酸。请在装置A、B、C中选择一个合适的装置放在②处:____________。
(2)部分学生认为上述装置存在缺点,他们指出在①②装置之间应增加如D所示的装置,你认为D中所盛液体是________,其作用是________________________________________。

(3)该小组对产品的性质进行了如下探究。
第一步,测其pH=10。结合相关离子方程式解释原因:_________________________________________________________________。
第二步,该小组的同学选用了紫色石蕊试液对次氯酸钠的性质进行探究。请你帮助他们完成下表:
?
参考答案:(1)分液漏斗 C
(2)饱和食盐水 除去Cl2中的HCl
(3)NaClO是强碱弱酸盐,水解呈碱性,ClO-+H2O?HClO+OH-
实验操作
预期现象
结论
取一干净试管,加入1~2 mL产品,然后滴加几滴紫色石蕊试液
溶液先变蓝后褪色
次氯酸钠溶液具有碱性和氧化性(或漂白性)
本题解析:(1)由于氯气和氢氧化钠反应是放热反应,且温度过高时,会发生副反应,所以应选择装置C。(2)由于盐酸易挥发,制得的Cl2中含有HCl杂质,所以需要加洗气装置。(3)次氯酸钠溶液水解呈碱性;由于次氯酸钠溶液除呈碱性外还有漂白性,故加入紫色石蕊试液后先变蓝后褪色。
本题难度:一般