微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (16分)辉铜矿是冶炼铜的重要原料。
(1)工业上冶炼粗铜的某种反应为:Cu2S+O2=2Cu+SO2
①当产生标况下11.2L气体时,转移电子数目为?;
②将粗铜进行电解精炼,粗铜应与外电源的?极相接;若精炼某种仅含杂质锌的粗铜,通电一段时间后测得阴极增重ag,电解质溶液增重bg,则粗铜中含锌的质量分数为?;
(2)将辉铜矿、软锰矿做如下处理,可以制得碱式碳酸铜:

①铜单质放置于潮湿空气中,容易生成碱式碳酸铜,反应化学方程式是?;
②步骤Ⅱ中,碳酸氢铵参与反应的离子方程式为?;
③步骤Ⅰ中发生如下3个反应,已知反应i)中生成的硫酸铁起催化作用。请写出反应iii)的化学方程式。
i)Fe2O3+3H2SO4 =Fe2(SO4)3+3H2O
ii) Cu2S+ Fe2(SO4)3 =CuSO4+CuS+2FeSO4
iii)?
④步骤Ⅱ中调节pH后的溶液中,铜离子浓度最大不能超过?mol/L。
(已知Ksp[(Cu(OH)2)]=2×10-a)
参考答案:(1)3NA?(2)正 ③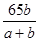 ?(2)①2Cu+O2+CO2+H2O=Cu2(OH)2CO3?②HCO3-+H+=H2O+CO2↑
?(2)①2Cu+O2+CO2+H2O=Cu2(OH)2CO3?②HCO3-+H+=H2O+CO2↑
③iii)MnO2+2FeSO4+2H2SO4=MnSO4+Fe2(SO4)3+2H2O?④2×1021-a
本题解析:(1)①根据反应Cu2S+O2=2Cu+SO2可知,反应中氧元素化合价和铜元素化合价降低,只有硫元素的化合价从-2价升高到+4价,失去6个电子,所以当产生标况下11.2L气体即0.5mol二氧化硫时,转移电子物质的量是0.5mol×6=3mol,其数目为3NA。
②将粗铜进行电解精炼,粗铜应与外电源的正极相接;若精炼某种仅含杂质锌的粗铜,通电一段时间后测得阴极增重ag,增加的质量即为析出的铜,电解质溶液增重bg,设参加反应的锌和铜的质量分别是mg、ng,则m+n-a=b,根据电子守恒可知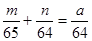 ?,解得m=65b,则粗铜中含锌的质量分数为
?,解得m=65b,则粗铜中含锌的质量分数为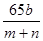 ?=
?=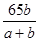 。
。
(2)①铜单质放置于潮湿空气中,容易与氧气、水、二氧化碳等结合生成碱式碳酸铜为生锈,反应化学方程式是2Cu+O2+CO2+H2O=Cu2(OH)2CO3。
②步骤Ⅱ是调节溶液pH的,因此碳酸氢铵与氢离子反应,则反应的离子方程式为HCO3-+H+=H2O+CO2↑。
③硫酸铁起催化作用,则第二步中生成的硫酸亚铁需要在第三步中重新被氧化生成硫酸铁,因此反应的化学方程式为MnO2+2FeSO4+2H2SO4=MnSO4+Fe2(SO4)3+2H2O。
④溶液的pH=3.5,则溶液中氢氧根浓度是10-10.5mol/L,所以根据氢氧化铜的溶度积常数可知,铜离子的浓度不能超过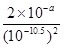 ?=2×1021-a mol/L。
?=2×1021-a mol/L。
本题难度:一般
2、填空题 (4分)已知Cu+在酸性溶液中可发生自身氧化还原反应生成Cu和Cu2+。CuH是一种难溶物,它会在氯气中燃烧,也能与盐酸反应放出气体。写出这两个化学方程式:
①在氯气中燃烧:?
②与盐酸反应:?
参考答案:(1)? 2CuH+3Cl2= 2CuCl2+2HCl?(2)? 2CuH+2HCl = CuCl2+2H2↑+Cu
本题解析:(1)根据组成元素可知,燃烧产物是氯化铜和氯化氢,方程式是2CuH+3Cl2= 2CuCl2+2HCl。
(2)Cu+在酸性溶液中可发生自身氧化还原反应生成Cu和Cu2+,所以CuH在盐酸中反应生成氯化铜、铜和氢气,反应的方程式是2CuH+2HCl = CuCl2+2H2↑+Cu。
本题难度:一般
3、填空题 以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等。实验室模拟工业以硫酸渣制备铁红(Fe2O3),过程如下:
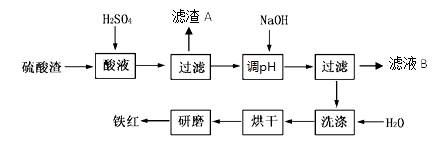
(1)硫酸渣的成分中属于两性氧化物的是?,写出酸溶过程Fe2O3与稀硫酸反应的离子反应方程式?;
(2)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是?(部分阳离子以氢氧化物形式沉淀时溶液的pH见下表)
沉淀物
| Fe(OH)3
| Al(OH)3
| Fe(OH)2
| Mg(OH)2
|
开始沉淀
| 2.7
| 3.8
| 7.5
| 9.4
|
完全沉淀
| 3.2
| 5.2
| 9.7
| 12.4
|
?
(3)滤渣A的主要成分为?,滤液B可以回收的物质有____________;
(4)简述洗涤过程的实验操作?;
(5)已知硫酸渣质量为w kg,假设铁红制备过程中,铁元素损耗25%,最终得到铁红的质量为m kg,则原来硫酸渣中铁元素质量分数为?(用最简分数表达式表示)。
参考答案:(1)Al2O3? Fe2O3 + 6H+ ==2Fe3+ + 3H2O
(2)3.2―3.8
(3)SiO2? Na2SO4? Al2(SO4)3? MgSO4
(4)沿玻璃棒向漏斗(过滤器)的沉淀加蒸馏水至淹没沉淀,静置使液体自然流出,重复操作数次(3次)至沉淀洗涤干净。
(5)14m/15w
本题解析:(1)Al2O3为两性氧化物,硫酸渣的成分中属于两性氧化物的是Al2O3;Fe2O3与硫酸反应生成Fe2(SO4)3和H2O,离子方程式是Fe2O3+6H+=2Fe3++3H2O;
(2)由题所给的数据可以看出,要使Fe3+完全沉淀而其它离子不能沉淀,其pH范围是3.2-3.8;
(3)硫酸渣中SiO2不与硫酸反应,所以滤渣A的主要成分是SiO2;加入NaOH调节pH后,Fe3+转化为Fe(OH)3沉淀,其它离子仍为硫酸盐,所以滤液B可以回收的物质有:Na2SO4、Al2(SO4)3、MgSO4。
(4)利用蒸馏水洗涤的方法是,沿玻璃棒向漏斗(过滤器)的沉淀加蒸馏水至淹没沉淀,静置使液体自然流出,重复操作数次(3次)至沉淀洗涤干净。
(5)m kg铁红含铁元素的质量为112m/160,所以硫酸渣中铁元素质量分数为
14m/15w。
本题难度:一般
4、填空题 铜是生命必需的元素,也是人类最早使用的金属之一,铜的生产和使用对国计民生各个方面产生了深远的影响。请完成(1)~(3)题:
(1)在西汉古籍中曾有记载:曾青得铁则化为铜[即曾青(CuSO4)与铁反应生成铜]。试写出该反应的化学方程式: _____________________________。
(2)铜器表面有时会生成铜绿,请写出生成铜绿的化学方程式:____________________________。
这层铜绿可以用化学方法除去,试写出除去铜绿而不损伤器物的化学方程式: _________________________。
(3)铜钱在历史上曾经是一种广泛流通的货币。试从物理性质和化学性质的角度分析为什么铜常用于制造货币。(铜的熔点是1 183.4 ℃,铁的熔点是1 534.8 ℃)_________________ ___________。
参考答案:(1)Fe+CuSO4=FeSO4+Cu
(2)2Cu+O2+H2O+CO2=Cu2(OH)2CO3
Cu2(OH)2CO3+4HCl=2CuCl2+CO2↑+3H2O
(3)选择铜做货币是因为铜的熔点比较低,容易铸造成型;铜的化学性质比较稳定,不易被腐蚀
本题解析:本题考查有关铜的冶炼方法、铜化合物的性质,同时考查了有关铜的
应用。一方面要注意铜的性质很稳定,不易发生化学反应。但又应知道这种
稳定性是相对的,在适宜条件下也会与一些物质反应。
本题难度:一般
5、选择题 往2支分别装有浅绿色的Fe(NO3)2和FeSO4溶液的试管中,逐滴加入稀盐酸时,溶液的颜色变化应该是
A.前者基本没有改变、后者变棕黄色
B.前者变棕黄色、后者也变棕黄色
C.前者变棕黄色、后者基本没有改变
D.前者、后者都基本没有改变
参考答案:C
本题解析:当向装有浅绿色的Fe(NO3)2溶液的试管中,逐滴加入稀盐酸时,发生反应:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑,产生了Fe3+,所以溶液变为黄色;而当向装有浅绿色的FeSO4溶液的试管中,逐滴加入稀盐酸时,不会发生任何反应。所以溶液的颜色基本不变。因此选项为C。3-在酸性条件下发生的反应及溶液的颜色的变化的知识。
本题难度:一般