微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 (9分)10 mL含有a mol HCl的稀盐酸和10 mL含有b molNa2CO3的稀溶液,按下图方式分别缓慢向对方溶液中滴加,并不断摇动试管,试分析下表并完成各题:(题中气体体积均在标准状况下测定,且不考虑气体在水中的溶解)
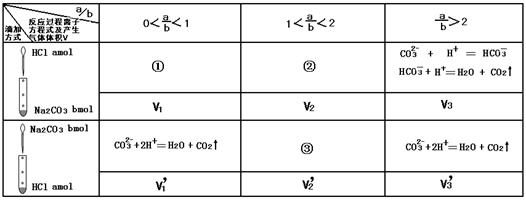
(1)表中对应过程的离子反应方程式:
①?;③?。
(2)上述所测六种情况下气体体积V1、V1"、V2、V2"、V3、V3"中为0的有?。
(3)V3与V3"的大小关系为V3?V3"(用“<” 、“>” 或“=”填空)
(4)若a=0.01,b=0.008,则V2=?mL、V2"=?mL。
参考答案:(1)①CO32-+H+ = HCO3-(1分)?③CO32-+2H+ = CO2↑+H2O(1分)
(2)V1(1分)?(3)=(2分)?(4)V2=44.8mL(2分)、V2"=112mL(2分)
本题解析:(1)碳酸钠和盐酸的反应是分步进行的,所以①、③的离子方程式是CO32-+H+ = HCO3-。反应③中盐酸是过量的,所以反应的离子方程式是CO32-+2H+ = CO2↑+H2O。
(2)由于碳酸钠和盐酸反应是分步进行的,所以若a小于b,则V1=0,其余都不是0。
(3)由于a大于2b,所以不论怎么滴加,生成的CO2都是相同的,即V3=V3"。
(4)若a=0.01,b=0.008,则根据方程式CO32-+H+ = HCO3-、HCO3-+H+ = CO2↑+H2O可知在反应②中生成的CO2是(0.01-0.008)mol=0.002mol,标准状况下的体积是44.8ml;而在反应③中根据方程式CO32-+2H+ = CO2↑+H2O可知,生成的CO2是0.01mol÷2=0.005mol,所以标准状况下的体积是0.005mol×22.4L/mol=0.112L=112ml。
本题难度:一般
2、选择题 有X、Y、Z三种溶液,在Na2CO3溶液中加入X,生成白色沉淀,在沉淀中加入Y,沉淀溶解并产生气体,再加入Z,又出现白色沉淀。X、Y、Z分别是()
X? Y? Z
A.CaCl2 HNO3 KCl
B.BaCl2 HNO3 Na2SO4
C.KCl H2SO4 CaSO4
D.BaCl2 H2SO4 CaCl2
参考答案:B
本题解析:通过在Na2CO3溶液中加入X,生成白色沉淀,可排除C选项。通过加入Y,沉淀溶解,可排除D选项,因为BaCO3不溶于稀H2SO4。再加入乙,又出现白色沉淀,可知B选项符合。
本题难度:简单
3、选择题 以下各组物质的性质比较中,正确的是(?)
A.热稳定性:Na2CO3>NaHCO3>H2CO3
B.溶解度:Na2CO3<NaHCO3<H2CO3
C.熔点:Rb>K>Na>Li
D.还原性:Rb<K<Na<Li
参考答案:A
本题解析:本题主要考查碱金属的性质递变规律和钠的化合物的性质。
本题难度:简单
4、选择题 把2.3 g钠放入水中,要使每100个水分子中含有1个Na+离子,所需水的质量是(?)。
A.184 g
B.181.8 g
C.180 g
D.183.6 g
参考答案:B
本题解析:
正确答案:B
2Na+2H2O=2NaOH+H2↑,2.3gNa为0.1mol,?末反应的水为100倍,10mol,反应的水为0.1mol,共10.1mol,181.8g
本题难度:一般
5、选择题 把一小块金属钠投入饱和石灰水中,不会出现的现象是(?)
A.溶液中出现白色浑浊
B.有金属被还原出来
C.钠与石灰水接触即爆炸
D.有气体放出
参考答案:BC
本题解析:钠与水首先反应,有氢气放出;产生的热量将使溶液的温度升高,而石灰水温度升高,溶解度降低,所以溶液中会出现白色浑浊。
本题难度:简单