微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 某反应是吸热反应,且所吸收的热能由外部热源(如酒精灯)提供,提供的热能主要起到的作用是
__________________________________________________________________________。
参考答案:①断裂化学键需要吸收能量;②以化学能形式储存于新的物质中
本题解析:一个化学反应的发生必定伴随着化学键的断裂,这需要吸收能量;同时这是个吸热反应,所以吸收的热能可以以化学能的形式储存于新的物质中。
本题难度:简单
2、选择题 下列有关电解质溶液的推理中正确的是
A.室温下,pH=4的醋酸和pH=10的氢氧化钠溶液等体积混合,其pH> 7
B.pH=3的盐酸与pH=11的氨水等体积混合后,溶液中:
c(NH4+)>c(Cl-)>c(OH-)>c(H+)
C.物质的量浓度相等的NH4Cl溶液和NH4HSO4溶液中,NH4+浓度相等
D.在有AgI沉淀的上清液中滴加 NaCl溶液,可以观察到白色沉淀产生
NaCl溶液,可以观察到白色沉淀产生
参考答案:B
本题解析:略
本题难度:一般
3、选择题 常温下,下列有关溶液的说法不正确的是
A.某物质的水溶液中由水电离出的c(H+)=1×10-a mol/L,若a>7,则该溶液的pH为a或14-a
B.将0.2 mol/L的某一元弱酸HA溶液和0.1mol/L NaOH溶液等体积混合后溶液中存在:2c(OH-)+ c(A-)=2c(H+)+c(HA)
C.pH=3的二元弱酸H2R溶液与 pH=11的NaOH溶液混合后,混合液的pH等于7,则混合液中c(R2-) > c(Na+) > c(HR-)
D.相同温度下,0.2mol/L的醋酸溶液与0.1mol/L的醋酸溶液中c(H+)之比小于2:1
参考答案:C
本题解析:
分析:A、酸或碱溶液能抑制水的电离.
B、根据溶液的酸碱性、溶液呈电中性、电离和水解的关系等分析各种离子浓度的关系.
C、根据电荷守恒和物料守恒判断离子浓度之间的关系.
D、相同温度下,弱电解质溶液的浓度越大其电离程度越小.
解:A、某物质的水溶液中由水电离出的c(H+)=1×1b-amol/L,若a>7,说明该溶液能抑制水的电离,可能是酸溶液或碱溶液,所以该溶液的PH值为a或14-a,故A正确.
B、pH=多的6元弱酸H2R溶液与 pH=11的NaOH溶液混合后,混合液的pH等于7,说明溶液中阴阳离子所带电荷相等,因为弱根离子能水解导致溶液中钠离子浓度大于c(R2-)的2倍,水解程度是微弱的,所以c(R2-)>c(HR-).所以离子浓度大小顺序是c(Na+)>c(R2-)>c(HR-),故B错误.
C、将b.2 mol/L的某一元弱酸HA溶液和b.1mol/L NaOH溶液等体积混合后,溶液中盐和酸的浓度都是b.b左mol/L,根据电荷相等有c(OH-)+c(A-)=c(H+)+c(Na+),根据物料守恒得c(A-)+c(HA)=2c(Na+),所以得2c(OH-)+c(A-)=2c(H+)+c(HA),故C正确.
D、相同温度手,当b.2mol/L的醋酸溶液与b.1mol/L的醋酸溶液电离度相等时,其氢离子浓度之比为2:1,但实际上
弱电解质溶液的浓度越大其电离程度越小,所以b.2mol/L的醋酸溶液与b.1mol/L的醋酸溶液中氢离子浓度小于2:1,故D正确.
故选B.
本题难度:一般
4、选择题 室温下,向20.00mL 1.000mol・L-1氨水中滴入1.000mol・L-1盐酸,溶液pH和温度随加入盐酸体积变化曲线如下图所示。下列有关说法错误的是


A.室温下,a点的氨水电离常数为
B.将此氨水稀释,溶液的导电能力减弱
C.c点时消耗盐酸体积V(HCl)<20mL
D.a、d两点的溶液,水的离子积Kw(a)>Kw(d)
参考答案:D
本题解析:水的离子积只与温度有关,温度相同水的离子积相同,错误;
本题难度:一般
5、填空题 下表是不同温度下水的离子积常数:
温度/℃
| 25
| T1
| T2
|
水的离子积常数
| 1×10-14
| a
| 1×10-12
|
?
试回答以下问题:
(1)若25<T1<T2,则a__________1×10-14 (填“>”、“<”或“=”),做此判断的理由是______________________________________。
(2)25℃时,某Na2SO4溶液中c(SO42―)=5×10-4 mol/L,取该溶液1 mL加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)=__________。
(3)T2℃时,将pH=11的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1∶V2=__________。此溶液中各种离子的浓度由大到小的顺序是____________________________。
(4)常温下,设某pH值的硫酸中水电离出的c(H+)=1.0×10-a mol/L,设相同pH值的硫酸铝中水电离出的c(H+)=1.0×10-b mol/L,(a、b都是小于14的正数),那么a、b之间满足的关系式是________________。
参考答案:(1)> 水的电离吸热,温度升高,水的电离程度增大,所以水的离子积增大?
(2)1000 (3)9∶11 c(Na+)>c(SO42―)>c(H+)>c(OH-) (4)a+b=14
本题解析:(1)温度升高水的电离程度增大KW增大,a>1×10-14,(2)Na2SO4溶液中c(Na+)=1×10-3,稀释后为1×10-4,c(OH-)=1×10-7,所以c(Na+)∶c(OH-)=1000,(3)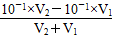 =10-2,10-1V2-10-1V1=10-2V2+10-2V1,即9×10-2V2=11×10-2V1,
=10-2,10-1V2-10-1V1=10-2V2+10-2V1,即9×10-2V2=11×10-2V1,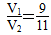 ,所以c(Na+)>c(SO42―)>c(H+)>c(OH-),(4)硫酸的pH为-lg
,所以c(Na+)>c(SO42―)>c(H+)>c(OH-),(4)硫酸的pH为-lg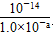 ,硫酸铝的pH=-lg1.0×10-b,
,硫酸铝的pH=-lg1.0×10-b,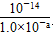 =1.0×10-b,所以a+b=14。
=1.0×10-b,所以a+b=14。
本题难度:一般