��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪2Fe3+ +Cu=Cu2+ +2Fe2+,�ְ���ͬ���ʵ���������ͭ���Ȼ�����п����ˮ�г�ַ�Ӧ��Ӧ�������û�������SO42-?��Cl-�⣬ ������(? )
A��Zn2+��Cu��Fe3+
B��Zn��Cu2+��Fe3+
C��Zn2+��Cu2+��Cu��Fe2+
D��Zn2+��Cu2+��Fe��Fe2+
�ο��𰸣�C
������������ݷ�Ӧ��֪�����ԣ�Fe3+>Cu2+>Fe2+������Zn����Fe3+��Ӧ��ΪZn+2Fe3+=Zn2++2Fe2+��������ͭ���Ȼ�����п�����ʵ���Ϊ1mol����һ����Ӧ���ʣ���ZnΪ0.5mol������Cu2+��Ӧ��ΪZn+Cu2+=Zn2++Cu����Cu2+��ʣ�ࡣ������Һ�д���Zn2+��Cu2+��Fe2+����Cu���ɣ���ѡC��
������������Ҫ�����������м��㣬����ѧ�������Ϣ�������ͷ���������
�����Ѷȣ�һ��
2������� �����£���û����������ʱ������ˮ��������Ӧ���������£�������ˮ������Ӧ��
��1��������ˮ������Ӧ�Ļ�ѧ����ʽ�ǣ�
��2��ֹͣ��Ӧ����װ����ȴ��ȡ����Ӧ�������ۻ������������ϡ�����ַ�Ӧ�����ˡ���������������Һ��Fe3���IJ���������
��3��������������Һ�в���Fe3�����ⲻ��˵��������ˮ������Ӧ���ò����в�����3�۵�����ԭ���ǣ���ϻ�ѧ����ʽ˵������
��4��ijͬѧ����������Һ��ȡ��ɫ��Fe��OH��2����������Һ�м���NaOH��Һ�۲쵽���ɵİ�ɫ����Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ��
�ٳ����ɰ�ɫ��Ϊ���ɫ�Ļ�ѧ����ʽ�ǣ�
��Ϊ�˵õ���ɫ��Fe��OH��2��������������ʹ������ʱ�䱣�ְ�ɫ�������������ͼ��ʾ��װ�ã�
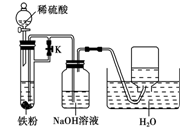
�����ʵ�������ԭ����
�ο��𰸣���1��? 3Fe��4H2O��g�� Fe3O4��4H2��?
Fe3O4��4H2��?
��2��ȡ������Һ���Թ��У����뼸��KSCN��Һ���۲���Һ��ɫ�������Һ��ɫ��ΪѪ��ɫ��˵����Һ�к���Fe3��������Fe3��?
��3�������Ӧ������ۻ���������۹������ɷ�����Ӧ��Fe��Fe2��SO4��3===3FeSO4�����۽���Һ�е�Fe3��ȫ����ԭΪFe2�����������KSCN��ҺҲ����Ѫ��ɫ
��4��?��? 4Fe��OH��2��O2��2H2O===4Fe��OH��3?
��ʵ��ʱ���ȴ���K���ٽ���Һ©���е�������ʹϡ�������������ã��ò�����H2�ų�װ���еĿ�����Ȼ��ر�K��ʹ���ɵ�H2���Թ��е�FeSO4��Һѹ��NaOH��Һ�У������ʢNaOH��Һ���Լ�ƿ�нϳ�ʱ��۲쵽���ɵİ�ɫFe��OH��2����
���������
���⿼�������仯�ϵ��ص�֪ʶ�㣬���ڶ����֪ʶ��������ֱ��Ӧ�ã��Ƚ����ס�
��1��ע�������Fe3O4�� 3Fe��4H2O��g�� Fe3O4��4H2��?
Fe3O4��4H2��?
��2��Fe3���ļ��飺ȡ������Һ���Թ��У����뼸��KSCN��Һ���۲���Һ��ɫ�������Һ��ɫ��ΪѪ��ɫ��˵����Һ�к���Fe3��������Fe3��?
��3�������Ӧ������ۻ���������۹������ɷ�����Ӧ��Fe��Fe2��SO4��3===3FeSO4�����۽���Һ�е�Fe3��ȫ����ԭΪFe2�����������KSCN��ҺҲ����Ѫ��ɫ
��4��?��? 4Fe��OH��2��O2��2H2O===4Fe��OH��3?
��ʵ��ʱ���ȴ���K���ٽ���Һ©���е�������ʹϡ�������������ã��ò�����H2�ų�װ���еĿ�����Ȼ��ر�K��ʹ���ɵ�H2���Թ��е�FeSO4��Һѹ��NaOH��Һ�У������ʢNaOH��Һ���Լ�ƿ�нϳ�ʱ��۲쵽���ɵİ�ɫFe��OH��2����
�����Ѷȣ�һ��
3��ѡ���� ����˵��������ǣ�
A��ij��ˮ��Ʒ�ɼ������һ��ʱ�䣬pH��4.68��Ϊ4.28������Ϊˮ���ܽ��˽϶��CO2
B��������NaAlSiO4��nH2O�ɸ�д����������ʽΪ��Na2O��Al2O3��2SiO2��2nH2O
C��Al65Cu23Fe12��һ���⾧�����кϽ�������������ܣ���Ӳ�ȱȽ���Al��Cu��Fe����
D����������Ũ������ȷ�Ӧ���Եõ�����
�ο��𰸣�A
���������A��ij��ˮ��Ʒ�ɼ������һ��ʱ�䣬pH��4.68��Ϊ4.28������Ϊˮ���ܽ��˽϶��SO2��������Ӧ��2SO2+2H2O+ O2=2H2SO4���������Ϊǿ�ᣬ��Һ��H+Ũ����������pH��С������B�������μȿ������ε���ʽ��ʾ��Ҳ���������������ʽ��ʾ�����ò�ͬ����ʽ��ʾʱ������Ԫ�ص�ԭ�Ӹ�������ͬ�����NaAlSiO4��nH2OҲ�ɸ�д����������ʽΪ��Na2O��Al2O3��2SiO2��2nH2O����ȷ��C. Al65Cu23Fe12��һ���⾧�����кϽ�������������ܣ��Ͻ�����������������ܣ���Ӳ�ȱȳɷֽ������۷е�ȳɷֽ����͵ȡ�����Ӳ�ȱȽ���Al��Cu��Fe������ȷ��D������Ũ������ȷ�Ӧ�õ������������������ˮ���������������������Fe������Ӧ�õ��������������ŷ�Ӧ�Ľ��У������Ϊϡ���ᣬ����Fe��ϡ���ᷴӦ�õ�����������������������տ��Եõ���������ȷ��
�����Ѷȣ�һ��
4��ѡ���� �����±�����ʵ�鼰����ó��Ľ��۲���ȷ���ǣ�?��
ʵ����Ŀ
| ʵ������
|
FeCl3��Һ�м���ά����C(VC)
| ��Һ��ɫΪdz��ɫ
|
����FeCl3��Һ�����ˮ��
| �õ����ɫҺ��
|
��ͭ�����������
| ����ɫ���ݲ���
|
?
A��ά����C(VC)���л�ԭ��
B��FeCl3ˮ������Fe(OH)3����
C��ͭ�������ᷴӦ��H2����
D��ͭ���к���̼���
�ο��𰸣�C
�����������FeCl3��Һ�м���VC����Һ�ɻ�ɫ��Ϊdz��ɫ(Fe2��)��˵��Fe3��������������VC����ԭ�������л�ԭ�ԣ�A��ȷ������FeCl3�����ˮ�еõ����ɫҺ�壬˵��FeCl3����ˮ�ⷴӦ����Fe(OH)3���壬B��ȷ��ͭ�����Ҫ�ɷ���Cu2(OH)2CO3�������ᷴӦ������������CO2������H2��D����ȷ��
�����Ѷȣ�һ��
5��ѡ���� ��Fe2(SO4)3��CuCl2�����Һ��Ͷ�����������۳�ַ�Ӧ�õ��Ĺ��徭���ˡ�������أ������ù�����������������۵�������ȣ���ԭ��Һ��c(SO42��)��c(Cl��)֮��Ϊ��
A��3�U14
B��1�U7
C��2�U7
D��3�U2
�ο��𰸣�A
������������ݷ���ʽ��2Fe2(SO4)3+2Fe="3" Fe2(SO4)3��������ȫ�ܽ⣬������������112g��? 14Fe+14CuCl2=14FeCl2+14Cu ��������������112g������c(SO42��)��c(Cl��)֮��Ϊ��6:28=3:14����ȷ��ΪA��
�����Ѷȣ�һ��