微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (8分)A、B、C、D、E、F为原子序数依次增大的短周期元素,B、C相邻且同周期,A、D同主族。C原子最外层电子数是核外电子层数的3倍,A、C能形成两种化合物甲和乙,原子个数比分别为2∶1和1∶1,甲为常见的溶剂。E是地壳中含量最多的金属元素;F元素为同周期电负性最大的元素。D和F可形成化合物丙,E和F可形成化合物丁。G为第四周期未成对电子数最多的元素。请回答下列问题:
(1)写出G基态原子的价电子排布式?。
(2) B和C比较,第一电离能较大的是?(填元素符号),其原因为?。
(3)甲、乙两分子的中心原子的杂化类型是否相同?(相同、不相同)。
(4)已知化合物丁熔点190℃,沸点183℃。丙和丁比较,熔点较高的是?(填化学式),
(5)配合物戊由G3+与甲、元素F构成,已知该配合物的配位数为6。在含有0.1mol戊的溶液中加入AgNO3溶液至过量,经过滤、洗涤、干燥后,得到28.7g白色沉淀。,则戊的化学式为?。
参考答案:(1)3d54s1 (2)N;N 原子价电子为2s22p3,2p轨道半充满,能量较低,难失1个电子,O原子价电子为2s22p4,易失1个电子;(3)相同;(4)NaCl;(5)[Cr(H2O)5Cl]Cl2
本题解析:根据题意可推出:A是H;B是N;C是O;D是Na;E是Al;F是Cl;G是Cr。甲是H2O;乙是H2O2;丙是NaCl;丁是AlCl3.(2)24号元素Cr基态原子的价电子排布式3d54s1;(2)一般情况下,同一周期的元素,元素的非金属性越强,其第一电离能越大,但是由于N原子核外的2p轨道上的电子处于半充满的稳定状态,能量较低,所以失去电子较难,因此N和O比较,第一电离能较大的是N;(3)在H2O和H2O2两分子的中心原子O的杂化类型是相同的,都是sp3杂化。(4)NaCl是离子晶体;而AlCl3.是分子晶体,分子晶体中分子之间通过分子间作用力结合,而离子晶体中离子之间通过离子键结合,离子键是一种强烈的相互作用,断裂较难,因此熔点较高的是NaCl。(5)在0.1mol戊电离产生的Cl-的物质的量为:n(Cl-)="n(AgCl)=" 28.7g÷143. 5g/mol=0.2mol,因此在一个戊的外围含有2个Cl-.由于配合物戊由Cr3+与甲、元素F构成,已知该配合物的配位数为6。所以在其络离子中含有一个Cl-.其余的是水分子。因此根据化合物中正负化合价的代数和为0的原则,可知该络合物的化学式是[Cr(H2O)5Cl]Cl2。
本题难度:一般
2、选择题 下列各组原子中,化学性质一定相似的是
A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子
B.原子核外M层上仅有两个电子的X原子与原子核外N层上仅两个电子的Y原子
C.2p轨道上只有一个空轨道的X原子与3p轨道上只有一个空轨道的Y原子
D.最外层都只有一个电子的X、Y原子
参考答案:C
本题解析:A、原子核外电子排布式为1s2为He,原子核外电子排布式为1s22s2为Be,二者性质不同,故A错误;B、原子核外M层上仅有两个电子的X为Mg元素,原子核外N层上仅有两个电子的Y可能为Ca、Sc、Ti、V、Fe、Co、Ni、Zn等元素,但价电子数不同,性质不相同,故B错误;C、2p轨道上只有一个电子的X为B元素,3p轨道上只有一个电子的Y为Al,二者位于周期表同一主族,最外层电子数相同,性质相似,故C正确;D、最外层都只有一个电子的X、Y原子,可能为H与碱金属元素,性质有相似地方,都具有还原性,但与ⅠB族元素性质不同,虽然最外层也有1个电子,故D错误,故选C。
本题难度:一般
3、选择题 原子半径由小到大,且最高正价依次降低的是(?)
A.Al、Mg、Na
B.N、O、F
C.Ar、Cl、S
D.Cl、P、Si
参考答案:D
本题解析:题中所给选项的元素都是第二、第三周期元素,而在同周期的元素由左到右原子序数依次递增,原子半径依次递减,它们所属主族数也依次递增,最外层电子数依次递增,最高正价依次递增。所以选择D选项。
本题难度:简单
4、推断题 由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有下图的转化关系,已知C为密度最小的气体,甲为非电解质。
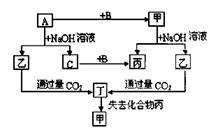
根据以上转化关系回答下列问题:
(1)写出下列物质的化学式:A ?B?丁?。
(2)元素A在周期表中的位置是?,写出甲的一种用 途?。
(3)写出下列变化的方程式:
A与NaOH溶液反应的化学方程式?。
乙与过量CO?2反应的离子方程式?。
参考答案:
(1)Si(2分)? O2(2分)? H2SiO3或H4SiO4(2分)
(2)第三周期第ⅣA族(2分)?是玻璃、光导纤维等(2分)
(3) ①Si+2NaOH+H2O=Na2SiO3+2H2↑(2分)
② SiO32―+2CO?2+2H2O=H2SiO3↓+2HCO3―(2分)
本题解析:根据题意可知A:SiB:O2、C:H2、甲:SiO2、乙:Na2SiO3、丙:H2O、丁:H2SiO3。
(1)突破口:C为密度最小的气体,知C是H2;甲为非电解质,不能是Al2O3,只能是SiO2;则A为Si、B为O2、 乙是Na2SiO3,通CO?2生成丁,丁为H2SiO3。丁失去丙生成甲,丙为H2O。
(2)A为Si,在周期表的第三周期第ⅣA族;用途是做玻璃、光导
本题难度:一般
5、选择题 英国《自然》杂志曾报道,科学家用DNA制造出一种臂长只有7nm的纳米(1nm=10-9m)级镊子,这种镊子能钳起分子或原子,并对它们随意组合,下列分散系中分散质的微粒直径与纳米级镊子具有相同数量级的是
A.溶液
B.乳浊液
C.悬浊液
D.胶体
参考答案:D
本题解析:分析:据分散质的微粒直径大小判断.
解答:纳米级镊子的直径在1-100nm之间,溶液中溶质的直径<1~100nm,悬浊液、乳浊液分散质粒子直径>1~100nm,胶体粒子的直径在1~100nm之间;答案为胶体;
故选D.
点评:本题考查了胶体分散系的本质特征,主要掌握分散质微粒直径的大小.
本题难度:简单