��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ������ػ�ѧԭ���������ж���ȷ����
[? ]
A����X��ԭ�Ӿ��壬Y�Ƿ��Ӿ��壬���۵㣺X<Y
B����KXO3+Y2===2KYO3+X2���������ԣ�Y2> X2
C����R2- ��M+�ĵ��Ӳ�ṹ��ͬ����ԭ��������R>M
D��������HA������ǿ������HB����ͬŨ��������Һ�ļ���:NaA<NaB
�ο��𰸣�D
���������
�����Ѷȣ�һ��
2��ѡ���� ij��Һ��ֻ����Na����H����OH����A���������ӣ�����˵����ȷ����
[? ]
A����c(OH��)>c(H��)����Һ�в����ܴ��ڣ�c(Na��)>c(OH��)>c(A��)>c(H��)
B����Һ�в����ܴ��ڣ�c(Na��)>c (A��)>c(OH��)>c(H��)
C������Һ��c(A��) = c(Na��)������Һһ��������
D��������ΪNaA��HA����һ�����ڣ�c(A��)>c(Na��)>c(H��)>c(OH��)
�ο��𰸣�C
���������
�����Ѷȣ�һ��
3��ѡ���� 25��ʱ����ϡ��ˮ��μ��뵽ϡ�����У�����Һ��pH=7ʱ�����й�ϵ��ȷ����
[? ]
A��c��NH4+��=c��SO42-��
B��c��NH4+��>c��SO42-��
C��c��NH4+��<c��SO42-��?
D��c��OH-��+c��SO42-��=c��H+��+��NH4+��
�ο��𰸣�B
���������
�����Ѷȣ�һ��
4��ѡ���� �����Σ���FeCl3?��CH3COONa?��NaCl����ˮ��Һ��pH�ɴ�С������ȷ���ǣ�������
A���٣��ۣ���
B���ڣ��ۣ���
C���ۣ��ڣ���
D���٣��ڣ���
�ο��𰸣�B
���������
�����Ѷȣ���
5������� ��ҵ�ϵ�ⱥ��ʳ��ˮ�ɵõ����ֹ�ҵԭ�ϣ�����������������;�dz��㷺��
��1����ͼ��ʾ�����ӽ���Ĥ������������ͨ������������������������ͨ��������ⱥ��ʳ��ˮʾ��ͼ���������У�A����������______�����������ԭ������Ӧ��B���ĵ缫��Ӧ����ʽΪ______�������缫���ϻ�Ϊ��������B���ĵ缫��ӦΪ______��
��2�����Ϸ�Ӧ�õ���H2��C12��ֱ�ӻ��������ᣮ������������ԭ���ԭ��ֱ���Ʊ����ᣬͬʱ��õ��ܣ�������������У���ͨ�����ĵ缫Ϊ______����ͨ�����ĵ缫��ӦʽΪ______��
��3����ҵ�Ƶõ�Ũ���������ʻ�ɫ��ԭ�����������������ܵ�����ʴ���£���д���йط�Ӧ�Ļ�ѧ����ʽ______�����ָ�ʴ����______��
��4�������£���1.000mo1?L-1�������20.00mL1.000mo1?L-1��ˮ�У�����ҺpH=7ʱ��c��C1-��______c��NH4+������=������������������20.00mL����ʱ����Һ�и�����Ũ���ɴ�С��˳��Ϊ______��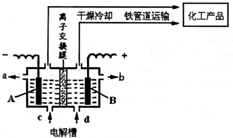
�ο��𰸣���1����ͼ��֪��AΪ��������������������ԭ��Ӧ����BΪ�������õ缫��ӦΪ2C1--2e=C12���������缫���ϻ�Ϊ������BΪ����������ʧȥ���ӣ��缫��ӦΪFe-2e=Fe2+��
�ʴ�Ϊ����ԭ��2C1--2e=C12����Fe-2e=Fe2+��
��2����H2+C12�T2HCl��HԪ�صĻ��ϼ����ߣ���ͨ����Ϊ������ClԪ�صĻ��ϼ۽��ͣ���ͨ����Ϊ��������������ӦΪC12+2e=2Cl-��
�ʴ�Ϊ������C12+2e=2Cl-��
��3��Ũ���������ʻ�ɫ���������Fe3+������Fe�������Ļ�ѧ��Ӧ����ӦΪ2Fe+3C12=2FeC13�����ڻ�ѧ��ʴ���ʴ�Ϊ��2Fe+3C12=2FeC13����ѧ��ʴ��
��4��pH=7ʱ��c��H+��=c��OH-�����ɵ���غ��֪��c��OH-��+c��C1-��=c��NH4+��+c��H+������c��C1-��=c��NH4+����������20.00mL����ʱ��ǡ�������Ȼ�泥�笠�����ˮ�������ԣ���������Ũ�ȵĹ�ϵΪc��C1-����c��NH4+����c��H+����c��OH-����
�ʴ�Ϊ��=��c��C1-����c��NH4+����c��H+����c��OH-����
���������
�����Ѷȣ�һ��