��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �кͷ�Ӧ�ǵ��͵ķ��ȷ�Ӧ���������кͷ�Ӧ����1molˮʱ���ͷŵ�������Ϊ�к��ȡ����й����к��ȵ�˵����ȷ����
[? ]
A���кͷ�Ӧ�����κ�ˮ��������������ͼ��������
B��ϡ������������ƹ��巴Ӧ����1molˮ�ͷŵ�������Ϊ�к���
C��ϡ���������������Һ��Ӧ����1molˮ�ͷŵ�������Ϊ�к���
D���к��ȵIJⶨʵ����Ӧ������ֹ��Ӧ�е�������ʧ
�ο��𰸣�D
���������
�����Ѷȣ���
2������� ��1����1L1mol/L��NaOH��Һ�м����������ʣ���ŨH2SO4����ϡ�����ϡ���ᣬǡ����ȫ��Ӧ����ЧӦΪ��H1����H2����H3����������С����˳��Ϊ______��
��2���ɸ�˹���ɽ��������Ӧ����ʽ���ش����⣺
��NH3��g��+HCl��g���TNH4Cl��s����H=-176kJ/mol
��NH3��g��+H2O��l���TNH3?H2O��aq����H=-35.1kJ/mol
��HCl��g��+H2O��l���THCl��aq����H=-72.3kJ/mol
��NH3?H2O��aq��+HCl��aq���TNH4Cl��aq����H=-52.3kJ/mol
��NH4Cl��s��+2H2O��l���TNH4Cl��aq�����H����______?kJ/mol��
��3�����������Ȼ�ѧ����ʽ������д��C��s��ȼ���ȵ��Ȼ�ѧ����ʽ______��
C��s��+H2O��l���TCO��g��+H2��g����H1=+175.3kJ?mol-1
2CO��g��+O2��g���T2CO2��g����H2=-566.0kJ?mol-1
2H2��g��+O2��g���T2H2O��l����H3=-571.6kJ?mol-1��
�ο��𰸣���1��ǿ����ǿ���ϡ��Һ�����кͷ�Ӧ����ЧӦ��H+��aq��ʮOH-��aq��=H2O��H=һ57.3kJ/mol��
�ֱ���1L1mol/L��NaOH��Һ�м��룺��ŨH2SO4����ϡ�����ϡ���ᣬ����ĵ������ȣ�Ũ��������ˮ���ȣ���
ǡ����ȫ��Ӧʱ�ķų�������Ϊ�٣��ڣ��ۣ����ԡ�H1����H2����H3���ʴ�Ϊ����H1����H2����H3��
��2�����ݸ�˹���ɣ���+��-��+�۵�
? NH4Cl��s��+H2O��l��=NH4Cl��aq����H=��-35.1KJ?mol-1��+��-52.3KJ?mol-1��-��-176KJ?mol-1��+��-72.3KJ?mol-1��
? ?��NH4Cl��s��+H2O��l��=NH4Cl��aq����H=+16.3KJ?mol-1��
�ʴ�Ϊ��+16.3��
��3����C��s��+H2O��l���TCO��g��+H2��g����H1=+175.3kJ?mol-1
? ��2CO��g��+O2��g���T2CO2��g����H2=-566.0kJ?mol-1
? ?��2H2��g��+O2��g���T2H2O��l����H3=-571.6kJ?mol-1��
���ݸ�˹���ɣ���+�ڡ�12+�ۡ�12�ã�C��s��+O2��g���TCO2��g����H=-393.5?kJ?mol-1��
�ʴ�Ϊ��C��s��+O2��g���TCO2��g����H=-393.5?kJ?mol-1��
���������
�����Ѷȣ�һ��
3������� �ֱ�ȡ4��mL�Ĵ�?�˴�mol/L������4��mL?��.����mol/L����������Һ�����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ���ش��������⣮
��o���к��Ȳⶨ��ʵ���У��õ��IJ����������ձ����¶ȼơ�______��______��
���ã�Ϊʲô�к��Ȳⶨ��Ҫ���Թ����ļ���ᣩ��______
��3���������������������Һ���ܶȶ���og/��m3����֪�кͺ�������Һ�ı�������=4?o8J/��g?�棩��Ϊ�˼����к��ȣ�ijѧ��ʵ���¼�������£�

���ݸ�ѧ����ʵ�����ݼ��㣬��ʵ���õ��к��ȡ�H=______��?���������һλС����
��4������ʵ����ֵ������к��ȵ�����ֵ��7.34J/mol��ƫ�����ƫ���ԭ������ǣ�����ĸ��______��
a��ʵ��װ�ñ��¡�����Ч����?b����ȡ����������������Һʱ���Ӷ����ֶ�ΰ�Na��H��Һ����ʢ�������С�ձ���
d�����¶ȼƲⶨNaOH��Һ��ʼ�¶Ⱥ�ֱ�Ӳⶨ������Һ���¶ȣ�
�ο��𰸣��������к��Ȳⶨ��ʵ���У��õ��IJ����������ձ����¶ȼơ��������Լ���Ͳ���ʴ�Ϊ�����β������������Ͳ��
��2�����к��Ȳⶨ��ʵ���У�Ϊ�˱�֤�ᣨ���ܹ���ȫ���кͣ�����ʹ��һ���������ʴ�Ϊ��Ϊ�˱�֤�ᣨ���ܹ���ȫ���кͻ�ͨ������ֵ������Ƿ�Ӧ������mqlˮʱ�ķ�Ӧ�ȼ��к��ȣ�
��3��40mL��0?50mql/L������40mL?0.55mql/L����������Һ�У���Һ����m=30mL����g/mL=30g��c=4?��3J/��g?�棩�����빫ʽ��H=Q=cm��x�á�H=Q=4.��3J/��g?�棩��30g��(23.2-20.��)+(23.��-20.2)+(25.3-20.5)3=-50.2KJ/mql���ʴ�Ϊ��-50.2KJ/mql��
��4��a��ʵ��װ�ñ��¡�����Ч������ã�����Ӱ��ʵ��������a��ȷ��
b����ȡNaqH��Һ�����ʱ���Ӷ������ᵼ�������������������ƫ��b��ȷ��
c�������ֶ�ΰ�NaqH��Һ����ʢ�������С�ձ��У���c����
d�����¶ȼƲⶨNaqH��Һ��ʼ�¶Ⱥ�Ҫ���¶ȼƻ���ֱ�ٲⶨH2Sq4��Һ���¶ȣ���d��ȷ��
��ѡabd��
���������
�����Ѷȣ���
4������� ��ش��������к��ȵIJⶨʵ���йص����⣺
��1����ȡ��Ӧ��ʱ����ȡ50 mL 0.50 moI��L-1������뷴Ӧ�����У���Ӧ������Լ���____������ĸ���� A��50 mL 0.50 mol��L-1NaOH��Һ
B��50 mL0.55 mol��L-1NaOH��Һ
C��1.0 g NaOH����
D��1.05 g NaOH����
��2����ʵ������У���ͬѧ��Ҫ�ⶨ����¼��ʵ�������� ____������ĸ����
A�������Ũ��
B��������¶�
C������������Һ��Ũ��
D������������Һ���¶�
E��ˮ�ı�����
F����Ӧ������Һ����ֹ�¶�
�ο��𰸣���1��B
��2��BDF
���������
�����Ѷȣ�һ��
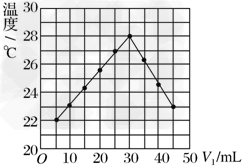
5��ѡ���� ��V1?mL?1.00?mol/L?HCl��Һ��V2?mLδ֪Ũ�ȵ�NaOH��Һ��Ͼ��Ⱥ��������¼��Һ�¶ȣ�ʵ������ͼ��ʾ(ʵ����ʼ�ձ���V1��V2��50?mL)������������ȷ����
[? ]
A������ʵ��ʱ�����¶�Ϊ22��?
B����ʵ�������ѧ�ܿ���ת��Ϊ����
C��NaOH��Һ��Ũ��ԼΪ1.0?mol/L?
D����ʵ�������ˮ���ɵķ�Ӧ���Ƿ��ȷ�Ӧ
�ο��𰸣�B
���������
�����Ѷȣ�һ��