��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���������У��������ᷴӦ�������ܲ�����������?��?����
A��Pb(NO3)2��Һ
B��Na2S��Һ
C��CuSO4��Һ
D��ϡH2SO4
�ο��𰸣�B
���������A������PbS������B������NaHS��C������CuS������D�в���Ӧ����ѡB��2S������
������������ʶ����֪ʶ�Ŀ��飬�ص㿼��ѧ����H2S���ʵ���Ϥ�˽�̶ȣ�ּ�ڿ���ѧ��������û���֪ʶ���ʵ��������������ѶȲ���������ס����������ü��ɡ�
�����Ѷȣ�һ��
2��ʵ���� ijУ������ѧ�о���ѧϰС�飬��ѧϰ��ͭ��Ũ����ķ�Ӧ��ֱ�̽��������п��Ũ���ᷴӦ�Ĺ��̡���С���������ͼװ�ã��Իش�

(1)��Ӽס�����ѡ����ʵ�װ������B��C�У���������ȷ���ӣ�a��______, c��______(����ű�ʾ����
(2)D��E��֧�Թ���CCl4��������______��
(3)��ʵ����֤��Ũ�������ǿ�����Ե�ʵ������Ϊ______��
(4)D�г��ֻ��ǵ����ӷ���ʽΪ______��
(5)ijѧ��ע��۲쵽��ʵ�鿪ʼ��C��D��E�о������ݲ�����������������٣�Ʒ����Һ��ɫ��D�г��ֻ��ǣ���Ӧһ��ʱ���C��D��E�е��������ֻ��������ӡ����û�ѧ����ʽ��ʾ����Ӧһ��ʱ����������ֻ��������ӡ���ԭ����______��
��С���������ͼװ�ã�

(6)��������С��������ͼ��______��
(7)װ��B�е�ҩƷ��______��
(8)��֤������SO2��H2�Ⱥ�˳���ʵ��������______��
�ο��𰸣���15�֣�(1) 3(��4)?2����1�֣���2�֣� (2) ��������2�֣�
(3) C��Ʒ����Һ��ɫ��2�֣�
(4) Ca2+��2OH-��SO2===CaSO3��+H2O��2�֣�
(5) Zn+H2SO4��ϡ����?ZnSO4+H2����2�֣�
(6) ��֤�������Ȳ���ˮ��SO2�������H2��2�֣����������𰸲��ո��֣�
(7) ��ˮCuSO4(����ˮ����ͭ) ��1�֣�
(8) C��Ʒ����ɫ��D�����Ը��������ɫ���ٱ�dz��F�й����ɺ�ɫ���ɫ��G����ˮ����ͭ������2�֣����������𰸲��ո��֣�
�����������1������ͭ��Ũ���ᷴӦ�ķ���ʽ��֪��п��Ũ���ᷴӦ�ķ���ʽΪZn+2H2SO4��Ũ���TZnSO4+SO2��+2H2O������ͨ��״���£�1���ˮ�п��ܽ�40����Ķ����������壬���װ���ҿɷ�ֹ����������Ʒ������ʱ������п�����ᷴӦ�������У�����������Ʒ�����ã��賤�ܽ���������ȷ������˳����3����4����4����3����b��c��2��1��d��
��2����������������ˮ�����������Ȼ�̼����������ͨ�����Ȼ�̼��Ȼ����������ʯ��ˮ��Ӧ�������ã��ɷ�ֹ������
��3�����������ʹƷ����Һ��ɫ�������ڼ����������Ĵ��ڣ����Ա�ʵ����֤��Ũ�������ǿ�����Ե�ʵ������ΪC��Ʒ����Һ��ɫ��
��4����������ͳ����ʯ��ˮ��Ӧ����������ƺ�ˮ���������Ϊ������ˮ�ij�������Ӧ�����ӷ���ʽΪCa2++2OH-+SO2�TCaSO3��+H2O��
��5��пΪ�ϻ��õĽ������ڽ����˳������������ǰ�棬����п�ܺ�ϡ���ᷴӦ��������п�������������ŷ�Ӧ�Ľ��У�Ũ�����Ũ�����ͣ�����Ϊϡ�������п��Ӧ������������Ӧ�Ļ�ѧ����ʽΪZn+H2SO4��ϡ���TZnSO4+H2����
��6������װ��ͼ��֪����С����Ƶ�װ�ã����ð�ɫ����ˮ����ͭ����ˮ�Ĵ��ڣ�����Ʒ������������Ĵ��ڣ��ø�������������������ȥ��������Ũ���������ˮ�ԣ���ȥˮ��п��ϡ���ᷴӦ��������������п������ͨ���ȵ�����ͭ����ͭ��ˮ��ˮ��������ˮ����ͭ����ɫ���ɼ��������Ĵ��ڣ���˸���Ƶ�Ŀ������֤�������Ȳ���ˮ��SO2�������H2��
��7����������ͨ����Һʱһ�������ˮ����������Ҫ���ȼ���ˮ����������ˮ��������ˮ����ͭ����ɫ��֪��װ��B�е�ҩƷ����ˮCuSO4������ˮ����ͭ������������ˮ�Ĵ��ڡ�
��8�����������ʹƷ����Һ��ɫ��C��Ʒ����ɫ���ɼ����������Ĵ��ڡ�SO2�����л�ԭ�ԣ��������������������ɳ�ȥ��������D�����Ը�����ز�����ɫ��˵�����������Ѿ�������п��ϡ���ᷴӦ��������������п������ͨ���ȵ�����ͭ����ͭ��ˮ��F���к�ɫ�������ɣ�˵����ͭ���ɣ�G����ˮ����ͭ������˵����ˮ���ɣ���֤��������������
�����Ѷȣ�һ��
3��ѡ���� ���Т�HSO3������S2������SO32������HS������������Һ���������Һ�зֱ��������NaOH��������Ũ���ᣬ�������Ը��������Һ����������Ŀ�����ٵ���?
A���٢�
B��ֻ�Т�
C��ֻ�Т�
D���ڢ�
�ο��𰸣�A
���������������ȼ����������ƣ��������������ƣ�Ȼ��������ᣬ������SO2���壬������Һ��������Ŀ���٣������Ӻ��������Ʋ���Ӧ�����������������������Ʒ�Ӧ�����������Ը��������Һ�������������ӣ�����SO42����������Ŀ���䣻ͬ����������������Ŀ���䣻������ȼ����������ƣ����������ƣ�Ȼ��������ᣬ������H2S���壬������Һ��������Ŀ���٣���ѡA��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣�����ۺ���ǿ����ע�ض�ѧ��������֪ʶ���̺�ѵ����ͬʱ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ��������������ѧ�������������������ѧ��������û���֪ʶ���ʵ�������������
�����Ѷȣ���
4��ѡ���� X��Y��Z��W����ͼ��ʾ��ת����ϵ����X��Y�����ǣ�?��

��C��CO����AlCl3��Al(OH)3����N2��NO����S��SO2����NaOH��Na2CO3
A���٢ڢ�? B���ڢۢ�? C���ۢ�?D���٢ڢ�
�ο��𰸣�A
�����������ת����ϵΪC��CO��CO2��C��CO2���ʢ���ȷ����ת����ϵΪAlCl3��Al(OH)3��NaAlO2��AlCl3��NaAlO2���ʢ���ȷ����N2��O2��Ӧ����NO��NO��O2��Ӧ����NO2��N2����һ����Ӧ����NO2���ʢ۴��ܶ��������ڴ���������������������������һ����Ӧ�����������ʢܴ���ת����ϵΪNaOH��Na2CO3��NaHCO3��NaOH��NaHCO3���ʢ���ȷ��
�����Ѷȣ�һ��
5������� ���Ṥҵ����Ӧ�����ۺϾ���Ч�����⡣
��1���ݲ��㣬�Ӵ�������������У�����Ӧ�ȶ�δ�����ã���ÿ����1 t 98%������������3.6��105 kJ����������ͨ�������жϣ�����ӦSO2(g)+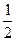 O2��g��
O2��g�� SO3����H="-98.3" kJ��mol-1�ų��������������������еõ�������ã���ÿ����1 t 98%������ֻ������ṩ�������������������ǧ����������H2SO4��Ħ������Ϊ98 g��mol-1��
SO3����H="-98.3" kJ��mol-1�ų��������������������еõ�������ã���ÿ����1 t 98%������ֻ������ṩ�������������������ǧ����������H2SO4��Ħ������Ϊ98 g��mol-1��
��2��CuFeS2�ǻ��������һ�ɷ֣�ȼ��ʱ��CuFeS2ת��ΪCuO��Fe2O3��SO2���÷�Ӧ�Ļ�ѧ����ʽΪ?��
��3�����᳧����¯�ų��Ŀ����к���Fe2O3��CuO��CuSO4����CuO��SO3�ڷ���¯�л��϶��ɣ�����������ͭ���������������¯�¶ȵIJ�ͬ���仯�����±�����
����¯�¶�/��
| 600
| 620
| 640
| 660
|
������CuSO4����������/%
| 9.3
| 9.2
| 9.0
| 8.4
|
��֪CuSO4�ڵ���660 ��ʱ����ֽ⣬���Ҫ�����ϱ���CuSO4�������������¶����߶����͵�ԭ��?��
�ο��𰸣���1��6.23��105 kJ������
��2��4CuFeS2+13O2 4CuO+2Fe2O3+8SO2
4CuO+2Fe2O3+8SO2
��3��SO2ת��ΪSO3������Ӧ���ȵĿ��淴Ӧ�����¶ȵ����ߣ�ƽ�����淴Ӧ�����ƶ���SO3�����ʵ������٣�����CuSO4��������
�����������1��SO2~SO3~H2SO4?�ų�������
98 g? 98.3 kJ
1��106��98% g?x
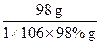 =
=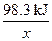
x=9.83��105 kJ
9.83��105 kJ-3.6��105 kJ=6.23��105 kJ
���Կ���������6.23��105 kJ������
��2��4CuFeS2+13O2 4CuO+2Fe2O3+8SO2
4CuO+2Fe2O3+8SO2
��3��SO2ת��ΪSO3������Ӧ���ȵĿ��淴Ӧ�����¶ȵ����ߣ�ƽ�����淴Ӧ�����ƶ���SO3�����ʵ������٣�����CuSO4��������
�����Ѷȣ���