微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 天然气、液化石油气燃烧的化学方程式分别为:CH4 +2O2 CO2+2H2O, C3H8+5O2
CO2+2H2O, C3H8+5O2 3CO2+4H2O。现有一套以天然气为燃料的灶具,欲改烧液化石油气,应采取的正确措施是
3CO2+4H2O。现有一套以天然气为燃料的灶具,欲改烧液化石油气,应采取的正确措施是
[? ]
A.两种气体进入量都减少
B.增大空气进入量或减小液化气进入量
C.两种气体进入量都增大
D.减小空气进入量或增大液化气进入量
参考答案:B
本题解析:
本题难度:简单
2、填空题 由固体碱熔氧化法可制备重铬酸钾,已知精选后的铬铁矿主要成分是亚铬酸铁[Fe(CrO2)2或
FeO・Cr2O3],还含有硅、铝的氧化物等杂质。
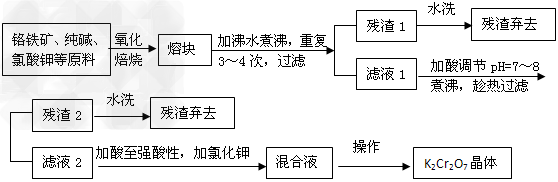
(1)若氧化焙烧在实验室进行,所用的主要仪器是______(填序号,下同);蒸发浓缩时所用的主要仪器是_______。
A.蒸发皿?B.普通坩埚?C.铁坩埚
(2)氧化焙烧时,发生重要反应的化学方程式有:
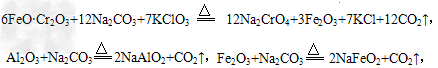 ?
?
以及:__________________。
(3)用水浸取熔块时,NaFeO2强烈水解,生成氢氧化铁沉淀而除去,试写出离子方程式: __________________________________。
(4)残渣2的主要成分有(填化学式)___________、_____________。
(5)已知K2Cr2O7和NaCl两种物质的溶解度随温度变化变化如下
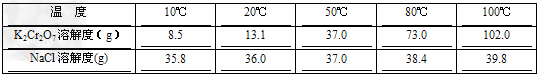
则最后一步由混合液转变成K2Cr2O7晶体的操作是_______、_______、过滤、洗涤、烘干。
参考答案:(1)C;A
(2)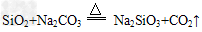
(3)FeO2-+?2H2O?=?Fe(OH)3↓?+?OH-
(4)Al(OH)3;H2SiO3
(5)蒸发浓缩;冷却结晶
本题解析:
本题难度:一般
3、选择题 最近,我国从新疆开发天然气,通过管道输送到上海等东部城市,下列有关天然气的说法中不正确的是( )
A.天然气和沼气的主要成分都是甲烷
B.用液化石油气主要成分为丙烷的炉具与用天然气的炉具不能通用,需要调整和更换
C.天然气是比燃油更清洁的燃料,产物污染少
D.用天然气替代汽油作为汽车燃料,是因为使用起来更方便
参考答案:D
本题解析:
本题难度:一般
4、填空题 为回收利用废钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,主要流程如下:
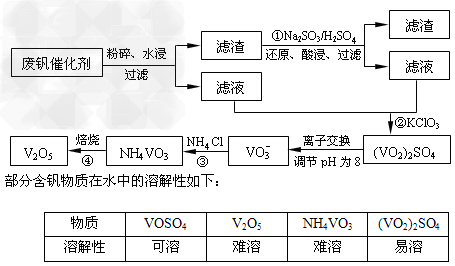
回答下列问题:
(1)工业由V2O5冶炼金属钒常用铝热剂法,该反应的氧化剂为_____________。
(2)滤液中含钒的主要成分为______________(填化学式)。
(3)该工艺中反应③的沉淀率(又称沉钒率)是回收钒的关键之一,该步反应的离子方程式?______________;沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度。根据下图判断最佳控制氯化铵系数和温度为___________、_________℃。
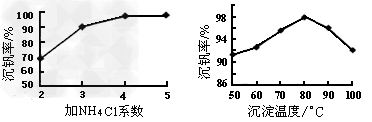
(4)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应②后溶液中含钒量,反应方程式为:2VO2++H2C2O4+2H+?=?2VOn+?+?2CO2↑+?mH2O,其中n、m分别为______________、________?。
(5)全矾液流电池的电解质溶液为VOSO4溶液,电池的工作原理为:VO2++?V2++?2H+ VO2++H2O+V3+,电池放电时正极的电极反应式为___________。
VO2++H2O+V3+,电池放电时正极的电极反应式为___________。
参考答案:(1)V2O5
(2)VOSO4
(3)NH4++VO3-?==?NH4VO3↓;4;80
(4)2;2
(5)VO2++?2H++e-==?VO2++H2O
本题解析:
本题难度:一般
5、填空题 (三选一)【化学--选修2:化学与技术】
现有一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高。其主要流程如下
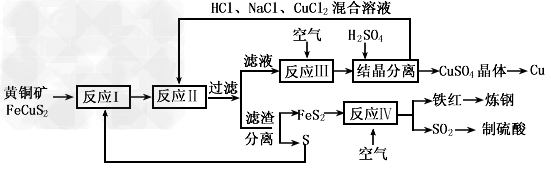
注:反应II的离子方程式为 ?
?
请回答:
(1)?从黄铜矿冶炼粗铜的传统丁艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜、这种方法的缺点是__________________________________
(2)?反应I的产物为(填化学式)?________________________________
(3)?反应III的离子方程式为________________________________
(4)?一定温度下,在反应III所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,其原因是_______________________
(5)?黄铜矿中Fe的化合价为+2,关于反应:
下列说法正确的是______________?(填选项字母)
A. 反应中被还原的元素只有氧
B. 反应生成的SO2直接排放会污染环境
C. SO2既是氧化产物又是还原产物
D. 当有8mol铜生成时,转移电子数目为100?NA
(6)?某硫酸厂为测定反应IV所得气体中SO2的体积分数,取280mL(已折箅成标准状况)气体样品与足量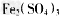 溶液完全反应后,用浓度为0.02000?mol/L?的?K2Cr2O7标准溶液滴定至终点,消耗?K2Cr2O7溶液25.00ml. 已知:
溶液完全反应后,用浓度为0.02000?mol/L?的?K2Cr2O7标准溶液滴定至终点,消耗?K2Cr2O7溶液25.00ml. 已知: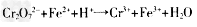 (未配平)
(未配平)
①SO2通入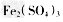 溶液,发生反应的离子方程式为________________________,
溶液,发生反应的离子方程式为________________________,
②反应IV所得气体中SO2的体积分数为________________
参考答案:(1)反应有SO2生成,易造成环境污染,同时消耗大量热能
(2)CuS、FeS2
(3)4[CuCl2]-?+O2+4H+=4Cu2+?+8Cl-+2H2O
(4)该温度下,硫酸铜的溶解度小于氯化铜
(5)BCD
(6)①?SO2+2Fe3++2H2O=SO42-+2Fe2++4H+;②?12.00?%
本题解析:
本题难度:一般